रासायनिक ऊर्जा उदाहरण
रसायन विज्ञान / / July 04, 2021
रासायनिक ऊर्जा वह है जो रासायनिक प्रतिक्रियाओं से आती है. रासायनिक प्रजातियों के बीच परस्पर क्रिया टूटना और / या बंधनों का निर्माण करती है, जिसका अर्थ है क्रमशः ऊर्जा का विमोचन या अवशोषण। रासायनिक ऊर्जा को विमोचित ऊर्जा कहा जाता है, जिसका उपयोग तापीय ऊर्जा और विद्युत ऊर्जा के रूप में किया जा सकता है, उदाहरण के लिए।
रासायनिक प्रतिक्रियाओं में ऊर्जा
रासायनिक ऊर्जा को इसकी अधिकतम अभिव्यक्ति में दो मुख्य स्रोतों से प्राप्त किया जा सकता है: दहन और इलेक्ट्रोलाइटिक समाधान। दूसरी ओर, मानव शरीर के स्तर पर, भोजन के रासायनिक विघटन के माध्यम से ऊर्जा प्राप्त करना संभव है।
दहन ऊर्जा
उदाहरण के लिए, जब ईंधन मीथेन CH4सबसे सरल हाइड्रोकार्बन, ऑक्सीजन ऑक्सीडाइज़र की उपस्थिति में जलने लगता है, यह विघटित होकर कार्बन डाइऑक्साइड CO उत्पाद बनाता है।2 और पानी एच2या। इसके अलावा, कार्बन परमाणुओं के साथ हाइड्रोजन परमाणुओं के बंधनों को तोड़ने से गर्मी के रूप में ऊर्जा निकलती है।
चौधरी4 (जी) + 2O2 (जी) → सीओ2 (जी) + 2H2 हे (एल) H = -212.8 किलो कैलोरी / मोल
मीथेन दहन समीकरण। इस अभिक्रिया की ऊष्मा को H द्वारा निरूपित किया जाता है। नकारात्मक संकेत ऊर्जा की रिहाई को इंगित करता है। प्रतिक्रिया एक्ज़ोथिर्मिक है।
 मीथेन गैस का दहन। प्रतिक्रिया एक लौ के साथ प्रकट होती है।
मीथेन गैस का दहन। प्रतिक्रिया एक लौ के साथ प्रकट होती है।
25 डिग्री सेल्सियस पर कार्बनिक यौगिकों के दहन के उदाहरण।
यौगिक |
सूत्र |
ΔH (Kcal / mol) |
मीथेन (जी) |
चौधरी4 |
-212.80 |
ईथेन (जी) |
सी2एच6 |
-372.82 |
प्रोपेन (जी) |
सी3एच8 |
-530.60 |
एन-ब्यूटेन (जी) |
सी4एच10 |
-687.98 |
एन-पेंटेन (जी) |
सी5एच12 |
-845.16 |
एथिलीन (जी) |
सी2एच4 |
-337.23 |
एसिटिलीन (जी) |
सी2एच2 |
-310.62 |
बेंजीन (जी) |
सी6एच6 |
-787.20 |
बेंजीन (एल) |
सी6एच6 |
-780.98 |
टोल्यूनि (एल) |
सी7एच8 |
-934.50 |
नेफ़थलीन (ओं) |
सी10एच8 |
-1,228.18 |
सुक्रोज |
सी12एच22या11 |
-1,348.90 |
मेथनॉल (एल) |
चौधरी3ओह |
-173.67 |
इथेनॉल (एल) |
सी2एच5ओह |
-326.70 |
एसिटिक एसिड (एल) |
चौधरी3कूह |
-208.34 |
बेंजोइक एसिड (ओं) |
सी6एच5कूह |
-771.20 |
एक ईंधन के लिए दहन की सभी ऊष्मा प्रदान करने के लिए जिसमें वह सक्षम है, उसे गैसीय अवस्था में होना चाहिए. जैसा कि तालिका में देखा जा सकता है, तरल बेंजीन दहन की गर्मी का योगदान देता है जो गैसीय बेंजीन द्वारा जारी की तुलना में 6.22 किलो कैलोरी / मोल कम है। इसका मतलब है कि तरल से गैस में परिवर्तन करने के लिए 6.22 किलो कैलोरी / मोल का निवेश किया जाना चाहिए।
पर अधिक जानकारी के लिए क्लिक करें ईंधन.
इलेक्ट्रोलाइटिक समाधान ऊर्जा
इलेक्ट्रोलाइटिक कंडक्टर एक ऐसा माध्यम है जिसमें एक या एक से अधिक आयनिक प्रजातियां शामिल होती हैं, जो है अपने विद्युत आवेश के साथ छितराया हुआ, एक विद्युत प्रवाह को इसके माध्यम से गुजरने की अनुमति देता है संविधान। इलेक्ट्रोलाइटिक समाधान इलेक्ट्रोलाइटिक कंडक्टर हैं।
इलेक्ट्रोलाइटिक कंडक्टरों में शामिल हैं, इलेक्ट्रोलाइट समाधान के अलावा, पिघला हुआ लवण, और कुछ ठोस लवण, जैसे सोडियम क्लोराइड NaCl, और सिल्वर नाइट्रेट अग्नि3.
इलेक्ट्रॉन स्थानांतरण आयनिक प्रवास द्वारा होता है, सकारात्मक और नकारात्मक, इलेक्ट्रोड की ओर। इस प्रवास में न केवल बिजली का हस्तांतरण शामिल है, बल्कि कंडक्टर के एक हिस्से से दूसरे हिस्से में पदार्थ का परिवहन भी शामिल है।
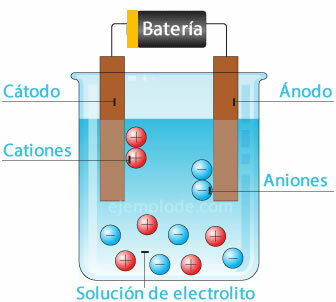 विद्युत रासायनिक सेल
विद्युत रासायनिक सेल
एक संभावित स्रोत को धात्विक इलेक्ट्रोड (कैथोड और एनोड) से जोड़ना, और इन्हें a. में डुबाना जलीय घोल, इलेक्ट्रान एनोड के माध्यम से यात्रा करेंगे, समाधान से सकारात्मक ध्रुव तक बचने के लिए झरना। यह मामला है, उदाहरण के लिए, क्लोराइड आयन के साथ, जो अपने इलेक्ट्रॉन से मुक्त होता है, और पहले से ही एक तटस्थ चार्ज के साथ, यह डायटोमिक अणु बनाने के लिए एक और क्लोरीन परमाणु से जुड़ता है। घोल से क्लोरीन गैस निकल जाएगी।
2Cl- = 2Cl + 2e-
स्रोत के ऋणात्मक ध्रुव को छोड़ने वाले इलेक्ट्रॉनों को जलमग्न कैथोड में रखा जाएगा। जलीय विलयन (आयनों) में उपस्थित जातियाँ कैथोड से इलेक्ट्रॉन ग्रहण करेंगी। उदाहरण के लिए, पानी बनाने वाले हाइड्रोजन आयन, धनात्मक आवेश में होने के कारण, एक इलेक्ट्रॉन को निष्क्रिय करने के लिए, और अणु बनाने के लिए एक अन्य हाइड्रोजन परमाणु के साथ जुड़ गया द्विपरमाणुक यह विलयन से हाइड्रोजन गैस के रूप में निकलेगा।
2 एच+ + 2e- = 2H
2एच = एच2 (छ)
इलेक्ट्रॉनों का यह आदान-प्रदान कार बैटरी के संचालन का समर्थन कर सकता है, जिसमें सल्फ्यूरिक एसिड एच के समाधान में डूबे हुए लीड पीबी इलेक्ट्रोड होते हैं।2दप4.
घरेलू स्तर पर संचालित सभी प्रकार की बैटरी में यही ऊर्जा प्राप्त होती है: 9वी, एए, एएए, डी, कुछ उदाहरण देने के लिए।
खाद्य ऊर्जा
मनुष्य अपने शरीर में खाने वाले भोजन को विघटित करके जो ऊर्जा निकलती है उसे आत्मसात कर लेते हैं। यह ऊर्जा वह है जो हमारा शरीर अचेतन कार्यों (पाचन, दिल की धड़कन, सेलुलर कार्यों) के लिए उपयोग करता है और जिन्हें हम करते हैं।
जब तक आप तीव्र शारीरिक गतिविधि नहीं करते हैं और आपका चयापचय धीमा है, तब तक नियमित रूप से कैलोरी का सेवन करने की सलाह दी जाती है, क्योंकि उच्च खाद्य पदार्थ जटिल लिपिड और कार्बोहाइड्रेट, जिनमें बहुत बड़ी संरचनाएं होती हैं, को तोड़ना अधिक कठिन होता है, जिसके परिणामस्वरूप का उलटा होता है ऊर्जा। उस स्थिति में प्रभाव क्षण भर में विपरीत होगा।
रात में काम करते समय फलों का सेवन करने की सलाह दी जाती है, क्योंकि फल में फ्रुक्टोज होता है, एक साधारण कार्बोहाइड्रेट जिसे तोड़ना आसान है और आपके बाद हमें ऊर्जा उपलब्ध होगी खपत।
रासायनिक ऊर्जा और उसके परिवर्तन
थर्मोइलेक्ट्रिक प्लांट
थर्मोइलेक्ट्रिक संयंत्रों में उच्च और लंबे समय तक चलने वाले ऊष्मीय मान के लिए भारी ईंधन का उपयोग किया जाता है। आम तौर पर यह ईंधन तेल (ईंधन तेल) होता है। दहन, जो प्रक्रिया का रासायनिक चरण है, बॉयलर के लिए एक हीटिंग एजेंट के रूप में काम करेगा, जो संतृप्त भाप उत्पन्न करेगा। यह भाप भाप वितरण नेटवर्क के माध्यम से दबाव में बाहर आएगी और जनरेटर के टर्बाइनों को स्थानांतरित करना शुरू कर देगी। ये उपकरण संबंधित आबादी की आपूर्ति के लिए विद्युत ऊर्जा का उत्पादन करेंगे।
रासायनिक ऊर्जा → यांत्रिक ऊर्जा → विद्युत ऊर्जा
ऑटोमोटिव ऑपरेशन
कारें शक्ति के स्रोत पर निर्भर करती हैं, जो कि बैटरी है। बैटरी में, इलेक्ट्रोलाइटिक चालन पहले से ही होने के लिए जाना जाता है, इग्निशन सिस्टम, डैश एक्सेसरीज़ और सहायक पावर आउटलेट को सशक्त बनाता है। इस उपलब्ध बिजली के लिए धन्यवाद, कार चालक को वांछित स्थान पर ले जाने में सक्षम होगी।
रासायनिक ऊर्जा → विद्युत ऊर्जा → यांत्रिक ऊर्जा



