चार्ल्स के नियम का उदाहरण
भौतिक विज्ञान / / July 04, 2021
चार्ल्स का गैस नियम या स्थिर दाब का नियम, गैस के अन्य नियमों में से एक है, जैक्स चार्ल्स के काम को जारी करने वाले गे-लुसाक द्वारा प्रतिपादित, लगभग 20. प्रकाशित हुआ वर्षों पूर्व।
चार्ल्स का नियम गैस के द्रव्यमान के व्यवहार की भविष्यवाणी करता है जब दबाव स्थिर रहता है और तापमान और आयतन बदलता रहता है।
चार्ल्स का नियम इस प्रकार बताया गया है:
स्थिर दाब पर किसी गैस का आयतन उसके तापमान में परिवर्तन के समानुपाती होता है।
निरंतर दबाव: इस तथ्य को संदर्भित करता है कि कंटेनर की दीवारों पर गैस का दबाव पूरे अनुभव में भिन्न नहीं होगा।
आयतन: यह कब्जा की गई जगह है जिस पर गैस रहती है, सामान्य तौर पर इसे दीवारों के साथ एक कंटेनर माना जाता है जो विकृत नहीं होता है, और जिसका ढक्कन एक सवार की तरह काम करता है।
तापमान: यह गर्मी की वृद्धि या हानि है जो प्रयोग के दौरान गैस से गुजरती है। यदि तापमान बढ़ता है, तो मात्रा बढ़ जाती है। यदि तापमान कम हो जाता है, तो मात्रा भी घट जाती है।
बीजगणितीय रूप से, चार्ल्स का नियम निम्नलिखित सूत्र द्वारा व्यक्त किया जाता है:

कहा पे:
वी = गैस की मात्रा
टी = गैस तापमान
k = गैस के उस द्रव्यमान के लिए आनुपातिकता का स्थिरांक।
इसका मतलब है कि गैस के दिए गए द्रव्यमान के लिए, निरंतर दबाव में, आयतन और के बीच संबंध तापमान भिन्नता, हमेशा समान आनुपातिक संबंध होगा, जिसे स्थिरांक द्वारा दर्शाया गया है क:

इसलिए एक बार स्थिरांक निर्धारित हो जाने के बाद, हम अन्य ज्ञात डेटा से किसी अन्य मान की गणना कर सकते हैं:
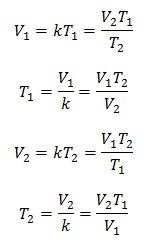
समस्याओं पर लागू चार्ल्स के नियम के 3 उदाहरण:
उदाहरण 1: नए आयतन की गणना करें, यदि एक कंटेनर में 280 K के तापमान पर 1.3 लीटर की मात्रा में गैस का द्रव्यमान है। 303 K के तापमान तक पहुँचने पर आयतन की गणना करें।
वी1 = 1.3 एल।
टी1 = 280 के
वी2 = ?
टी2 = ३०३ के
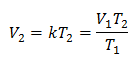
मूल्यों को प्रतिस्थापित करना:
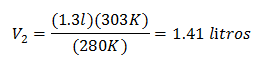
303 K पर नया वॉल्यूम 1.41 लीटर है।
उदाहरण 2. यदि हमारे पास 10 डिग्री सेल्सियस पर 2.4 लीटर गैस है, तो अंतिम तापमान की गणना करें, यदि अंत में यह 2.15 लीटर है।
वी1 = २.४ एल
टी1 = 10 डिग्री सेल्सियस = 283 के
वी2 = २.१५ लीटर
टी2 = ?
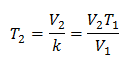
मूल्यों को प्रतिस्थापित करना:
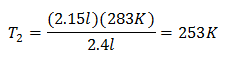
नया तापमान 253 K है, जो -20 डिग्री सेल्सियस के बराबर है।
उदाहरण 3. हमारे पास एक गैस है जिसका प्रारंभिक तापमान 328 K है, इसका अंतिम आयतन 3.75 l है, और इसका अनुपात स्थिरांक 0.00885 है।
वी1 = ?
टी1 = ३२८ के
वी2 = 3.75 एल
टी2 = ?
कश्मीर = 0.00885
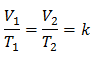
मूल्यों को प्रतिस्थापित करना:
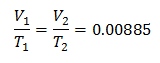
प्रारंभिक मात्रा जानने के लिए:
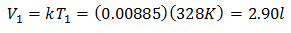
प्रारंभिक मात्रा 2.90 एल है।
अंतिम तापमान जानने के लिए:
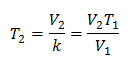
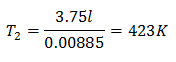
अंतिम तापमान 423 K होगा, जो कि 150 ° C के बराबर है।
