50 Primjeri kiselina i baza
Miscelanea / / July 04, 2021
U polju kemija, se zovu baze (ili hidroksidi) na tvari koje kad se otope u vodi oslobađaju hidroksilne ione (OH–) i nazivaju se kiseline tvari koje su sposobne otpuštati protone (H+) u vodenoj otopini. Na primjer: sumporna kiselina, dušična kiselina, kalcijev hidroksid, kalijev hidroksid.
Klasifikacija kiselina i baza
Prema njihovoj tendenciji disocijacije na ione, kiseline i baze klasificiraju se na:
Kiseline se smanjujupH otopina, baze ili lužine ga podižu. Jake kiseline često su nagrizajuće, neke se tvari bolje otapaju u podlogama koje su blago zakiseljene ili alkalizirane.
Primjeri kiselina
Neke poznate kiseline su:
- Sumporna kiselina (H2SW4). Jaka je kiselina za mnoge namjene, posebno u teška industrija, vrlo nagrizajuće i iritantno. Kada se razrijedi, oslobađa puno topline, pa se s njom mora rukovati (kao i s ostalim jakim kiselinama) s velikom pažnjom. Intenzivno oksidira.
- Klorovodična kiselina (HCl). Iako je jaka kiselina, prisutna je u ljudskom tijelu, posebno u želucu, gdje igra važnu ulogu u probavnom procesu. Njegov višak stvara žgaravicu.
- Fosforna kiselina (H3PO4). Ova je kiselina čest sastojak gaziranih pića. Redovita se konzumacija takvih pića ne preporučuje zbog negativnog utjecaja ove kiseline na metabolizam kalcija, što utječe kosti a posebno zubi.
- Dušična kiselina (HNO3). Priznata je jaka kiselina, koja se koristi za proizvodnju eksploziva i dušičnih gnojiva, među ostalim.
- Klorovodična kiselina (HClO4). To je jaka kiselina, tekućina a temperatura okoliš. Jedan je od najoksidirajućih.
- Vodikov sulfid (H2S). To je plinovita tvar snažnog i neugodnog mirisa, otrovna u visokim koncentracijama. Ima brojne industrijske primjene.
- Ribonukleinska kiselina. To je središnja komponenta ribosoma, neophodna za završetak globalnog procesa sinteze proteina iz deoksiribonukleinske kiseline.
- Acetilsalicilna kiselina. To je vrlo važna organska kiselina, s analgetskim i protuupalnim svojstvima. To je osnova aspirina.
- Mliječna kiselina. Dolazi iz razgradnje glukoze tijekom anaerobnih vježbi visokog intenziteta i kratkog trajanja. U normalnim uvjetima ova se mliječna kiselina ponovno koristi, ali ako se akumulira, uzrokuje oštećenje mišićnih vlakana, što prije svega uzrokuje grčeve.
- Alilična kiselina. To je kiselina prisutna u povrću poput češnjaka ili luka, a potječe od prekursora koji je također prisutan u takvim vrstama, alicina. Djeluje mikrobiološki i antioksidativno.
- Retinoična kiselina. Lokalno primijenjen, inhibira keratinizaciju, koristi se u kremama protiv akni i starenja kože. Treba ga koristiti pod liječničkim nadzorom.
- Maslačna kiselina. Krajnji je proizvod vrenje nekih ugljikohidrata koje provodi mikroorganizmi buraga. Obično je dio masti životinje u malim količinama.
- Propionska kiselina. Konzervans je hrane, koristi se kako bi se spriječilo gljivično i bakterijsko kvarenje pekarskih proizvoda i drugih.
- Benzojeva kiselina. Koristi se kao konzervans koji se dodaje različitim proizvodima (majoneza, konzervirana roba), često u obliku soli (natrijev benzoat).
- Octena kiselina (CH3COOH). Konzervans je hrane koji se široko koristi u kući, također kao osnova za vinaigrete i kisele krastavce. Većinski je sastojak octa.
- Jodovodična kiselina (HI(izmjenično)). To je jaka kiselina koja se može koristiti za povećanje razine joda u Izađi van.
- Jantarna kiselina (C4H6ILI4). To je kristalna krutina koja se može dobiti iz jantara. Može se stvoriti u procesu fermentacije vina i piva.
- Bromovodična kiselina (HBr(izmjenično)). To je vrlo nagrizajuća jaka kiselina. Njegova reakcija s bazama vrlo je burna, a također je iritantna. Koristi se u kemijskoj i farmaceutskoj industriji.
- Limunska kiselina (C6H8ILI7) To je organska kiselina koja obiluje voćem. Prirodni je antioksidans.
- Oksalna kiselina (H2C2ILI4). To je organska kiselina koja se prirodno nalazi u bilje. Koristi se u pčelarstvu za suzbijanje bolesti kod pčela. Također se koristi za proizvodnju proizvoda za čišćenje, u tekstilnoj industriji, između ostalog.
Primjeri osnova
Metalne baze su općenito poznate kao hidroksidi. Neke su baze:
- Natrijev hidroksid (NaOH, kaustična soda). Snažna je baza koja se koristi u industriji papira i u proizvodnji deterdženata. U svakodnevnom životu koristi se za odčepljivanje cijevi u kupaonici i kuhinji.
- Magnezijev hidroksid (Mg (OH)2, mlijeko magnezija). To je snažna baza koja se ponekad koristi kao antacid ili laksativ.
- Kalcijev hidroksid (Ca (OH)2, vapno). Poznat i kao hidratizirano vapno, koristi se u metalurškoj i naftnoj industriji. Također se koristi za proizvodnju pesticida, među ostalim u industriji šećera i mliječnih proizvoda.
- Kalijev hidroksid (KOH). To je jaka i korozivna baza koja se široko koristi u različitim industrijama. Široko se koristi za izradu sapuna.
- Barijev hidroksid (Ba (OH)2). Zbog svoje toksičnosti koristi se za stvaranje otrova. Također se koristi u industriji keramike, u industriji papira i u procesu rafiniranja šećera.
- Željezo II ili III hidroksid (Fe (OH)2 ili Fe (OH)3). Obično se generira kao dio metalurške industrije. Koristi se u proizvodnji boja, između ostalog.
- Amonijak (NH3). To je plin karakterističnog mirisa. Od njega se izrađuju gnojiva i mnogi lijekovi. Vrlo je opasno ako se udiše u velikim dozama.
- Sapun. To je natrijeva ili kalijeva sol. Koristi se za osobnu i opću higijenu.
- Deterdžent. Također je široko korišten higijenski proizvod.
- Kinin. Prirodna je baza koju proizvode neke biljke. Ima antipiretička i analgetička svojstva. U davna vremena koristila se za liječenje malarije.
- Anilin. Otrovni je spoj kad se proguta ili udiše. Koristi se u gumarskoj industriji, među ostalim u proizvodnji herbicida i eksploziva.
- Guanine. Jedna je od dušičnih baza koje su dio nukleinskih kiselina (DNA i RNA).
- Pirimidin. Dušične baze koje čine nukleinske kiseline potječu od pirimidina.
- Citozin. Jedna je od dušičnih baza koje su dio nukleinske kiseline.
- Adenin. Jedna je od dušičnih baza koje su dio nukleinskih kiselina.
- Cink hidroksid (Zn (OH)2). Amfoterna je tvar (može djelovati i kao kiselina i kao baza). Otrovna je tvar ako dolazi u kontakt s očima ili kožom. Koristi se u procesu proizvodnje kirurških obloga.
- Bakreni hidroksid (Cu (OH)2). Koristi se kao fungicid i za bojanje keramičkih predmeta. Također se koristi kao katalizator za neke kemijske reakcije.
- Cirkonijev hidroksid IV (Zr (OH)4). Koristi se u industriji keramike i stakla.
- Berilijev hidroksid (Be (OH)2). Ima amfoterna svojstva. Koristi se u industriji za dobivanje metalnog berilija. To je tvar ograničenog obilja.
- Aluminijev hidroksid (Al (OH)3, antacid). U medicini se koristi kao antacid i pomoćno sredstvo cjepivima.
Teorije o kiselinama i bazama
Koncept baza i kiselina mijenjao se tijekom vremena. Bilo je Arrhenius koji je izradio prvu definiciju koja definira kiselinu kao tvar koja daje H ione u vodenoj otopini+, i na bazu kao što je tvar koja u vodenoj otopini odustaje od OH iona–. Njegova je teorija imala određena ograničenja, jer se određene tvari (poput amonijaka) ponašaju kao baze, a nemaju ih molekula na hidroksilni ion.
Uz to, Arrhenius je tvari razmatrao samo u vodenom mediju, ali kiselinsko-bazne reakcije se javljaju i u drugim medijima. otapanje ne vodeni. Prikaz kiseline i baze prema Arrheniusovoj teoriji je:
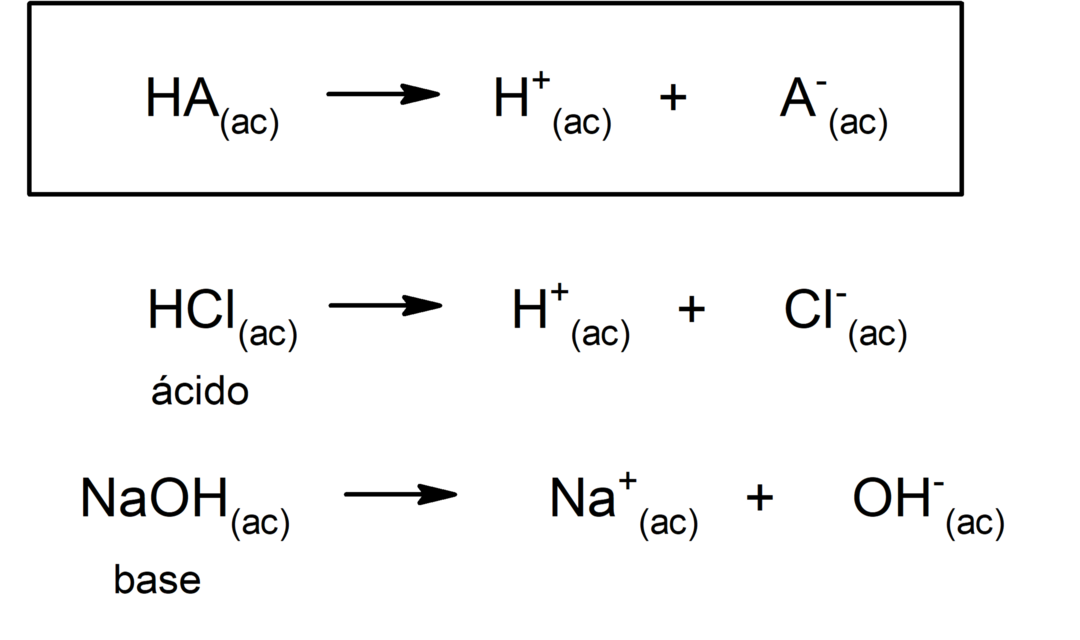
Gotovo četrdeset godina kasnije, oko 1923. godine, Brönsted i Lowry formulirali su drugu teoriju izjavivši da kiseline i baze djeluju kao konjugirani parovi. Prema ovoj teoriji, kiselina je tvar sposobna odreći se protona (u ovom se slučaju ne odnosi na protone atomske jezgre, već na katione H+, budući da je H+ kratica za kation H3ILI+) a baza je ta tvar koja je sposobna prihvatiti te protone.
Ova teorija navodi da je u kiselinsko-baznoj reakciji konjugirana baza kemijska vrsta koja nastaje nakon kiselina daruje proton, a konjugirana kiselina je kemijska vrsta koja nastaje nakon što baza prihvati proton. Ova teorija nije u potpunosti cjelovita, jer postoji nekoliko tvari koje imaju kisela svojstva, a da ih nemaju atoma vodik ionizirajući se u svojoj strukturi.
Ali s druge strane, u ovoj teoriji nije obvezno postojanje tvari u vodenoj otopini. Prikaz kiseline (i njezine konjugirane baze) i baze (i njezine konjugirane kiseline) prema Brönsted-Lowry teoriji je protonacija amonijaka koji se ne mora dogoditi u vodenom mediju:
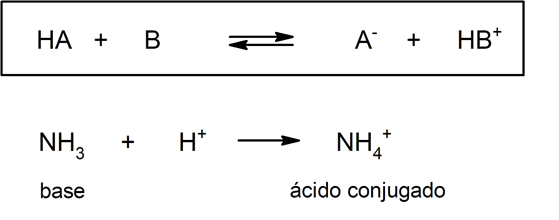
Stoga, kao dodatni dio njegove teorije o kovalentna veza, Lewis je razvio teoriju u kojoj definira kiselinu kao sve to supstancija koji mogu prihvatiti par elektrona, dok je baza bilo koja tvar koja se može odreći navedenog elektroničkog para.
Prema Lewis, koncepti kiseline i baze ne uključuju dobitak ili gubitak OH iona– i H+Umjesto toga, predlaže da je sam H + kiselina (može prihvatiti elektrone), a OH baza (može donirati elektrone). Prikaz kiselinsko-bazne reakcije prema Lewisovoj teoriji je:

Gdje OH- (koji pripada NaOH) donira nepodijeljeni elektronski par H + (koji pripada HCl), kao rezultat koordinatna ili dativna veza (kovalentna veza u kojoj zajedničkom paru elektrona doprinosi samo jedan od atoma koji su uključeni u vezu) da tvore molekulu vode.


