50 Primjeri aldehida i ketona
Primjeri / / November 06, 2023
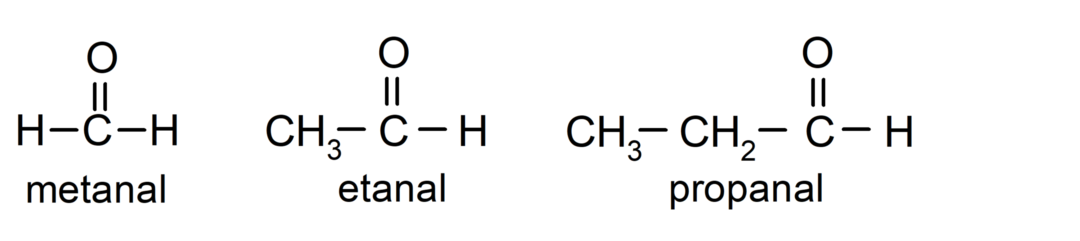
The aldehidi su organski spojevi koji u svojoj strukturi imaju karbonilnu funkcionalnu skupinu (= C = O) koja je povezana s ugljikovim lancem i atomom vodika. Na primjer: metanal (koji se naziva i formaldehid), etanal (koji se naziva i acetaldehid) i propanal (koji se naziva i propaldehid).
The ketoni Oni su organski spojevi koji u svojoj strukturi imaju karbonilnu skupinu povezanu s dva atoma ugljika. Na primjer: propanon (također nazvan aceton), butanon i 2-pentanon.
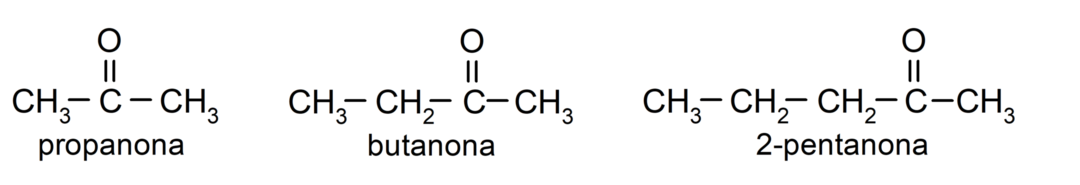
Razlike između aldehida i ketona
Glavne razlike između aldehida i ketona su:
- Aldehidi u svojoj strukturi imaju karbonilnu funkcionalnu skupinu koja se nalazi na jednom terminalnom kraju, dok ketoni imaju karbonilnu skupinu smještenu na svojim neterminalnim pozicijama struktura.
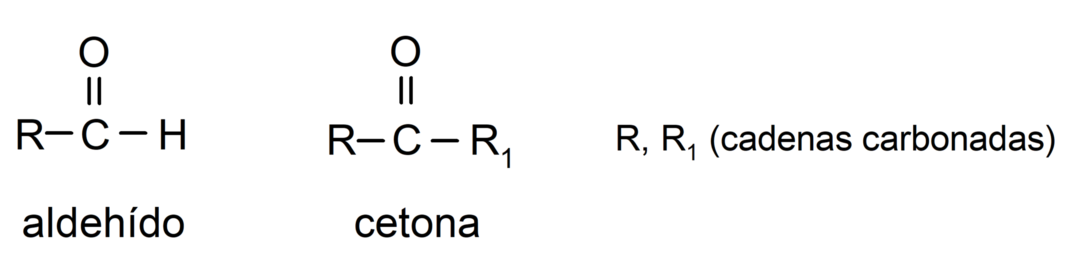
- Aldehidi se oksidiraju reakcijom s Tollensovim reagensom, stvarajući metalno srebro. Oni također oksidiraju protiv Benedictovog reagensa, stvarajući bakrov oksid. Ketoni se ne oksidiraju niti jednim reagensom.
- Aldehidi se reduciraju u primarne alkohole, dok se ketoni reduciraju u sekundarne alkohole.
Fizička svojstva
Fizikalna svojstva aldehida
Fizikalna svojstva aldehida vrlo su raznolika jer ovise o građi ugljikovog lanca koji je vezan za karbonilnu skupinu.
Neki su:
- Aldehidi koji su najtopljiviji u vodi su oni manje veličine, kao što su metanal i etanal.
- Hlapljivi aldehidi imaju oštar, pa čak i iritantan miris.
- Karbonilna skupina daje im polaritet.
- Obično imaju više točke vrelišta od kemijskih spojeva slične veličine molekula.
Fizikalna svojstva ketona
Fizička svojstva ketona ovise o tome kako je formiran ugljikov lanac koji je povezan s karbonilnom skupinom.
- Mnogi ketoni imaju ugodan miris.
- Njegova topljivost u vodi ovisi o veličini ugljikovog lanca vezanog za karbonilnu skupinu. Što je ugljikov lanac manji, to će keton biti topljiviji u vodi.
- Karbonilna skupina daje im izraženu polarnost.
- Imaju prilično visoka vrelišta u usporedbi s kemijskim spojevima usporedive veličine molekula.
Kemijska svojstva
Kemijska svojstva aldehida
Među kemijskim svojstvima aldehida možemo pronaći:
Oni se oksidiraju u odgovarajuću karboksilnu kiselinu, to jest, nastala kiselina će imati isti broj ugljika u ugljikovom lancu kao i aldehid koja je dovela do toga. Na primjer:
- Oksidacija Tollensovim reagensom (amonijačni kompleks srebra u bazičnoj otopini, [Ag (NH3)2]+) iz etanala proizvodi etansku kiselinu i metalno srebro.
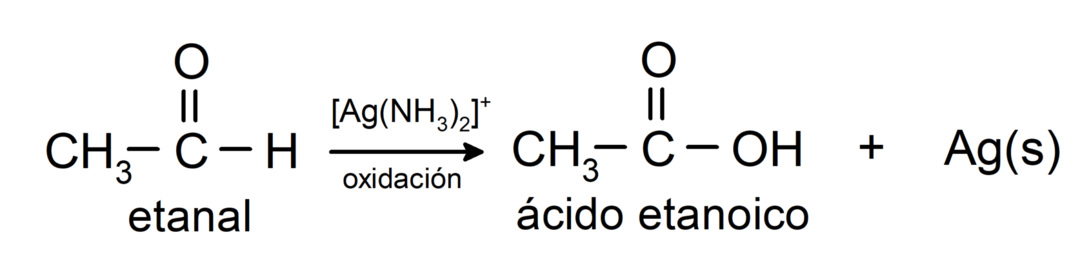
- Oksidacijom etanala Benedictovim reagensom (alkalna otopina bakrenog sulfata) nastaje etanska kiselina i bakrov oksid.
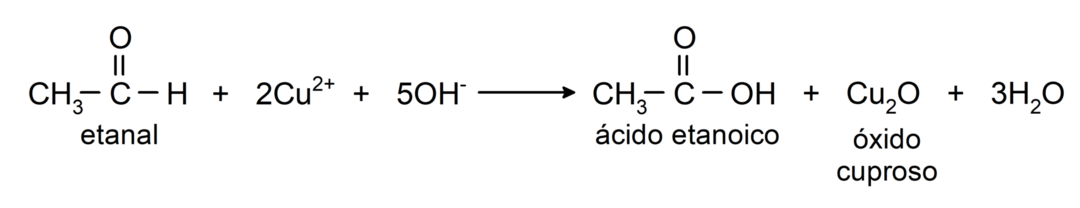
Podliježu reakcijama nukleofilne adicije, odnosno dodavanje nukleofila na karbonilnu skupinu. Na primjer:
- Adicija cijanovodične kiseline u cijanohidrine ili cijanohidrine.
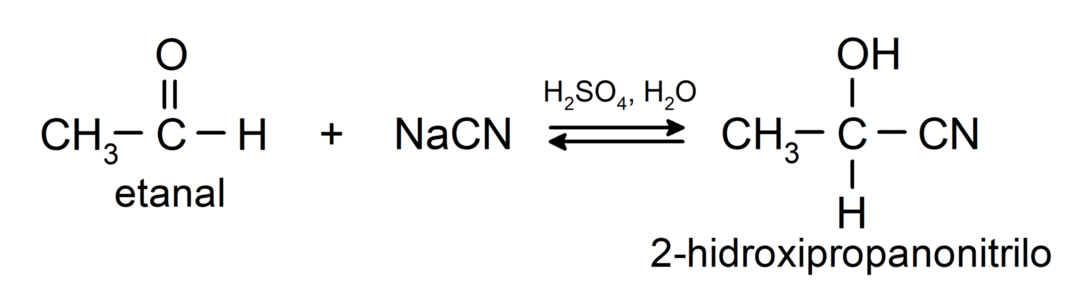
- U prisutnosti bezvodnih kiselina, alkoholi se dodaju karbonilnoj skupini aldehida kako bi nastali acetali i poluacetali.
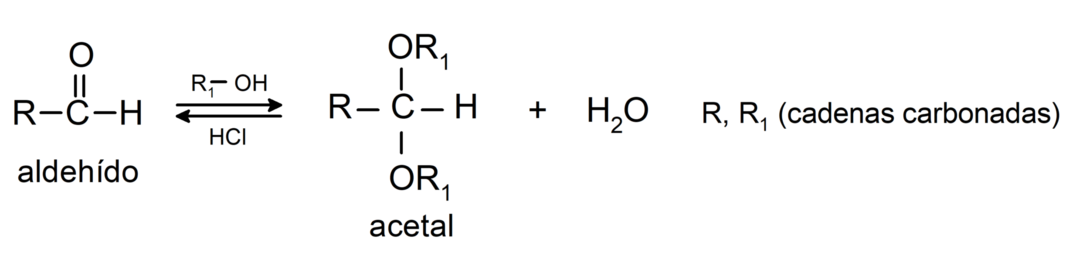
Podliježu reakcijama aldolne kondenzacije. U tim reakcijama dolazi do spajanja dvaju aldehida u prisutnosti natrijevog hidroksida (NaOH) i kemijski spoj koji nastaje naziva se aldol. Na primjer:
- Reakcija kondenzacije etanala u prisutnosti razrijeđenog NaOH.
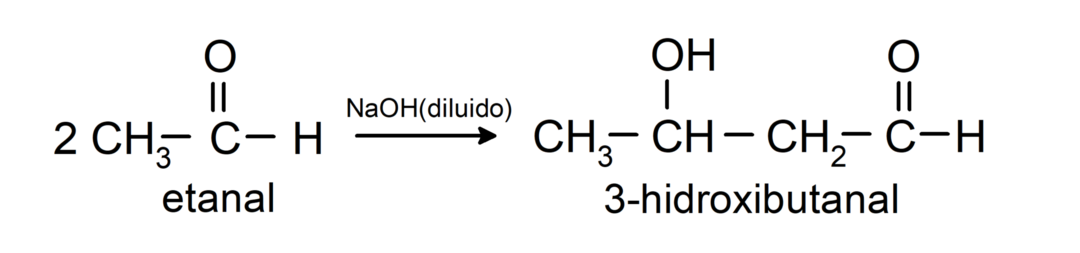
Smanjuju se na primarne alkohole. Aldehidi se mogu reducirati u primarne alkohole katalitičkom hidrogenacijom ili redukcijom s natrijevim borhidridom (NaBH).4) i litij aluminij hidrid (LiAlH4).
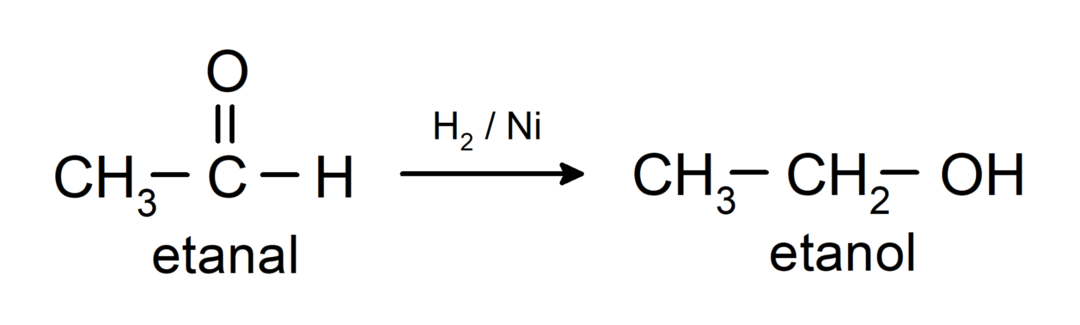
Kemijska svojstva ketona
Među kemijskim svojstvima ketona možemo pronaći:
Podliježu reakcijama nukleofilne adicije. Na primjer:
- Adicija cijanovodične kiseline u cijanohidrine ili cijanohidrine.
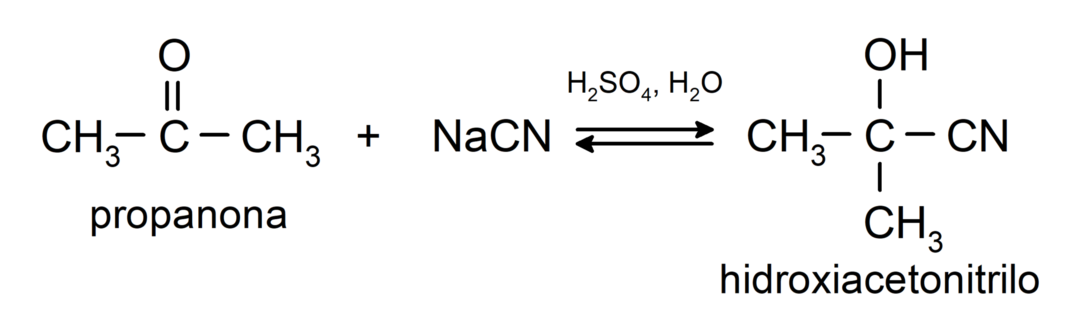
Dodaju alkohole (u prisutnosti bezvodnih kiselina) na karbonilnu skupinu ketona da bi se formirali ketali i poluketali. Na primjer:
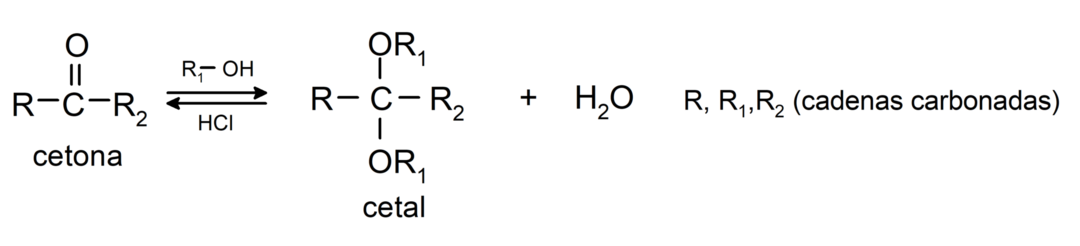
Podliježu reakcijama halogeniranja. Ketoni koji imaju alfa vodik (α) reagiraju zamjenom ovog vodika s halogenima (klor (Cl), brom (Br), jod (I), fluor (F)) u prisutnosti kiselih ili bazičnih katalizatora. Supstitucija se događa gotovo isključivo u ugljiku α, odnosno ugljik koji se vezao na vodik α. Na primjer:
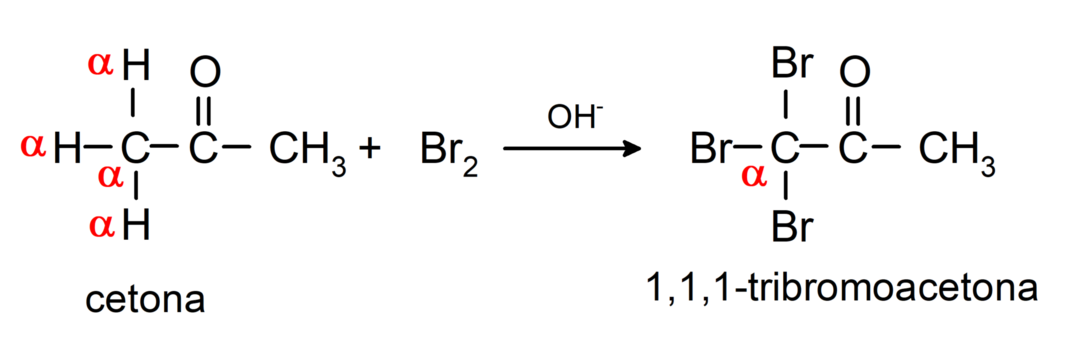
Smanjuju se na sekundarne alkohole katalitičkom hidrogenacijom ili redukcijom s natrijevim borhidridom (NaBH4) i litij aluminij hidrid (LiAlH4). Na primjer:
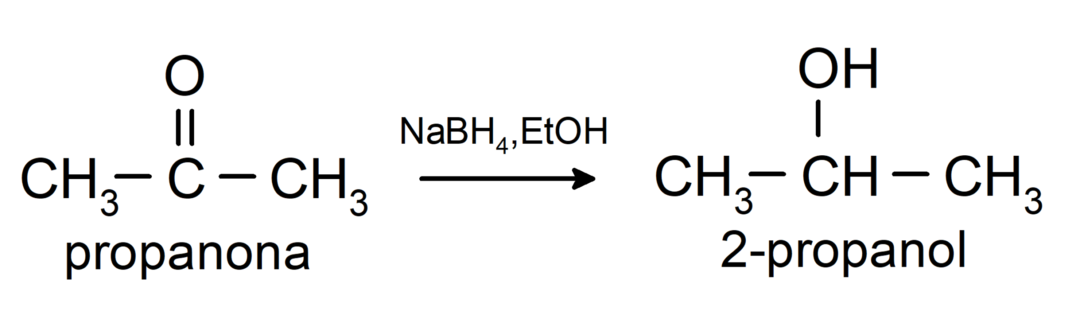
Ketoni se ne oksidiraju Tollensovim i Benedictovim reagensima.
Nomenklatura aldehida
Prema pravilima koje je uspostavila Međunarodna unija za čistu i primijenjenu kemiju (IUPAC), Aldehidi se imenuju pomoću prefiksa koji označavaju broj ugljika u lancu. gazirana. Nije potrebno specificirati položaj karbonilne skupine, budući da je uvijek na položaju jedan, na jednom kraju molekule. Osim toga, nastavak -al piše se na kraju naziva aldehida. Na primjer:
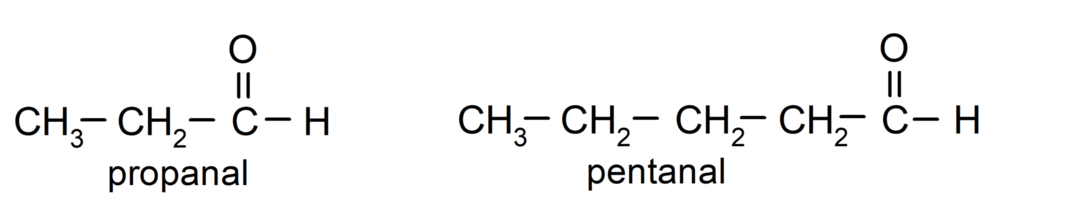
Ako je aldehid građen od više ugljikovih lanaca, odnosno ima grane, kao glavni lanac bira se ugljikov lanac s najvećim brojem ugljikovih atoma. Ostali lanci nazivaju se supstituentskim skupinama, a položaj svakog supstituenta odabire se tako da zauzima najmanji mogući broj u lancu. Osim toga, ugljikovi atomi počinju se brojati počevši od kraja koji ima karbonilnu skupinu. Na primjer:
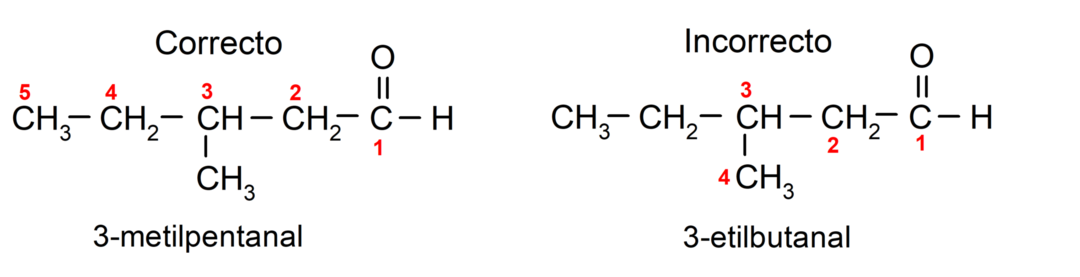
Aldehidi koji imaju dvije karbonilne skupine nazivaju se sufiksom -dial. Na primjer:
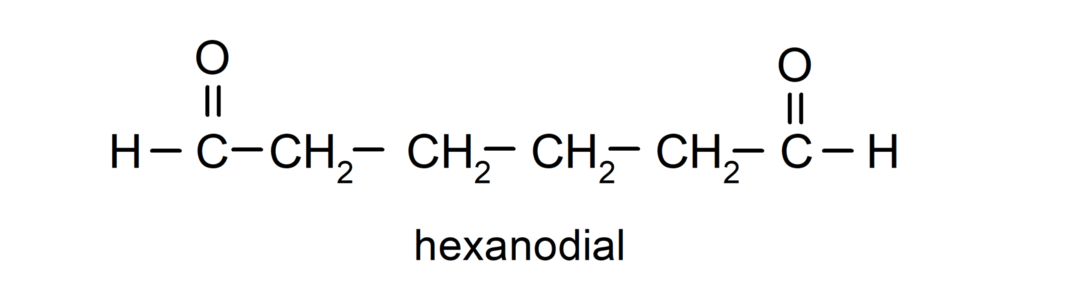
Nomenklatura ketona
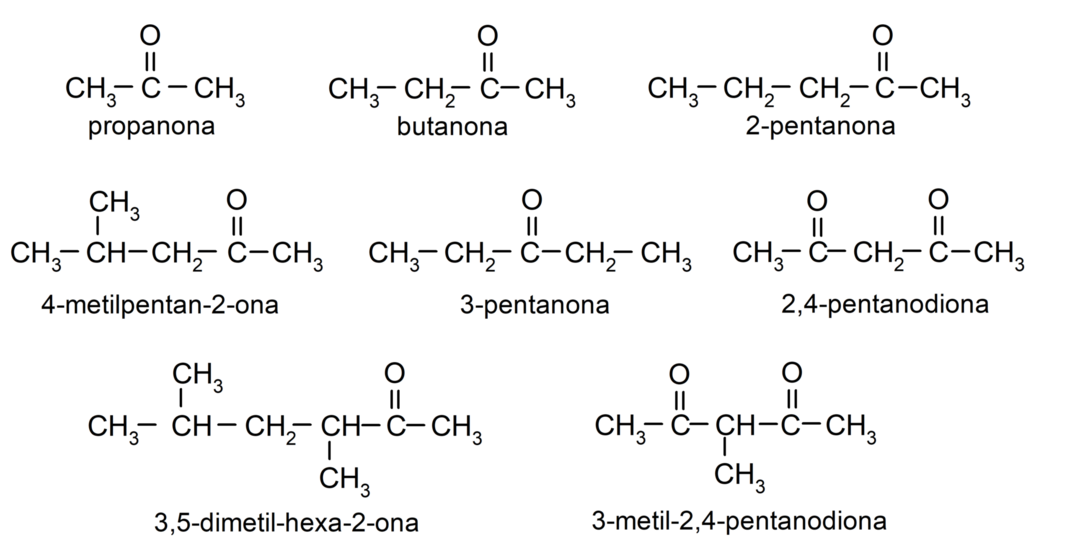
Prema Međunarodnoj uniji za čistu i primijenjenu kemiju (IUPAC), ketoni se imenuju pomoću prefiksa koji označavaju broj ugljika u ugljikovom lancu.
S druge strane, naziv acetona piše se pomoću sufiksa -one, ispred kojeg stoji broj koji označava položaj karbonilne skupine u ugljikovom lancu. Položaj karbonilne skupine treba odabrati na takav način da odgovara najnižem mogućem numeriranju. Na primjer:
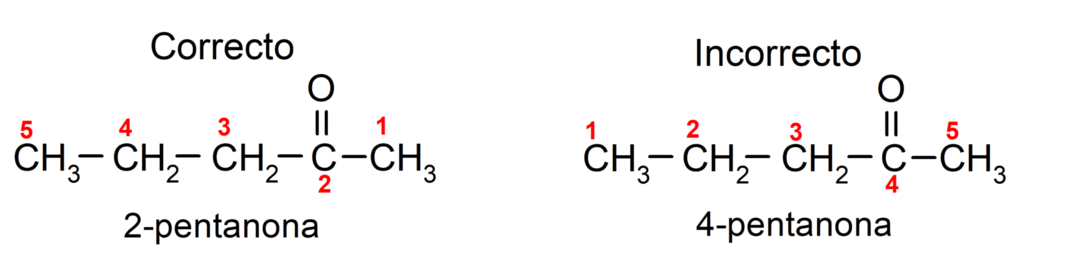
Za ime ketona koji se sastoji od nekoliko ugljikovih lanaca, odnosno s ograncima, biramo kao glavni lanac, ugljikov lanac s najvećim brojem ugljikovih atoma i koji sadrži skupinu karbonil. Ostali lanci nazivaju se supstituentskim skupinama. Na primjer:
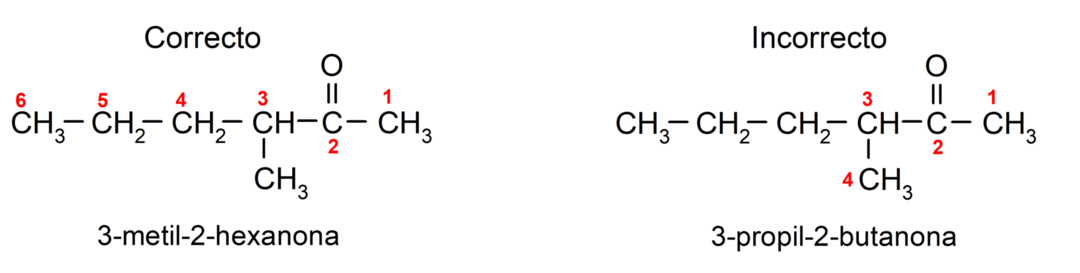
Postoje ketoni koji imaju dvije karbonilne skupine, nazivaju se dioni. Na primjer:
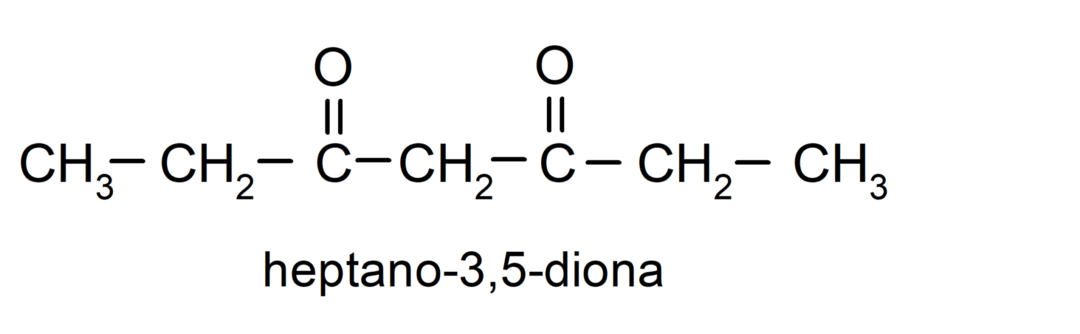
Primjeri aldehida
- metanal (formaldehid)
- etanal (acetaldehid)
- propanal (propaldehid)
- butanal
- pentanal
- heksanal
- 3-bromociklopentankarbaldehid
- cikloheksankarbaldehid
- benzaldehid
- 4,4-dimetilpentanal
- 2-hidroksi-butanal
- 2-hidroksi-2-metil-butanal
- 2,3-dimetilpentanal
- pentanedijalni
- 4-hidroksi-3-metoksibenzaldehid
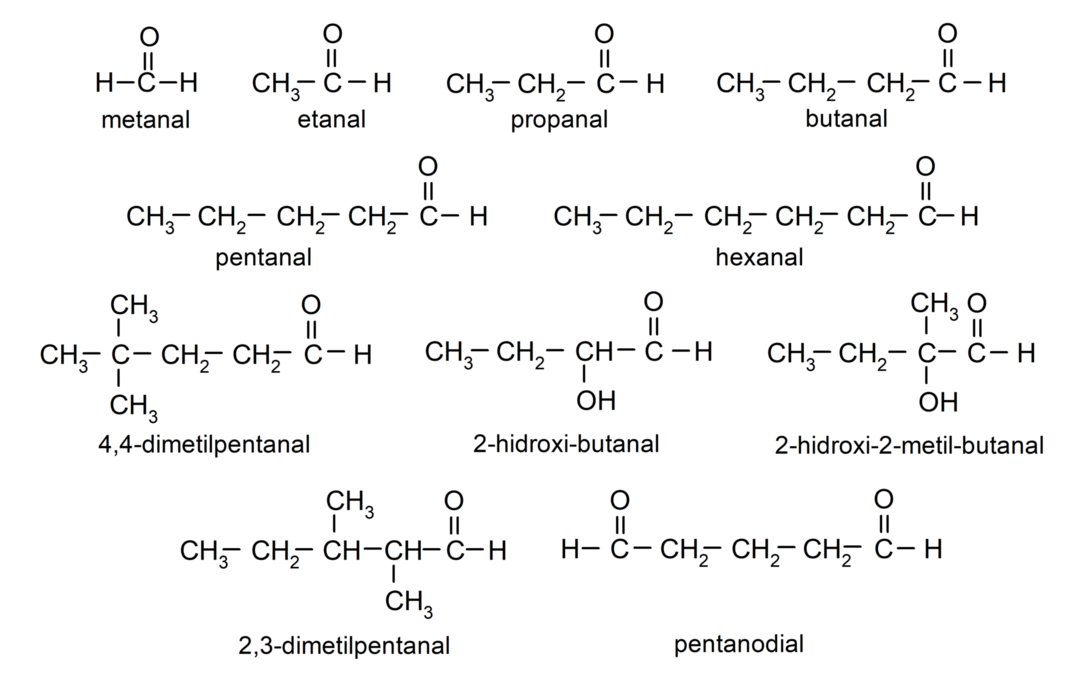
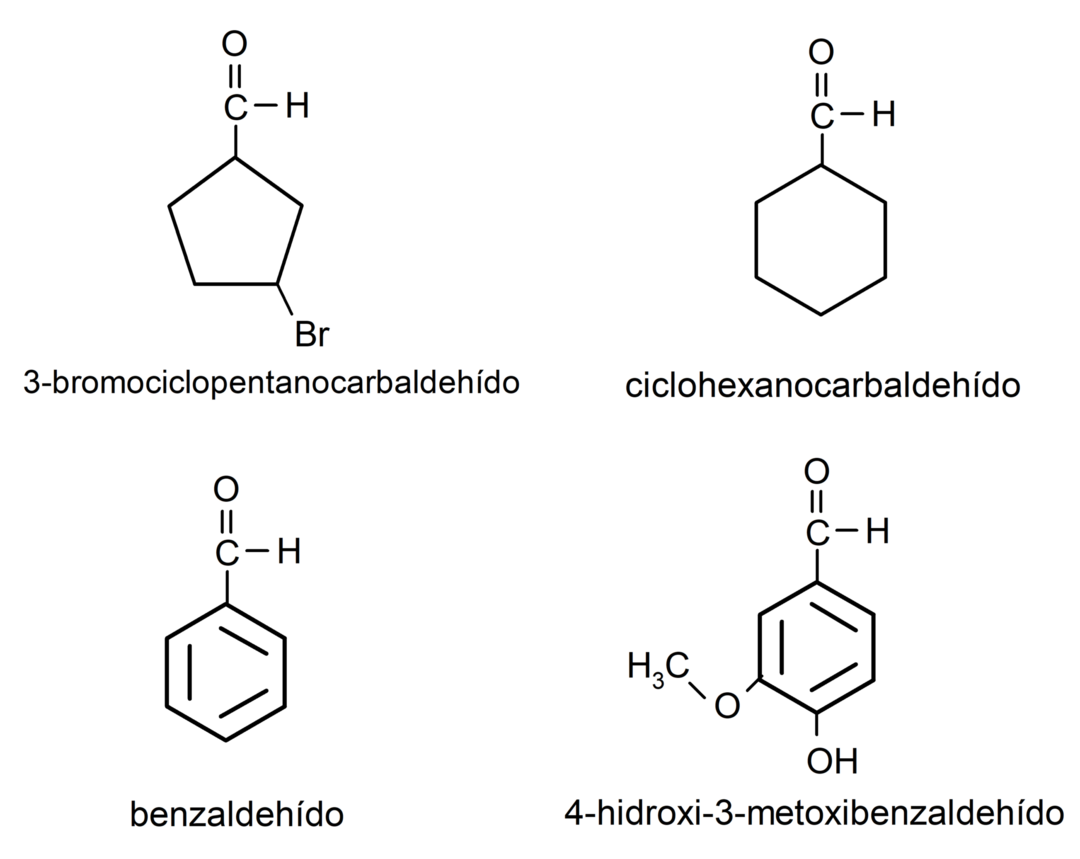
Primjeri ketona
- propanon (aceton)
- butanon
- 2-pentanon
- 4-metilpentan-2-on
- 3-metilcikloheksanon
- cikloheksilmetilketon
- 3,4-dimetil-heksan-2-on
- etil fenil keton
- 2,4-pentandion
- cikloheksanon
- 3-pentanon
- 3-metil-2,4-pentandion
- 1-fenilpropanon
- ciklopentanon
- difenil keton
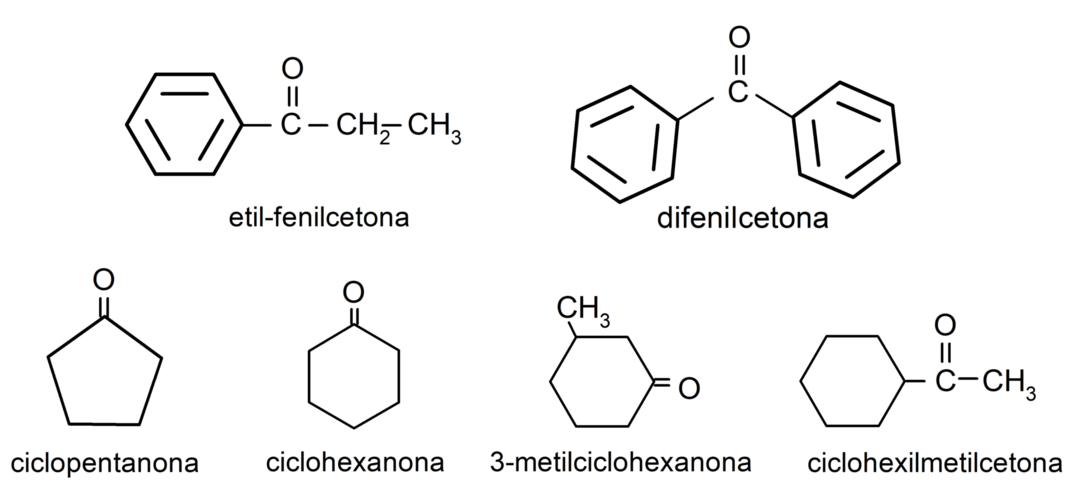
Upotreba aldehida u svakodnevnom životu
Neke upotrebe aldehida su:
- Koriste se za proizvodnju otapala, boja, parfema, smola i esencija.
- Koriste se kao konzervansi u kozmetičkim proizvodima, biološkim uzorcima i leševima. Za te namjene najviše se koristi formaldehid.
- Koriste se za proizvodnju plastike koja omogućuje zamjenu metalnih dijelova u automobilskoj industriji.
- Koriste se kao arome za neku hranu.
- Koriste se kao dezinfekcijska sredstva.
- Korišteni su za izradu nekih eksploziva, poput pentaeritritol tetranitrata (TNPE).
Upotreba ketona u svakodnevnom životu
Neke upotrebe ketona su:
- Koriste se u proizvodnji otapala. Aceton se osobito široko koristi za uklanjanje boja i lakova.
- Koriste se u proizvodnji nekih guma i maziva.
- Koriste se za proizvodnju boja, lakova i lakova.
- Koriste se za proizvodnju lijekova i kozmetike.
Toksičnost aldehida i ketona
- Aldehidi. Kontakt s aldehidima izaziva iritaciju kože, očiju i dišnih puteva. Osim toga, izloženost aldehidima povezana je s bolestima kao što su rak, kontaktni dermatitis te bolesti jetre i neurodegenerativne bolesti. Formaldehid, na primjer, WHO (Svjetska zdravstvena organizacija) smatra kancerogenim spojem.
- ketoni. Ponavljano izlaganje ketonima može uzrokovati oštećenje središnjeg živčanog sustava. To može dovesti do gubitka pamćenja, slabosti, bolova u mišićima i grčeva. Osim toga, ako koža dođe u dodir s ketonima, dolazi do suhoće i pucanja. S druge strane, ako se ketoni udišu, dolazi do iritacije dišnih puteva i kašlja.
Reference
- Llorens Molina, JA. (2018). “Aldehidi i ketoni: nekoliko primjera.” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015.) “Tollensov reagens: od identifikacije aldehida do njihove upotrebe u nanotehnologiji. Povijesni aspekti i didaktičke primjene.”Vol. 111 Br. 3. Kraljevsko španjolsko kemijsko društvo.
- William Bauer, Jr. (2000.) «Metakrilna kiselina i njeni derivati» u Ullmannovoj Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441.
- “Oni otkrivaju novi mehanizam toksičnosti u skupini kancerogenih spojeva koji potječu iz prehrane i okoliša” (2022.) U: www.conicet.gov.ar Dostupno u: https://www.conicet.gov.ar/ Pristupljeno: 20. lipnja 2023.
Slijedite s:
- Alkoholi
- Šećeri
- alkani