30 primjera binarne prodaje
Primjeri / / November 09, 2023
The binarne soli (neutralne soli) nastaju spajanjem metala i nemetala. Jesu li kemijski spojevi sastavljen od samo dva kemijski elementi. Na primjer: natrijev klorid (NaCl) i kalijev bromid (KBr).
- Vidi također: Metali i nemetali
Primjeri binarnih soli
- Natrijev klorid (NaCl)
- Željezov(II) klorid (FeCl2)
- Željezov(III) klorid (FeCl3)
- Kobalt(II) sulfid (CoS)
- Kobalt(III) sulfid (Co2Da3)
- Olovni (II) sulfid (PbS)
- Olovni (IV) sulfid (PbS2)
- Kalcijev klorid (CaCl2)
- Natrijev fluorid (NaF)
- Litijev klorid (LiCl)
- Stroncijev klorid (SrCl2)
- Barijev klorid (BaCl2)
- Aluminijev klorid (AlCl3)
- Magnezijev sulfid (MgS)
- Rubidijev klorid (RbCl)
- Kalcijev bromid (CaBr2)
- Kalijev sulfid (K2S)
- Magnezijev bromid (MgBr2)
- Cinkov sulfid (Zn2S)
- Litijev bromid (LiBr)
- Nikal klorid (NiCl2)
- Uran(III) klorid (UCl3)
- Srebrni bromid (AgBr)
- Srebrni jodid (AgI)
- Kalijev bromid (KBr)
Nomenklatura binarnih soli
Prema Tradicionalnoj nomenklaturi, binarne soli se imenuju pisanjem naziva nemetalnog elementa sa završetkom -ide. S druge strane, naziv metalnog elementa piše se prema njegovom oksidacijskom stupnju:
- Za najniže oksidacijsko stanje piše se sa završetkom -oso. Na primjer: željezni klorid (FeCl2), gdje željezo ima oksidacijski stupanj 2+.
- Za najviše oksidacijsko stanje piše se sa završetkom -ico. Na primjer: željezov klorid (FeCl3), gdje željezo ima oksidacijski stupanj 3+.
Prema Sustavnoj nomenklaturi binarne soli se imenuju ispisivanjem imena nemetalnog elementa s prefiksom koji označava količinu atomi ovog elementa u spoju. Osim toga, završetak -uro stavlja se u ime nemetalnog elementa. Zatim se stavlja naziv metalnog elementa. Na primjer: magnezijev diklorid (MgCl2) i željezov triklorid (FeCl3).
Prema Stockovoj nomenklaturi, binarne soli se imenuju pisanjem imena nemetalnog elementa sa završetkom -ide. Zatim se stavlja naziv metalnog elementa iza kojeg stoji njegovo oksidacijsko stanje napisano rimskim brojevima iu zagradi. Na primjer: željezov(II) klorid (FeCl2) i kobalt(III) sulfid (Co2Da3).
Primjena binarnih soli
- Koriste se kao rashladna sredstva u prehrambenoj i farmaceutskoj industriji. Na primjer: kalcijev klorid (CaCl2).
- Koriste se za zaštitu metalnih površina od korozije. Na primjer: natrijev fluorid (NaF).
- Koriste se za regulaciju vlage u papirnoj i građevinskoj industriji. Na primjer: kalcijev klorid (CaCl2).
- Koriste se u industriji stakla za uklanjanje nečistoća. Na primjer: silicijev tetraklorid (SiCl4).
- Koriste se kao sastojci za kuhanje. Na primjer: natrijev klorid (NaCl).
Fizikalna svojstva binarnih soli
- Imaju visoka tališta jer se sastoje od ionske veze.
- Oni provode električnu struju kada su otopljeni ili otopljeni.
- Najčešće soli imaju nisku tvrdoću.
- Nisu kompresibilne.
- Većina se može otopiti u vodi.
Kako se dobivaju binarne soli?
Binarne soli mogu se dobiti kroz neke od sljedećih kemijskih reakcija:
Reakcija između metala i nemetala. Na primjer: reakcija između natrija (Na) i diklorida (Cl2) proizvodi natrijev klorid (NaCl).
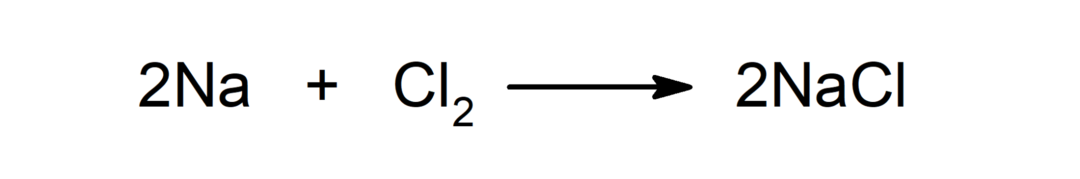
Reakcija između metala i kiseline. Na primjer: Reakcija između kalija (K) i klorovodične kiseline (HCl) proizvodi kalijev klorid (KCl) i dihidrogen (H2).
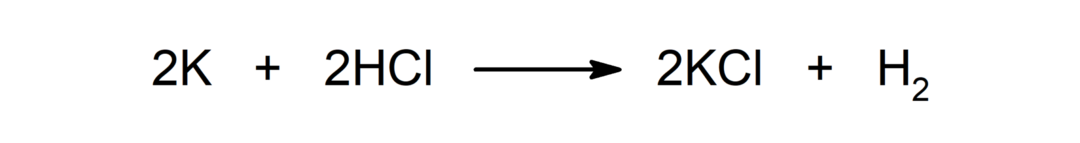
Reakcija između kiseline i baze. Na primjer: Reakcija između klorovodične kiseline (HCl) i natrijevog hidroksida (NaOH) proizvodi natrijev klorid (NaCl) i vodu (H2ILI).
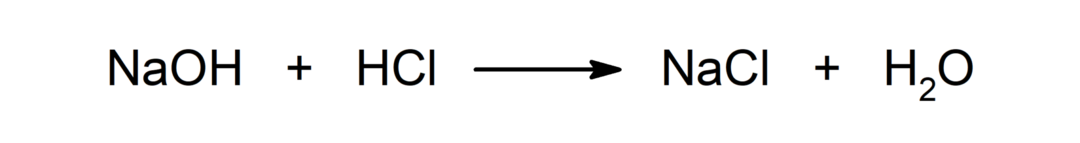
Slijedite s:
- oksisoli
- neutralne soli
- kisele soli
Reference
- Cerón Villalba, A., Novoa Ramírez, C. S. i Alpizar Juárez, E. (2020). Nomenklatura video 1: binarne soli i kemijske reakcije.
- Acurio Arias, M. V. i Delgado Méndez, M. I. (2022). Vodič za učenje temeljen na igrama za "binarne spojeve" u srednjoškolskoj kemiji na obrazovnoj jedinici "Herlinda Toral" (Diplomski rad, Nacionalno sveučilište za odgoj i obrazovanje).
- Cabrera, M. J. H. (2005). Proučavanje od prvih principa elektroničkih i strukturnih svojstava binarnih i ternarnih spojeva (Doktorska disertacija, Sveučilište La Laguna).



