Što je Elektroliza
Kemija / / July 04, 2021
U kemiji, Elektroliza je fenomen u kojem električna struja prolazi kroz vodenu otopinu ionskog spoja, i započinje usmjeriti ione (nabijene čestice) spoja a dvije elektrode, pozitivno (Anoda, privlači negativno nabijene anione) i negativne (Katoda, privlači pozitivno nabijene katione). Ovom pojavom upravlja zakon elektrostatike, koji ukazuje da se suprotni naboji međusobno privlače.
Elektroliti
1883. god. Michael Faraday otkrio da vodene otopine određenih tvari provode električnu struju, dok otopine drugih tvari ne.
Da bi ispitao provodi li vodena otopina električnu struju ili ne, Faraday je dizajnirao jednostavni aparat koji se sastoji od Istosmjerni krug od 110 volti, svjetiljka, Y dvije povezane metalne ili grafitne elektrode do trenutnog izvora.
Ako su elektrode uronjene u vodu, količina struje je toliko mala da žarulja ne svijetli; isto vrijedi ako su umočeni u otopinu šećera.
Naprotiv, ako su uronjeni u otopinu Natrijev klorid NaCl ili iz Klorovodična kiselina HCl, svjetiljka svijetli sjajno, što dokazuje da
otapanje je izvrstan provodnik. S druge strane, upotreba octene kiseline CH3Koncentrirana COOH, otopina loše vodi struju, ali kada se kiselina razrijedi vodom H2Ili se njegova električna vodljivost povećava.Tijekom prolaska struje kroz različite otopine, na elektrodama se dobivaju različiti proizvodi.
Tijekom studija Elektrolize, Faraday je izveo sljedeće zakone:
1. zakon: Količina tvari koja ima svoju kemijsku transformaciju u elektrodi proporcionalna je količini električne energije koja prolazi kroz otopinu.
2. zakon: Ako se ista količina električne energije propušta kroz različite otopine, težine tvari razgrađeni ili taloženi na različitim elektrodama proporcionalni su ekvivalentnim težinama navedenih tvari.
Da navedemo primjer:
Pretpostavit će se da imate pet različitih elektrolitičkih ćelija. Prvi sa Klorovodična kiselina HCl, drugi sa Bakar-sulfat CuSO4, treći sa Antimoniozni klorid SbCl3, četvrti sa Stannov klorid SnCl2 a peti sa Stannikov klorid SnCl4.
Ista struja prolazi kroz niz elektrolitičkih ćelija, sve dok se 1008 grama vodika (a Ekvivalentna težina vodika) otopine klorovodične kiseline, težine (u gramima) ostalih proizvoda koji su pušteni u isto vrijeme Oni su:
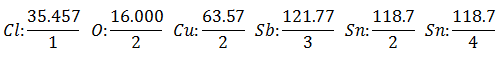
The Ekvivalentna težina ima vrijednost Atomska težina elementa podijeljena s Valencijom elementa.
Trebate osloboditi ekvivalentnu težinu bilo kojeg predmeta 96500 Kulomi. Ova količina električne energije se naziva 1 Faraday.
Faradayeva jedinica
Amper je definiran kao jednolična struja koja taloži 0,001118 grama srebra (Ag) iz otopine srebrnog nitrata (AgNO3) u sekundi. Budući da je atomska težina srebra 107,88 g / mol, omjer 107,88 / 0,001118 daje broj amperskih sekundi ili kulona potrebna struja položiti kemijski ekvivalent srebra. Ta je količina 96494 kuloma (vrijednost 96500 prilično je približna za jednostavnije izračune) i naziva se 1 Faraday of Electricity.
Elektrode
Nazvao je Faraday Anoda na pozitivnoj elektrodi, a katoda na negativnoj elektrodi. Također je stvorio izraze Anion i Kation, koji se primjenjuju na tvari koje se pojavljuju na anodi i na katodi tijekom Elektrolize.
Trenutno je druga definicija elektroda:
Anoda: Elektroda u kojoj dolazi do gubitka elektrona ili oksidacije.
Katoda: Elektroda u kojoj dolazi do pojačanja ili smanjenja elektrona.
Elektroliti i ne-elektroliti
Provođenje električne struje kroz otopine nije zadovoljavajuće objašnjeno sve do 1887. godine, kada je Svante Arrhenius objavio svoju teoriju. Prije uvažavanja i razumijevanja Arreniusove teorije, prvo smo iznijeli neke činjenice koje su bile poznate znanosti kad ju je Arrhenius formulirao:
The Otopine koje nisu elektroliti imaju svojstva koja se mogu izračunati primjenom Raoultovog zakona. Pritisci pare i promatrane točke vrenja i smrzavanja ovih otopina praktički su jednake izračunatim vrijednostima.
The Raoultov zakon objašnjava da tlak pare svake otopljene tvari u otopini ovisi o vlastitom molskom udjelu u njoj, pomnoženom s tlakom pare u čistom stanju.

Raoultov zakon propada kada se primjenjuje na otopine elektrolita u vodi. Varijacije tlaka pare i vrelišta i ledišta uvijek su veće od onih predviđenih gore spomenutim zakonom, a osim toga, povećavaju se pri razrjeđivanju.
Takva odstupanja predstavljaju vrijednost i, koja je omjer varijacije uočene u točki smrzavanja između varijacije izračunate u točki smrzavanja:

Vrijednost i mjera je odstupanja od Raoultovog zakona, koja je jednaka 1 kad odstupanja nema.
Električna vodljivost elektrolita
Arrhenius je istraživao vodljivost vodenih otopina elektrolita kako bi otkrio kako varira vodljivost s koncentracijom elektrolita.
Izmjerena je molarna vodljivost (što je vodljivost koja odgovara jednom molu otopljenog elektrolita; to jest, specifična vodljivost odnosila se na jedan mol i utvrdila je da se povećavala razrjeđivanjem.
Arrhenius je svoje rezultate usporedio s mjerenjima odstupanja od Raoultovog zakona i otkrio usku vezu između njih i molarne vodljivosti. U njegovoj teoriji objašnjava se ponašanje elektrolita:
“Molekuli elektrolita razdvajaju se na električki nabijene čestice zvane ioni. Otapanje je nepotpuno i postoji ravnoteža između molekula i njihovih iona. Ioni vode struju dok se kreću unutar otopine ”.
Odstupanja od Raoultovog zakona posljedica su povećanja broja čestica koje proizlaze iz djelomične disocijacije molekula.
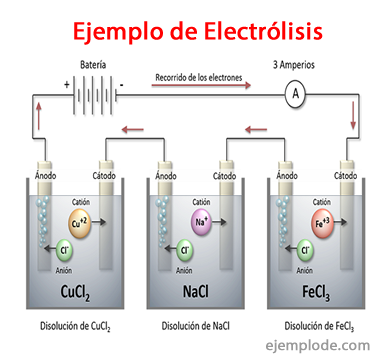
Primjeri elektrolize
Neka rješenja koja se ponašaju poput elektrolita, odnosno imaju sposobnost elektrolize su:
Natrijev klorid NaCl
Klorovodična kiselina HCl
Natrijev sulfat Na2SW4
Sumporna kiselina H2SW4
Natrijev hidroksid NaOH
Amonijev hidroksid NH4Oh
Natrijev karbonat Na2CO3
Natrijev bikarbonat NaHCO3
Dušična kiselina HNO3
Srebrni nitrat AgNO3
Cink sulfat ZnSO4



