Primjer kemijske energije
Kemija / / July 04, 2021
The Kemijska energija je ona koja dolazi iz kemijskih reakcija. Interakcija između kemijskih vrsta generira pucanje i / ili stvaranje veza, što podrazumijeva oslobađanje odnosno apsorpciju energije. Kemijska energija naziva se oslobođena energija, koja se na primjer može koristiti kao toplinska i električna energija.
Energija u kemijskim reakcijama
Kemijska energija može se dobiti u svom maksimalnom izražaju iz dva glavna izvora: izgaranje i elektrolitske otopine. S druge strane, na razini ljudskog tijela moguće je dobivati energiju kemijskim raspadanjem hrane.
Energija izgaranja
Na primjer, kada gorivo Metan CH4, najjednostavniji ugljikovodik, počinje izgarati u prisutnosti oksidansa kisika, on će se raspasti, stvarajući ugljikov dioksid CO proizvode.2 i Voda H2ILI. Uz to, prekidanjem veza vodikovih atoma s atomima ugljika oslobodit će se energija u obliku topline.
CH4 (g) + 202 (g) → CO2 (g) + 2H2 O (l) ∆H = -212,8 Kcal / mol
Jednadžba izgaranja metana. Toplinu ove reakcije predstavlja ΔH. Negativni znak ukazuje na oslobađanje energije. Reakcija je egzotermna.
 Izgaranje plina metana. Reakcija se očituje plamenom.
Izgaranje plina metana. Reakcija se očituje plamenom.
Primjeri toplina izgaranja organskih spojeva na 25 ° C.
Spoj |
Formula |
ΔH (Kcal / mol) |
Metan (g) |
CH4 |
-212.80 |
Etan (g) |
C2H6 |
-372.82 |
Propan (g) |
C3H8 |
-530.60 |
n-butan (g) |
C4H10 |
-687.98 |
n-pentan (g) |
C5H12 |
-845.16 |
Etilen (g) |
C2H4 |
-337.23 |
Acetilen (g) |
C2H2 |
-310.62 |
Benzen (g) |
C6H6 |
-787.20 |
Benzen (l) |
C6H6 |
-780.98 |
Toluen (l) |
C7H8 |
-934.50 |
Naftalen (i) |
C10H8 |
-1,228.18 |
Saharoza (e) |
C12H22ILI11 |
-1,348.90 |
Metanol (l) |
CH3Oh |
-173.67 |
Etanol (l) |
C2H5Oh |
-326.70 |
Octena kiselina (l) |
CH3COOH |
-208.34 |
Benzojeva kiselina |
C6H5COOH |
-771.20 |
Da bi gorivo moglo pružiti svu toplinu izgaranja za koju je sposobno, mora biti u plinovitom stanju. Kao što se može vidjeti u tablici, tekući benzen doprinosi toplini izgaranja koja je za 6,22 Kcal / mol manja od one koja se oslobađa plinovitim benzenom. To znači da se za promjenu tekućine u plin mora uložiti 6,22 Kcal / mol.
Kliknite za više informacija na Goriva.
Elektrolitska rješenja Energija
Elektrolitički vodič je medij u kojem je uključena jedna ili više ionskih vrsta, što je raspršeni sa svojim električnim nabojem, dopuštajući električnoj struji da prolazi kroz njegov Ustav. Elektrolitička rješenja su elektrolitski vodiči.
Elektrolitički vodiči uključuju, osim otopina elektrolita, Rastopljene soli, a također i neke čvrste soli, kao što su natrijev klorid NaCl i srebrni nitrat AgNO3.
Prijenos elektrona događa se ionskom migracijom, pozitivnom i negativnom, prema elektrodama. Ova migracija uključuje ne samo prijenos električne energije, već i transport materije iz jednog dijela vodiča u drugi.
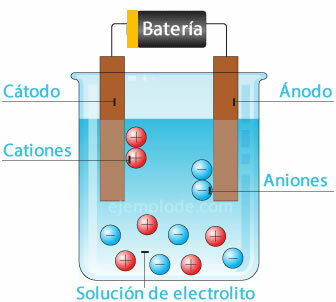 Elektrokemijska ćelija
Elektrokemijska ćelija
Povezivanje potencijalnog izvora s metalnim elektrodama (katoda i anoda) i njihovo potapanje u a Vodena otopina, elektroni će putovati kroz anodu, da pobjegnu iz otopine do pozitivnog pola fontana. To je slučaj, na primjer, s kloridnim ionom, koji se oslobađa iz svog elektrona, a već s neutralnim nabojem pridružuje se drugom atomu klora, stvarajući dvoatomsku molekulu. Iz otopine će izlaziti plinoviti klor.
2Cl- = 2Cl + 2e-
Elektroni koji napuštaju negativni pol izvora bit će smješteni u potopljenoj katodi. Vrste prisutne u vodenoj otopini (ioni) uzet će elektrone s katode. Na primjer, uzeli su ioni vodika koji čine vodu, budući da su bili u pozitivnom naboju elektron koji treba neutralizirati i spojiti s drugim atomom vodika da bi se stvorila molekula dvoatomni. Izlazit će kao plinoviti vodik iz otopine.
2H+ + 2e- = 2H
2H = H2 (g)
Ova izmjena elektrona može podržati rad automobilskih baterija, koje se sastoje od olovnih Pb elektroda uronjenih u otopinu sumporne kiseline H2SW4.
Ista se energija dobiva u svim vrstama baterija kojima se rukuje na domaćoj razini: 9V, AA, AAA, D, da nabrojimo nekoliko primjera.
Energija hrane
Ljudska bića asimiliraju energiju koja se oslobađa raspadajući hranu koju jedemo u tijelu. Ta je energija ono što naše tijelo koristi za nesvjesne funkcije (probavu, otkucaje srca, stanične funkcije) i one koje provodimo.
Sve dok nemate intenzivnu tjelesnu aktivnost i vaš je metabolizam spor, poželjno je redovito unositi kalorije, jer hrana bogata Složeni lipidi i ugljikohidrati, koji imaju vrlo velike strukture, teže se razgrađuju, što rezultira preokretom Energija. U tom bi slučaju učinak bio trenutno suprotan.
Poželjno je konzumirati voće kada morate raditi noću, jer voće sadrži fruktozu, jednostavan ugljikohidrat koji se lako razgrađuje i koji će nam imati na raspolaganju energiju nakon vašeg potrošnja.
Kemijska energija i njezine transformacije
Termoelektrična postrojenja
Teška goriva koriste se u termoelektranama kako bi imala visoku i dugotrajnu kalorijsku vrijednost. Općenito je to loživo ulje (loživo ulje). Izgaranje, koje je kemijska faza postupka, služit će kao sredstvo za grijanje kotla, koje će stvoriti zasićenu paru. Ova para će izlaziti pod pritiskom kroz mrežu za distribuciju pare i započet će pomicanje generacijskih turbina. Ovi će uređaji proizvoditi električnu energiju za opskrbu odgovarajuće populacije.
Kemijska energija → Mehanička energija → Električna energija
Automobilska operacija
Automobili ovise o izvoru energije, a to je akumulator. U bateriji je već poznato da dolazi do elektrolitske vodljivosti koja napaja sustav paljenja, pribor za pločice i pomoćne utičnice. Zahvaljujući ovoj dostupnoj električnoj energiji, automobil će se moći kretati kako bi odvezao vozača na željeno mjesto.
Kemijska energija → Električna energija → Mehanička energija


