20 Példák savakra
Vegyes Cikkek / / July 04, 2021
A savak fontos csoportját alkotják kémiai vegyületek, nagyon széles. A savak általában olyan vegyületek, amelyek adományozhatnak egy vagy több adományt kationok hidrogén (H+) egy másik vegyületté, más néven bázis. Bár a valóságban a savakat több elmélet alapján határozzák meg:
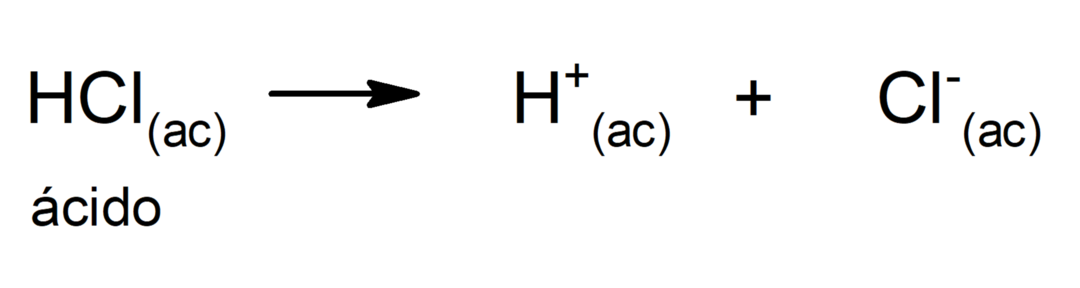 Ennek az elméletnek az a korlátja, hogy a savakat csak vizes oldatban határozzuk meg.
Ennek az elméletnek az a korlátja, hogy a savakat csak vizes oldatban határozzuk meg. 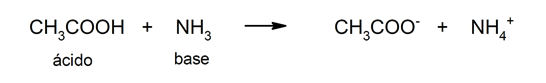

A kiadás tulajdona hidrogén-kationok az, ami a savakat oldatok előállítására készteti pH kevesebb, mint 7. Savak, amelyek egynél több protont szabadíthatnak fel (ezt a nevet használva a H+) poliprotikusnak vagy többfunkciósnak nevezzük.
Savas tulajdonságok
Ami az őket illeti tulajdonságait, savak bemutathatók folyadékok vagy mint gázok, ritkábban szilárd. A sav ízét, amelyet felismerhetünk és amely jellemzi ezeket a vegyületeket, megtaláljuk például a citrusfélék, amelyekben gazdag citromsav vagy ecet, amely savoldat ecetsav. Ezek szerves savak.
létezik szerves és szervetlen savak; a legerősebbek általában a szervetlenek. Számos szerves sav fontos biológiai szerepet tölt be. A szervetlenek között van egy, a sósav, amely nagyon fontos szerepet játszik az emésztési folyamatban. A
nukleinsavak Alapvető fontosságúak az élet számára is, mivel ezek az alapja a genetikai anyagnak sejtek és tartalmazzák a szintézis kulcsát fehérje.A protonok elvesztésére való hajlam határozza meg a sav erősségét.
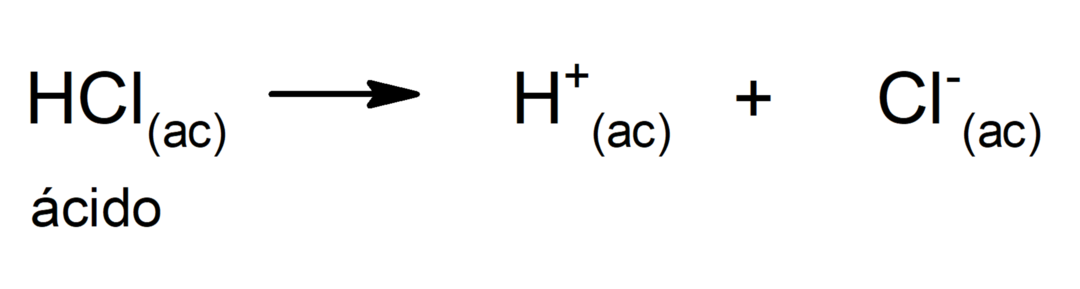
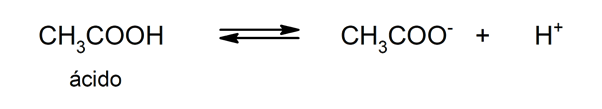
Savak felhasználása
A savaknak van sok felhasználás, mind ipari, mind otthoni méretekben. Gyakran adalékként és tartósítószerként használják a étel, kozmetikumok, italok stb. Néhány savas szilárd anyagot használnak katalizátorok (kémiai reakciógyorsítók) a petrolkémiai vagy papíriparban.
Vannak olyan savak is, amelyeket a fertőtlenítő szerek (karbolsav, szalicilsav). Ezenkívül felhasználhatók elektrolitként az autó akkumulátoraiban, mint a kénsav esetében. Ez utóbbi erős savat gyakran használják a ásványokIlyen a műtrágyák előállítása kőzetfoszfátokból.
Érdemes tisztázni, hogy bizonyos anyagokat csak savas közegben lehet oldani, és bizonyos reakciók csak ilyen körülmények között fordulnak elő. A salétromsavból és az ammóniából az ammónium-nitrát szintén fontos műtrágya a növények számára.
Példák savakra
Az alábbiakban húsz savat sorolunk fel példaként:
- Perklórsav (HClO4). Ez egy erős savfolyadék a hőfok környezet, erősen oxidáló hatású.
- Salétromsav (HNO3). Ez egy erős és intenzíven oxidáló sav, amelyet bizonyos robbanóanyagok és nitrogén műtrágyák előállítására használnak.
- Aszkorbinsav (C6H8VAGY6). C-vitamin, annyira szükséges az egészséghez. Antioxidáns hatása miatt védőanyag.
- Sósav (HClac)). Ez az egyetlen erős sav, amelyet az emberi test szintetizál. Ez a folyamat kifejezetten a gyomorban fordul elő a étel az emésztési folyamatban.
- Borkősav (C.4H6VAGY6). Fehér kristályos por, pezsgő italok készítéséhez, a pékségben, a borban és a gyógyszeriparban használják. A fogkrém, amelyet egyes receptek hordoznak, a borkősav.
- Fluorosav (HFac)). Az üveg megtámadásának képessége miatt kristályfaragásban és -metszésben használják.
- Kénsav (H2SW4). Ez egy kiváló sav par excellence, számtalan alkalmazási területtel rendelkezik iparágak és szintézis folyamatok.
- Trifluor-ecetsav (C2HF3VAGY2). Sokak számára jó oldószer szerves vegyületek.
- Foszforsav (H3PO4). Különböző kólaitalokban van jelen (alacsony koncentrációban). Ez egészségkárosítónak tekinthető, mivel elősegíti a vízkőmentesítést.
- Ecetsav (CH3COOH). Ez az ecet fő összetevője. Az általa létrehozott savasság miatt széles körben alkalmazott élelmiszer-tartósítószer.
- Fluorantimonsav (SbHF6). Ez a legerősebb ismert szuperav, 10-szer meghaladja a tiszta kénsav savasságát19.
- Krómsav (H2CrO4). Sötétvörös por, részt vesz a krómozás folyamatában. Kerámiák mázolására is használják.
- Indolecetsav (C10H9NEM2). Ez az auxinok fő képviselője, fontos a növények.
- Dezoxiribonukleinsav (DNS). Ez az, ami az élet kulcsa, mivel ez alkotja azokat a géneket, amelyek számtalan fehérje szintézisét irányítják.
- Trikarbonsavak. A karbonsavak egy csoportját tartalmazzák, amelyeknek három karbonsavcsoportja van (-COOH). Citromsav (C6H8VAGY7) Ez az egyik.
- Hangyasav (CH2VAGY2). A szerves savak közül a legegyszerűbb. Ennek a savnak a hosszan tartó expozíciója légzési elégtelenséget és halált okozhat.
- Glükonsav (C.6H12VAGY7). Ennek a savnak a sóit széles körben használják az üvegáru tisztítási folyamataiban.
- Tejsav (C3H6VAGY3). A biokémiai folyamatok fontos része.
- Benzoesav (C7H6VAGY2). Ez egy jellegzetes szagú sav, amelyet széles körben használnak olyan élelmiszerek tartósításához, amelyeknek a pH sav.
- Almasav (C4H6VAGY5). A gyógyszeriparban széles körben használják hashajtók előállítására.
- Szénsav (H2CO3). Egyes helyeken a barlangok kialakulásának része. A szénsavas italokban van jelen.



