A molekuláris geometria definíciója
Vegyes Cikkek / / January 11, 2022
Fogalmi meghatározás
Egy molekula szerkezete határozza meg az azt alkotó atomok háromdimenziós elrendezését a térben.

Vegyészmérnök
A molekuláris geometriákat jelenleg az alapján határozzák meg Elmélet a Valencia Layer elektronikus párjainak taszítása (TRPECV). Ez az elmélet lehetővé teszi a viselkedés előrejelzését kémiai anyagok (konkrétan kovalens) és segít megérteni a terjesztés elektronika, ami ahhoz vezet geometria a molekula. Ez pedig lehetővé teszi számunkra, hogy megértsük az anyagok számos tulajdonságát.
Ez az elmélet egy sor alapvető pilléren alapul, amelyeket áttekintünk, majd megpróbáljuk megérteni azokat Alkalmazás gyakorlat. Először is, a kötött és nem kötött (valencia) elektronokat olyan elektrontengernek tekintik, amelyek azonos típusú töltéssel rendelkeznek, taszítják egymást, így mindig olyan távol helyezkednek el a központi atomtól. molekula.
Másodszor, ez az elektrontenger vagy "elektronikus felhő" nagy elektronsűrűségű területeket képez, amelyek kötésekben állnak, ahol az elektronok megosztottak, vagy nem megosztott elektronpárokban. A kialakuló kötések lehetnek egyszeres, kettős vagy akár hármas kötések.
Végül azért döntsd el molekuláris geometria, nagyon hasznos a Lewis szerkezet, ahol megszámolják a központi atom körüli elektronsűrűség mennyiségét, és ez megadja jelzés geometriája nevéből és a molekula háromdimenziós alakjából.
Meg kell jegyezni, hogy ezek a sűrűségek a lehető legtávolabb helyezkednek el egymástól, hogy a legstabilabb szerkezetet hozzák létre, és ahol kisebb a taszítás. Így először az elektronikus geometriát, majd a molekuláris geometriát azonosítják.
Hat sűrűségi fokozat
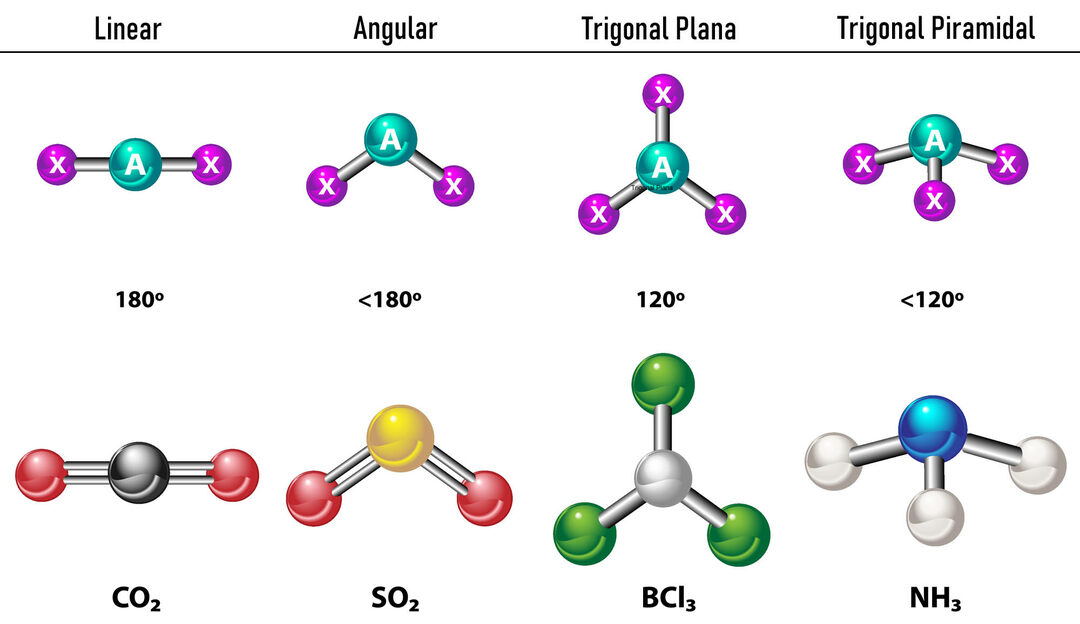
Abban az esetben, ha a központi atom körül két elektronsűrűség van, a kötések egymástól olyan távol helyezkednek el. közöttük, azaz 180°-ra egymástól, és ezért az elektronikus geometriájuk lineáris és molekulárisan is lineáris.
Abban az esetben, ha három elektronsűrűség van a központi atom körül, két lehetőség van: három kötés vagy két kötés és egy kötetlen pár. Ha három kötés van, akkor az elektronikus geometria Trigonális lapos120°-os szöggel a kötések között, és a molekuláris geometria ugyanazt a nevet viseli. Most, ha van nem kötött pár, akkor többel taszítják egymást intenzitás hogy a kötött töltések ezért hajlamosak kötésszögeket összenyomni. A szabad pár és az egyes kötések közötti szög 120º, az elektronikus geometria trigonális sík, míg a molekuláris geometria szögletes.
Abban az esetben, ha a központi atom körül négy elektronsűrűség van, az elektronikus geometria tetraéderes. Ha mind a négy elektronpár össze van kötve, akkor a molekuláris geometria név szerint egybeesik az elektrongeometriájukkal, és a kötési szög 109,5º. Most, ha az egyik pár szabad, a kötési szög kisebb lesz (107º), és a molekuláris geometria típusos. Trigonális piramis. Végül, ha kettő szabad pár és kettő össze van kötve, akkor a kötési szög 104,5°, míg a molekuláris geometriát ún. Szögletes.
Ha a központi atom körüli elektronsűrűség eléri az ötöt, azt a-nak nevezzük Trigonális bipiramis elektronikus geometriája. Ha az összes terhelés össze van kötve, akkor az egyenlítői kapcsolatok között 120ºC-os, az egyenlítői tengelyekkel pedig 90º-os szöget zárunk be. Manapság a molekuláris geometriát Trigonális Bipiramisnak is hívják, míg a négy összekapcsolt pár és egy szabad pár miatt a molekuláris geometria torzul, és a jól ismert "rocker”, Ott van a név, amit megszerz Torz tetraéder. Míg ha az öt elektronpárból kettő szabad, és közülük három kötődik, akkor annak „T” alakú geometriája van, és a nevét pontosan a szerkezetének köszönheti. Végül, ha fordítva van, három szabad pár és két kötött töltés, akkor a molekuláris geometria lineáris.
Végül hat elektronsűrűség van a központi atom körül, és egy oktaéder keletkezik, innen ered a neve az elektronikus geometriában. Hasonlóképpen, a molekuláris geometriát akkor nevezik el, ha minden párja össze van kapcsolva. Ha van öt összekapcsolt párja és egy szabad párja, akkor a molekuláris geometria négyzet alakú piramis. Ha négy kötött pár és két szabad pár van, akkor a molekuláris geometria a következő Négyzet alakú lakás.
ábra: Édes természet
Témák a molekuláris geometriában