A Raoult-törvény definíciója
Vegyes Cikkek / / February 21, 2022
fogalom meghatározása
Ez a kémia egyik törvénye, amelyet a francia Raoult dolgozott ki, ahol megállapítják, hogy a parciális gőznyomás A keveréket alkotó komponens megegyezik ugyanannak a tiszta komponensnek a parciális nyomásának a keverékben lévő móltörtével szorzatával. keverd össze.

Vegyészmérnök
Talán újra kell definiálni a gőznyomás fogalmát, úgy értelmezve, mint a gázfázis által a folyékony fázisra gyakorolt nyomást (mind a Egyensúly), bizonyos esetekben hőfok zárt rendszerben. Ez a dinamikus egyensúly annál gyorsabban jön létre, minél nagyobb a fázisok érintkezési felülete, és ebben az állapotban telített fázisokról beszélünk, gőzről és telített folyadékról egyaránt.
Ez törvény lefektette az egyik alapjait termodinamika 1887-ben és ezt követően logika A Raoult-törvényből azt látjuk, hogy egy anyag gőznyomásának értéke csökken, ha tisztaból keverék részévé válik. A fentiek alapján a kifejezés Ennek matematikája a következő:
Pén = xénL Pén0
Ez azt jelenti, hogy egy keverékben lévő i anyag parciális gőznyomása P_i egyenlő a tiszta komponens gőznyomásával, P
én0, (azonos hőmérsékleten) szorozva a folyadékfázisban lévő móltörtét, xénL.Amikor erről a törvényről beszélünk, az ehhez hasonló tipikus grafikonokra hivatkozunk:
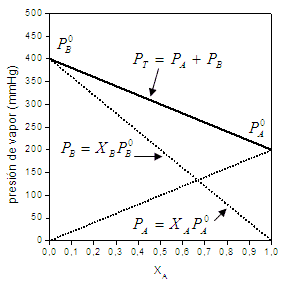
A kép az UCR3-ból készült
ezt az egyszerűt grafikus Nagyon hasznos a parciális gőznyomás becslésére, ha egy anyag egy keverék része, azt is lehetővé teszi, hogy leírjuk a keverék illékony oldószereinek összetételét annak gázfázisában, valamint sok más Alkalmazások.
A Raoult-törvény matematikai kifejezését minden grafikonon feltüntettük az A és B keverék komponenseire, jelen esetben két tiszta anyagból álló bináris keverékre. Az abszcissza tengelyen figyeljük az egyes komponenseknek megfelelő moláris frakciókat (folyékony fázisban), balra nagyobb mennyiségű B komponenst és arányosan kisebb mennyiségű A komponenst, amíg a B komponens mólaránya 1, az A komponensé az 0. Miközben jobbra az A komponens hányada növekszik, amíg csak az A komponenst nem kapjuk meg (xA=1). Az ordináták tengelyén rendre megvan a tiszta komponensek gőznyomása, vagyis amikor csak van A komponense (xA=1), megvan ennek a komponensnek a gőznyomása, és fordítva, a komponens ordináta tengelyén fordul elő bal. Az átmenet során a gázfázisú keverék össznyomása nem egyezik meg az egyes komponensek gőznyomásával. hanem összetevői parciális nyomásának összegére (Dalton törvénye), mindegyiket a Raoult.
Meg kell jegyezni, hogy az eredeti törvénynek vannak olyan módosításai, amelyek a vegyületeinek idealitásától való eltéréseken alapulnak. Amikor a működésbe lépő intermolekuláris erőktől függően kölcsönhatás lép fel a kettő között Ez eltéréseket generál, mivel többé-kevésbé hajlamos lesz valamelyik fázisban maradni folyékony vagy sem.
Röviden, ha az eltérés negatív Raoult ideális törvényétől, akkor az intermolekuláris erők az oldatban nagyobbak, mint a tiszta komponensekben, ezért a teljes nyomás kisebb lesz, mint a Becsült. Ez azt jelenti, hogy a tapadó erők erősebbek, mint a kohéziós erők, ami azt jelenti, hogy a komponenseket a keverék folyékony fázisában tartják vonzerő nagyobb, mint a tiszta folyadékoké. Másrészt, ha az eltérés pozitív, akkor a teljes nyomás nagyobb lesz, mint a becsült, mivel az oldatban az intermolekuláris erők kisebbek, mint a tiszta komponensekben. Itt a molekulák közötti kohéziós erők fontosabbak, mint az adhéziós erők, ezért a komponensek könnyebben mennek át a gázfázisba.
A Raoult-törvényt elsősorban az ipari technikákban alkalmazzák skála laboratóriumban, olyan eljárásokban, mint a desztilláció és a frakcionált desztilláció.
A Raoult-törvény témái
