Fogalom az ABC definíciójában
Vegyes Cikkek / / April 22, 2022
fogalom meghatározása
Az azeotrópok meghatározott összetételű kémiai vegyületek keverékei, amelyek bizonyos hőmérsékleteken forrnak. Alapvető jellemzője, hogy a keverék úgy viselkedik, mintha egyetlen tiszta anyag lenne, megőrzi tulajdonságait és megkönnyíti a kezelést.

Vegyészmérnök
A keveréket két vagy több komponens adhatja és annak fogalmazás folyadékfázisban és gázfázisban is ugyanaz, ez hasonlóságokat generál a tiszta anyagokkal. Ebből könnyen levezethető, hogy ezt a keveréket nem lehet komponenseire szétválasztani olyan eljárásokkal, mint pl frakcionált desztilláció, mivel, ahogy fentebb említettük, megőrzi arányait, és úgy viselkedik, mintha egyetlen összetevő.
További jellemző, hogy ennek a keveréknek a forráspontja lehet magasabb, alacsonyabb vagy akár egyenlő is lehet valamelyik komponensének forráspontjával. Amikor az azeotróp a hőfok A maximális forráspontnál maximális azeotrópnak nevezik, és ha ezt a lehető legalacsonyabb hőmérsékleten teszi, akkor minimális azeotrópnak nevezik. Ez azt jelenti, hogy a minimális azeotróp forráspontja alacsonyabb, mint a tiszta komponenseinek, és fordítva, a maximális azeotrópnál. Például a metanol-benzol keverékben az azeotróp minimális (0,61 benzol - 0,39 metanol frakciókban moláris), amelynek forráspontja 58 °C, olyan tartályban, ahol a benzol forráspontja 80 °C, a metanolé 65°C
Minimális és maximális azeotróp
Nos… honnan származik az azeotróp? Amikor eltérés van a Törvény Raoult, vagyis az azeotróp keverék gőznyomása nincs közvetlenül összefüggésben a moláris törtével, ekkor merül fel az azeotróp keverék fogalma. Ezek az eltérések akkor lépnek fel, ha a komponensek jelentősen vonzzák vagy taszítják egymást, vagyis az intermolekuláris erők nagyon eltérőek a különböző vegyületekben.
Ha az eltérés pozitív, akkor megvan a minimális azeotróp, míg ha az eltérés negatív, akkor a maximális azeotróp. A koncepció jobb megértése érdekében nézzünk meg néhány grafikát:
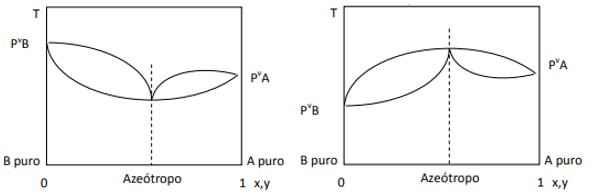
Itt megfigyelhetjük, hogy ha a keverék ideális lenne, a Raoult-törvény szerint a tiszta komponensek gőznyomását egyenes vonallal kellene összekötni, mivel Nos, van egy eltérés ettől a törvénytől, ami minimális és maximális azeotrópok képződését okozza, attól függően, hogy van-e nagyobb vagy kisebb affinitás a alkatrészek. Ha a Raoult-törvénytől való eltérés negatív, mint a bal oldali ábrán, akkor ez a minimum diagram nyomás, de maximum a hőmérséklet diagramban (tehát a maximum azeotrópja). Másrészt, ha az eltérés pozitív a Raoult-törvényhez képest, akkor ez a nyomás vs. összetétel, de minimum a hőmérséklet vs. diagramban. összetétele (itt van egy minimális azeotróp). Ne keverje össze a nyomás és a nyomás diagramjait. összetétel és hőmérséklet vs. fogalmazás.
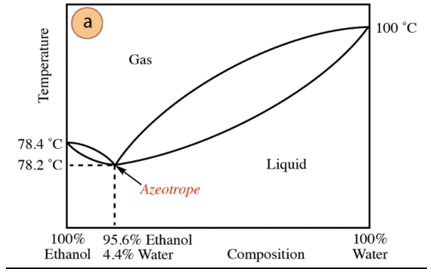
Az etanol-víz keverék esetében van egy minimális azeotróp, amelynek összetétele 95,6% etanol és 4,4% víz. Az azeotróp keverék forráspontja 78,2 °C-kal alacsonyabb, mint a tiszta komponenseké. Tehát tegyük fel, hogy magas víztartalmú (közel 100%-os) víz-etanol keveréket desztillálunk le. Tiszta alkoholt nem lehet előállítani, mivel minden desztillációs lépésben nagyobb frakciókat kapunk. etanol, de soha nem éri el a 100%-ot, fokozatosan megközelíti az azeotróp keverék összetételét (a legalacsonyabb pont alatt). Ez az oka annak, hogy a vízhez hasonlóan minimális azeotrópokat képez vele szerves vegyületek (a kölcsönhatásba lépő intermolekuláris erők típusától függően) a vizet előzetesen el kell távolítani a keverékből, hogy tiszta vegyületet kapjunk. Vagy ha az azeotrópot megkaptuk, a módszereket kitermelés további víz.
A fentiek alapján nem véletlenül találunk alkoholt (a szupermarketben ill gyógyszertár) 95%-kal a beszerezhető legolcsóbb termék. A tiszta alkohol előállításához az azeotrópot meg kell "törni". technika további, például szárítószerek vagy azeotróp desztillációk használata. Az azeotróp desztilláció abból áll, hogy egy extra komponenst adnak a keverékhez, amely elválasztással és kölcsönhatás a keverék bármely komponensével (nagyobb affinitású) eltávolítható a keverékből.
Témák az Azeotrópokban


