A kémiai egyensúly definíciója
Gátlás Húrelmélet / / April 02, 2023
1. A reverzibilis reakciókban jelenlévő stabilitási feltétel, ahol az előre és fordított reakciósebesség mindig ugyanaz marad.
Macska. nyelvtani: hímnemű főnév
szótagokban: e-qui-li-brio + quí-mi-co.
Kémiai egyensúly

Vegyészmérnök
Beindul a reakció egyensúly kémiai amikor a reakciósebesség közvetlen egyenlő sebesség fordított reakció. Minden kémiai reakció van egy bizonyos spontanitása az egyensúly felé, és ennek vizsgálatára a ∆G előjelen keresztül tesszük, Energia Gibbs-mentes, ami azt jelenti, hogy ennek a nagyságrendnek az értékén keresztül meg tudjuk jósolni, hogy egy reakció egy bizonyos irányban bekövetkezik-e vagy sem.
A Gibbs Free Energy ingadozása standard körülmények között általában a termékek és a reaktánsok energiái közötti különbségként fejeződik ki standard állapotban is:
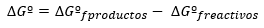
Míg ha a reakció nem szabványos körülmények között megy végbe, a ∆Gº és ∆G közötti összefüggést a következő határozza meg kifejezés:
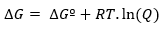
ahol Q a reakcióhányados.
A reakciósebesség és a kémiai egyensúly következményeinek megértéséhez tanulmányoznunk kell a ∆G előjelét:
Ha ∆G negatív, az azt jelenti, hogy a reakció közvetlen értelemben spontán (megtörténik).
Ha ∆G pozitív, az azt jelenti, hogy a reakció közvetlen értelemben nem spontán (nem következik be).
Míg ha ∆G=0, akkor nem lesz változás, mivel a rendszer egyensúlyban van, és mint már említettük, a közvetlen reakciósebesség megegyezik a közvetett reakciósebességgel. Ez azt jelenti, hogy a Q reakcióhányados megegyezik a K egyensúlyi állandóval, így nincs tendencia a reakció egy meghatározott irányának előnyben részesítésére.
Mivel a Q meghatározása a következő:
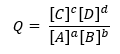
Általános reakcióhoz:
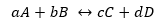
Míg a K ugyanazt a formát ölti, de a koncentrációk egyensúlyban vannak.
Ha visszamegyünk arra az esetre, amikor ∆G negatív, ez azt jelenti, hogy a Q reakcióhányados kisebb, mint K (állandó egyensúly), azt jelenti, hogy a termék koncentrációja kisebb, mint amennyinek lennie kellene, ha a reakció folyamatban lenne. egyensúly. Ezért a spontaneitás szempontjából közvetlen értelemben spontánsá válik.
Míg ha ∆G pozitív, akkor a szorzatok túlsúlya meghaladja azt, aminek lennie kellene, ha a rendszer egyensúlyban lenne, és Q nagyobb, mint K. Ezért a reakció fordított irányban spontán.
Meg kell jegyezni, hogy a Q és K szigorú meghatározása a termékek és a reagensek aktivitása szempontjából van megadva, az aktivitást koncentráció vagy nyomás tekintetében a következőképpen határozza meg:
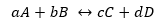
Ó hát:
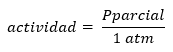
Ebből adódik, hogy mind a Q, mind a K dimenzió nélküli, és koncentrációban és parciális nyomásban egyaránt figyelembe vehető.
Ha a termékek és a reagensek koncentrációja vagy parciális nyomása idővel állandó marad, akkor ez a helyzet áll elő kémiai egyensúly, míg a dinamikus egyensúly helyzete azért jön létre, mert az előre és fordított reakció sebessége azonos. Fontos kiemelni az egyensúly dinamizmusát, kialakulásuk sebességét és fogyasztása termékek és reagensek azonosak, ezért a koncentrációk vagy a parciális nyomások nem ez változó.
Ha a feltétel eltávolodik az egyensúlyi helyzettől, akkor bizonyos fajok túlsúlyba kerülnek másokkal szemben, és onnan keletkezik a Kc direkt és inverz reakció sebességére vonatkozó kifejezés:
Tegyük fel a fent látható reakciót:
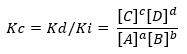
Mivel Kd és Ki, a reakciósebesség állandók előre, illetve fordított irányban.
Ismét, ha Kc>1, ez azt jelenti, hogy Ki kisebb, mint Kd, tehát a termékek nagymértékben átalakulnak reagensekké. Ebben az esetben az egyensúly a termékek felé tolódik el.
Ennek fordítottja történik, ha Kc<1, ami azt jelenti, hogy a közvetlen reakció sebessége kisebb, mint a közvetett reakciósebesség, és kevés fogyasztás reagensek közül az egyensúly a reagensek felé tolódik el.
Míg ha Kc=1, akkor a sebességek egyenlőek és a rendszer egyensúlyban van.
Két kérdést fontos meghatározni: először is, ennek az állandónak az értéke kizárólag a hőfok és viszont a termékek és a reagensek koncentrációjának vagy nyomásának kifejezésére használt nagyságrendtől függően változik.
Végül a törvény A kémiai egyensúly a híg oldatokhoz vagy alacsony nyomású gázokhoz igazodik.

