Térfogat-analízis példa
Kémia / / July 04, 2021
Tovább Analitikus kémia, a Volumetria egy elemzési módszer, amely a A sztöchiometrikus reakcióhoz az analitával szükséges reagens térfogatának mérése, amely a meghatározandó anyag.
Reagáljon sztöchiometrikusan a kémiailag kölcsönhatásba lépő anyagokra utal a kémiai egyenletet jelölő arány már kiegyensúlyozott.
A vizsgálandó anyagot ún Analyte. Ebből az anyagból egy ismert és pontosan mért térfogatot veszünk mintaként, amelyet hívunk Aliquotegy Erlenmeyer-lombikban található elemzés megkezdéséhez.
A volumetrikus elemzés fogalmai
A volumetrikus elemzés, amely egyfajta Kémiai elemzés, hordoz kémiai reakcióval járt. Ezt a kémiai reakciót a minta és a vizsgált anyag ismeretlen mennyisége, valamint egy ismert anyagmennyiség között hajtják végre, amely képes reagálni az előbbivel.
A A reakcióanyagok vizes oldatban lesznek, és megmérjük az oldatok térfogatát, amelyek kölcsönhatásba léptek a reakció végéig, ami látható lesz egy olyan indikátornak köszönhetően, amely színt ad a lombik belsejében.
A térfogati analízisben a
Az ismert koncentrációt standard megoldásnak nevezzük, Normál vagy Titrant, és referenciaként szolgál a reakció befejezéséhez, hogy elvégezzék a számítást, amely feltárja a vizsgált anyag mennyiségét.Ezt az eljárást úgy hívjuk meg, hogy mindkét megoldás reagáljon Kémiai fokozat o Értékelés, amely a volumetrikus elemzés alapvető része. Áll, hogy megy fokozatosan önteni a standard megoldást (Titrant) az alikvotban (Minta), amíg a jelző nem mutatja a változást színkülönbséggel.
A Indikátor Ez egy kémiai anyag, amelyet az alikvothoz adnak, színt mutatva, és amikor a reakció véget ér, megváltoztatja a színét.
A volumetrikus elemzés egyszerű lépések sorozatából áll:
1.- Standard oldat elkészítése
2.- A minta vagy az alikvot előkészítése
3.- kémiai fokozat
4.- Hangerő mérése
5.- A vizsgált anyag kiszámítása.
Addig a pontig, ahol már megtették teljesen reagált a két anyag, úgy hívják Ekvivalencia pont.
Mint minden kémiai elemzési módszerben, a Volumetrikus elemzésben is vannak követelmények a jó eredményekre:
-A kémiai reakciónak meg kell történnie SzelektívVagyis a standard oldat csak a mintával reagál.
-A kémiai reakciónak meg kell történnie Sztöchiometrikus, vagyis tartsa be a kiegyensúlyozott kémiai egyenletben megjelölt arányokat.
-A kémiai reakciónak meg kell történnie Mennyiségi; 99,9% -os teljességre utal az ekvivalencia ponton.
-Legyen egy kimutatható végpont a reakcióban, amelyet a mutató jobban megerősít.
Elsődleges minta
A Elsődleges minták Nagy tisztaságú anyagok, amelyek oldatbeli koncentrációját közvetlenül a kimért mennyiség és a felhasznált vízmennyiség alapján számítják ki.
A) Igen, működő megoldásokkal reagálhatunk, az utóbbiak koncentrációinak megismerésére és standard oldatokká alakítására.
Példák az elsődleges mintákra:
-Nátrium-karbonát (Na2CO3): Savak, például kénsav standardizálására szolgál.
-Kálium-biftalát: Az elsődleges standard a bázisok standard oldatainak, például a nátrium-hidroxidnak az elkészítése.
-Nátrium-klorid (NaCl): Ezüst-nitrát oldatok szabványosítására szolgál.
-Kálcium-karbonát (CaCO3): Az EDTA (etilén-diamin-tetraecetsav) elsődleges standardja.
Az elsődleges mintának számos alapvető jellemzőnek kell megfelelnie:
Kell egy Nagy tisztaságú, Légköri stabilitás, A hidratáló víz hiánya, Olcsó és könnyen beszerezhető, Y Nagy egyenértékű súly.
A volumetrikus elemzés osztályozása
Attól függően, hogy milyen vegyi anyagokkal dolgozik együtt az elemzés elkészítéséhez, ez a volumetria típusa lesz:
Sav-bázis térfogat: Vagy savval, mind bázissal működik a savakat vagy bázisokat tartalmazó minták elemzése.
Csapadéktérfogat: Argentometriának is nevezik, az ezüst-nitrát standard oldatát használja annak meghatározására, hogy hány klorid van a mintában.
Komplexitás volumetria: A keményítő, azaz a kalcium- és magnézium-karbonát koncentrációjának mérésére a vízben egy komplexképző szer, például EDTA standard oldatát használjuk.
REDOX térfogat: A reakció egy oxidáló és egy redukáló anyag között megy végbe.
Mutatók
A Volumetrics-ben használt számos mutató közül három kiemelkedik:
1.- Metil narancs: Az alikvot rész narancssárga színű, amelyet savval titrálunk. Az egyenértékűségi pont elérésekor a jelző sárga színűvé válik.
2.- Fenolftalein: Kezdetben átlátszó az alikvotban, amelyet egy alappal fognak címezni. Az egyenértékűségi pont elérésekor az indikátor rózsaszínűvé válik.
3.- Eriokróm fekete: Ez a mutató a víz keménységének meghatározására. Kezdetben lila az alikvot részében, amíg egy komplexképző szert nem titrálunk. A reakció végén elkékül.

Műszerek volumetrikus elemzésben
A térfogat-analízis során olyan eszközök sorozatát fogják használni, amelyek, ha nem állnak rendelkezésre, nem fejleszthetők megfelelően:
1.- Térfogatú lombik: Ez egy olyan tartály, mint egy izzó az alsó részén, alul ellapítva, amelynek vékony oszlopa van, amelybe a folyadékot adják. Van egy jelölése annak jelzésére, hogy hol kell lennie a folyadék meniszkuszának, hogy az fedje a pontos térfogatot. A standard megoldásokat tartalmazzák; térfogatának pontosságának köszönhetően ismert koncentráció biztosított.

2.- Pipetták: Osztott vékony csövek, amelyek lehetővé teszik a folyadék megbízhatóan pontos mennyiségének mérését. 25 ml-ig állnak rendelkezésre, és pontos mintavételt tesznek lehetővé.
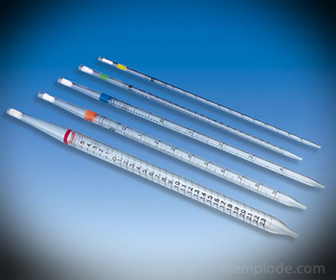
3.- Büretta: Ez egy hosszúkás cső, amelynek kapacitása 50 ml, amely tartalmazza a standard oldatot. Az egyik végén áramlásszabályozó szelep van, amely az oldatot az alikvotba üríti.
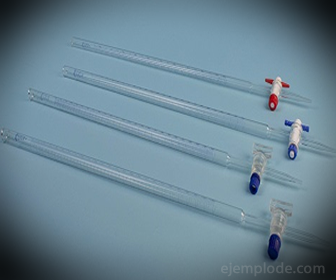
4.- Erlenmeyer-lombikok: lapos alapú, kúpos alakú tartályok, amelyek hengeres szélűek. Ez a kialakítás alkalmassá teszi őket kémiai titrálásokra, mivel nem engedik, hogy az oldatok rázása túlcsordítsa őket. Legalább háromra van szükség, ha ismételt tesztet kell végezni, a megbízható eredmény biztosítása érdekében.

Számítások volumetrikus elemzésben
Mivel vizes oldatokat kezelünk, a volumetrikus elemzés szempontjából fontos mennyiségek a koncentráció és a térfogat.
A volumetria fő egyenlete négy fő adaton alapul:
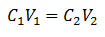
C1= Minta koncentrációja (ismeretlen)
V1= Az alikvot mennyisége, amellyel az elemzést dolgozták
C2= Az ekvivalencia pont eléréséhez használt standard oldat koncentrációja
V2= A reakció végének eléréséhez szükséges térfogat-standard oldat
Az adatokat az egyenlet helyettesíti, így csak a keresett koncentráció marad ismeretlen. Természetesen minden adatnak ugyanazon a meghajtón kell lennie.
Volumetrikus elemzési példák
Kloridok (Cl) meghatározása argentometriával, ezüst-nitráttal.
Bromidok (Br-) meghatározása argentometriával, ezüst-nitráttal.
Cianidok (CN-) meghatározása argentometriával, ezüst-nitráttal.
A magnézium-karbonát (MgCO3), komplexometriával, EDTA-val.
Kalcium-karbonát (CaCO3), komplexometriával, EDTA-val.
Kénsav-analízis (H2SW4) nátrium-hidroxiddal (NaOH).
A nátrium-hidroxid (NaOH) elemzése sósavval (HCl).
Antimon (III) meghatározása kálium-permanganáttal (KMnO4).
Az arzén (III) meghatározása kálium-permanganáttal (KMnO4).
Titán (III) meghatározása kálium-permanganáttal (KMnO4).
A molibdén (III) meghatározása kálium-permanganáttal (KMnO4).
Vas (II) meghatározása kálium-permanganáttal (KMnO4).
Oxalátion meghatározása kálium-permanganáttal (KMnO4).

