Szerves kémia példa
Kémia / / July 04, 2021
A Szerves kémia Ez az általános kémia része, amely a kémiai vegyületek tanulmányozásáért és funkcionális osztályozásáért felelős, és amelynek szerkezeti eleme a Szén, bőségesen jelen van a élő anyag; Ez a szervetlen kémia nagyon differenciált univerzumát hozza létre, amelyet az ásványi anyagokként besorolt kémiai vegyületeknek szentelnek.
A szénatom elektronikus konfigurációjának utolsó héjában négy elektron van. Ez a tulajdonság az atomsugarával együtt lehetővé teszi, hogy kovalens kötésekkel kapcsolódjanak máshoz ugyanazon elem atomjai, számos láncban, sokféle kémiai vegyületet alkotva stabil.
Ellenőrizheted Kovalens kötések.
Az ilyen kémiai vegyületek az ősszerkezetüket adó szénatomok mellett a szén vegyérték fő kiegészítőjeként hidrogénatomokat tartalmaznak. Ezen túlmenően a vegyületek ezen sokféleségében vannak olyanok, amelyek oxigénatomok közbeiktatásával Nitrogén, halogének, kén, sőt foszfor, alkáli és alkáliföldfém elemek, valamint a átmenet. Attól függően, hogy ki vesz részt a molekulában, ez lesz a végső anyag fizikai és kémiai tulajdonságai.
A szerves vegyületek az egész élő anyag; támogassák és fenntartsák mindenkit biológiai funkciókellentétben a szervetlen vagy ásványi anyagokkal, amelyeket az emberek kereskedelmi célokra, kísérletezésre vagy bizonyos háztartási feladatok ellátására használtak.
A szerves kémia története
1828 előtt már különbséget tettek a szerves kémia és a szervetlen kémia között. A szerves anyag egy alkotáshoz kapcsolódott a "életerő"és a szervetlenre az élettelenekkel, az ásványi anyaggal. Ezen elképzelések alapján nem várható, hogy szervetlen vegyületeket nyernek szervetlen anyagokból a laboratóriumban.
Azonban, 1828-ban Friedrich Wöhler (1800-1882) szerves anyagot sikerült előállítani, Karbamid CO (NH2)2, az állati anyagcsere fontos terméke, szervetlen vegyületekből. Kezelés Ólom-cianát Pb (CNO)2 val vel Ammónia NH3 hogy megszerezzem Ammónium-cianát NH4CNO; Ez a vegyület valóban létrejött, de amikor az oldatot az ammónium-cianát kristályosítása céljából forralták, karbamiddá alakították át.
Ez a kémiai változás a példa Belső átcsoportosítás, amelyben a molekulában lévő atomok száma vagy osztálya nem változik, csak azok sorrendje benne van. Az ilyen típusú transzformációk nagyon gyakoriak a szerves kémia területén.
Wöhler felfedezése később elindította az életerő elméletének elhagyását teljesen eldobják, és sok más szerves vegyület előállítása követi a laboratórium. Ennek ellenére a szervetlen és szerves tulajdonságok megmaradnak, mivel a szervetlen vegyületek ásványi termékekkel állnak kapcsolatban és a szerves vegyületek, amelyek valójában a szén és a hidrogén vegyületei és származékaik, az élő szervezetek által termeltek.
Bár az általános kémia törvényei mindkét vegyületre egyformán vonatkoznak, különböző okok indokolják és szükségessé teszik ezt a felosztást. Így a szerves és szervetlen vegyületek különböző tulajdonságokban különböznek, például: ezek Oldékonyság előnyös szerves oldószerekben (éter, alkohol, kloroform stb.), illetve vízben Stabilitás (a szerves vegyületek viszonylag alacsony hőmérsékleten bomlanak le), és a A reakciók jellege; szervetlen vegyületek esetében ionosak, egyszerűek és gyakorlatilag azonnaliak, szerves vegyületek esetében pedig kovalensek, összetettek és lassúak.
Szerves vegyületek
Legfeljebb kilencven atomot tartalmazó szénvegyületek ismertek. A láncok Szénatomok lehetnek egyenes és elágazó és egyetlen kovalens kötésük van, vagy kettős vagy hármas kötésük van. Több mint 2500 vegyületről ismert, hogy csak szenet és hidrogént (Szénhidrogének).
Szerves vegyületek izomerizmusa
Szervetlen vegyületekben a képlet általában egyetlen vegyületet jelent; így csak egy H képletű anyag létezik2SW4. A kénsavmolekula két hidrogénatomot tartalmaz, az egyiket a kén és a négy oxigént, egyedi és egyedi elrendezésben. Szerves vegyületekben az ritkán fordul elő ilyen. Így például két olyan vegyület van, amely reagál a C képletre2H6Vagy etil-alkohol vagy etanol és dimetil-éter.

Minél összetettebb a molekula, vagyis minél nagyobb a szénatomok száma, annál nagyobb a lehetséges izomerek száma.
Szerves vegyületek elemzése
Egy szerves vegyület elemzése a következőket tartalmazza: kvalitatív elemzés, a mennyiségi elemzés és a Funkcionális elemzés. Abban az esetben, ha feltételezzük, hogy a vegyület tisztátalan állapotban van, korábban tisztítottuk Kristályosodás, Lepárlás, Szublimáció, Kivonásstb. A tisztasági kritérium fizikai állandói, például olvadáspont, forráspont, sűrűség, oldhatóság, kristályos forma, törésmutató stb. Alapján ítélhető meg.
A kvalitatív elemzés Ezt a vegyületet alkotó elemek, különösen a szén, a hidrogén és a nitrogén, valamint a halogén, a kén és a foszfor jelenlétének vizsgálatával ellenőrizzük.
A mennyiségi elemzés A kvalitatív elemzéshez használt módszerek alapjául szolgál. A kiindulási pont egy bizonyos mennyiségű anyag, amely éget, és a szén-dioxidot összegyűjtik és lemérik. a szén és a vízgőz képződött a szén és a hidrogén százalékos arányának kiszámításához a összetett. A kvantitatív elemzés eredményei megkönnyítik a empirikus képlet, bár a molekulaképlet csak az anyag molekulatömegének meghatározása után található meg. De a probléma még nem megoldott, mert ugyanaz a molekulaképlet különböző izomereknek felelhet meg.
Szerves vegyületek osztályozása
Szerkezetük szerint a szerves vegyületeket vegyületekre osztják alifás, aromás Y heterociklusos. Az alifás vegyületek rokonok a metán CH-val4, nyitott láncúak, kivéve a cikloparaffinokat, és nevüket annak köszönhetik, hogy az állati és növényi zsírok ebbe a csoportba tartoznak.
A aromás vegyületek, zárt láncú, szorosan rokon a benzollal, C6H6, és nevüket annak köszönhetik, hogy sokuknak illatos, kellemes illata van.
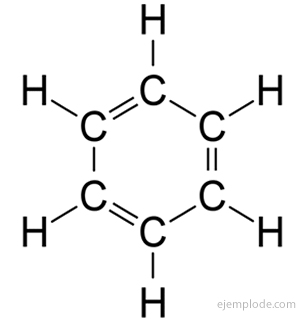
Benzol gyűrű
A heterociklusos vegyületek Zárt láncú vegyületek, amelyek gyűrűjében a szénatomtól eltérő elem található.
Alkotmányuk szerint:
Szénhidrogének, amely viszont a linkjeinek típusa miatt a következők közé sorolható Alkanes, Alkének Y Alkynes. Ezenkívül a cikloalkánok, a benzol és ezek csak szénből és hidrogénből álló származékai tartoznak ebbe a kategóriába.
Heterociklusos vegyületek
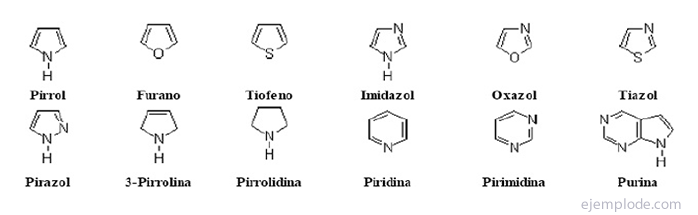
Halogénezett származékok:R-X
Nitrovegyületek:R-NO2
Szulfonsavak:R-SO3H
Nitrilek (OR alkil-cianidok) és izonitrilek:R-CN és R-NC. Abban különböznek, hogy a nitrogénatom hogyan kapcsolódik a molekulához.
Alkoholok:R-OH
Fenolok: Vegyületek, amelyek gerincén alapulnak egy benzolgyűrű és hozzáadott hidroxilcsoport.

Éterek:R-O-R
Merkaptánok: R-SH
Tioéterek:R-S-R
Tio-savak:R-COSH
Aldehidek:R-CHO
Ketonok:R-CO-R
Karbonsavak:R-COOH
Kimész:R-COOM (M a fémhez)
Észterek: R-COO-R
Anhidridek: R-CO-O-OC-R
Aminok:R-NH2, R-NH-R, 2R-N-R
Aldosa típusú szénhidrátok:-CHOH-CHOH-CHO
Ketóz típusú szénhidrátok:-CHOH-CO-CH2Oh
Fémorganikus vegyületek:R-M-R
Fém-alkil-halogenidek:R-MX (más néven Grignard Reagens)

