20 Contoh Gas Ideal dan Gas Nyata
Bermacam Macam / / July 04, 2021
Itu kimia adalah ilmu yang mempelajari komposisi dan transformasi yang dapat terjadi pada materi, dalam segala bentuknya. Salah satu bidang studi yang paling penting dalam kimia adalah gas.
Itu konsep gas Itu didirikan oleh ahli kimia Belgia Jan van Helmont. Untuk menjelaskan perilaku gas, persamaan matematika yang berbeda dikembangkan menggunakan alat statistik. Namun, persamaan ini perlu disederhanakan dan dimodifikasi karena tidak dapat digunakan untuk semua jenis gas, sehingga model gas yang berbeda didefinisikan (gas ideal kamu gas nyata, di antara pendekatan perantara lainnya). Sebagai contoh: nitrogen, helium, metana.
Dalam pengertian ini, tiga hukum ditetapkan untuk menghubungkan secara umum volume, suhu dan tekanan gas:
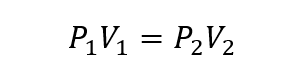
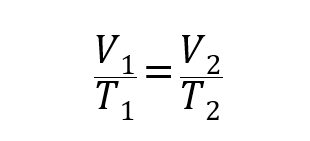
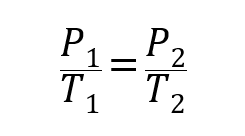
Dimana P1, V1 kamu T1adalah tekanan awal, volume dan suhu gas masing-masing, dan P2, V2 kamu T2 adalah final.
Jadi, dengan menghubungkan ketiga hukum tersebut, kita peroleh Hukum Gas Umum,
PV / T = C dimana C adalah konstanta yang bergantung pada jumlah gas.
Contoh gas ideal
Itu gas ideal itu adalah model teoritis yang mewakili gas yang tidak benar-benar ada. Ini adalah alat untuk memfasilitasi sejumlah besar perhitungan matematis, karena sangat menyederhanakan perilaku kompleks gas. Gas ini dianggap terdiri dari partikel-partikel yang tidak saling tarik-menarik atau tolak-menolak dan tumbukannya bersifat lenting mutlak. Ini adalah model yang gagal jika gas mengalami tekanan tinggi dan suhu rendah.
Itu persamaan umum gas ideal dihasilkan dari kombinasi hukum Boyle-Mariotte, Charles dan Gay Lussac dengan hukum Avogadro. Hukum Avogadro menyatakan bahwa jika zat gas yang berbeda terkandung dalam volume yang sama dan diberi tekanan dan suhu yang sama, maka mereka memiliki jumlah dari partikel. Dengan demikian, persamaan keadaan gas ideal adalah: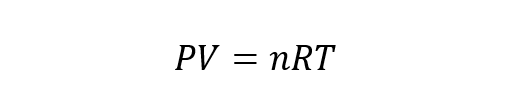
Dimana tidak adalah jumlah mol gas dan R adalah konstanta gas sama dengan 8,314 J / Kmol.
Tidak mungkin untuk membuat daftar spesifik dari gas ideal karena merupakan a gas hipotetis. e dapat membuat daftar sekelompok gas (termasuk gas mulia) yang perlakuannya dapat didekati dengan gas ideal, karena karakteristiknya serupa, asalkan kondisi tekanan dan suhunya normal.
- Nitrogen (N2)
- Oksigen (O2)
- Hidrogen (H2)
- Karbon dioksida (CO2)
- Helium (Dia)
- Neon (Ne)
- Argon (Ar)
- Kripton (Kr)
- Xenon (Xe)
- Radon (Rn)
Contoh gas nyata
Itu gas nyata Mereka adalah mereka yang memiliki perilaku termodinamika dan itulah sebabnya mereka tidak mengikuti persamaan keadaan yang sama seperti gas ideal. Dalam tekanan tinggi dan suhu rendah, gas pasti harus dianggap nyata, karena dalam hal ini interaksi antara partikelnya meningkat.
Itu perbedaan substansial antara gas ideal dan gas nyata adalah bahwa yang terakhir tidak dapat dikompresi tanpa batas tetapi kapasitas kompresinya relatif terhadap tingkat tekanan dan suhu.
Persamaan yang berbeda telah dikembangkan untuk menjelaskan perilaku gas nyata. Salah satu yang paling penting adalah yang disediakan oleh Van der Waals pada tahun 1873, yang harus diterapkan di bawah kondisi tekanan tinggi. Itu Persamaan Van der Waals direpresentasikan sebagai:
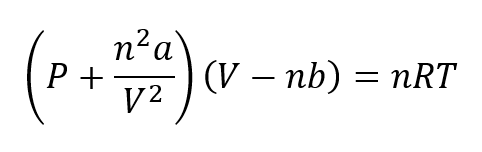
Dimana untukkamu bmereka adalah konstanta yang mengacu pada sifat masing-masing gas.
Daftar berikut menunjukkan beberapa contoh gas nyata, meskipun Anda juga dapat menambahkan yang sudah: telah terdaftar sebagai gas ideal, tetapi kali ini dalam konteks tekanan tinggi dan / atau rendah suhu.
- Amonia (NH3)
- Metana (CH4)
- Etana (CH3CH3)
- Eten (CH2CH2)
- Propana (CH3CH2CH3)
- Butana (CH3CH2CH2CH3)
Ikuti dengan:
