Contoh Hukum Charles
Fisika / / November 13, 2021
Hukum gas Charles atau Hukum tekanan konstan, adalah salah satu dari hukum gas, diucapkan oleh Gay-Lussac, yang merilis karya Jacques Charles, diterbitkan sekitar 20 tahun sebelumnya.
Hukum Charles memprediksi perilaku massa gas ketika tekanan tetap konstan dan suhu dan volume bervariasi.
Hukum Charles dinyatakan sebagai berikut:
Pada tekanan tetap, volume gas berbanding lurus dengan perubahan suhunya.
Tekanan konstan: mengacu pada fakta bahwa tekanan yang diberikan gas pada dinding wadah tidak akan bervariasi sepanjang pengalaman.
Volume: itu adalah ruang yang ditempati gas, secara umum dianggap sebagai wadah dengan dinding yang tidak berubah bentuk, dan tutupnya berfungsi seperti pendorong.
Suhu: Ini adalah peningkatan atau kehilangan panas yang dialami gas selama eksperimen. Jika suhu meningkat, volume meningkat. Jika suhu menurun, volume juga berkurang.
Secara aljabar, Hukum Charles dinyatakan dengan rumus berikut:

Di mana:
V = volume gas
T = suhu gas
k = konstanta proporsionalitas untuk massa gas tersebut.
Ini berarti bahwa untuk massa gas tertentu, pada tekanan konstan, hubungan antara volume dan variasi suhu, akan selalu memiliki hubungan proporsionalitas yang sama, diwakili oleh konstanta k:

Jadi setelah konstanta ditentukan, kita dapat menghitung nilai lain dari data lain yang diketahui:
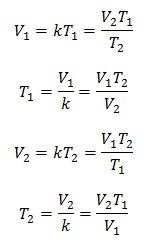
3 Contoh Hukum Charles yang diterapkan pada masalah:
Contoh 1: Hitunglah volume baru, jika dalam sebuah wadah terdapat massa gas yang menempati volume 1,3 liter, pada suhu 280 K. Hitung volume ketika mencapai suhu 303 K.
V1 = 1,3 liter.
T1 = 280 K
V2 = ?
T2 = 303 K
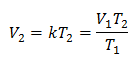
Mengganti nilai:
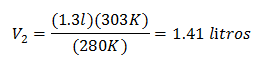
Volume baru pada 303 K adalah 1,41 liter.
Contoh 2. Jika kita memiliki gas yang menempati 2,4 liter pada 10 derajat Celcius, hitunglah suhu akhirnya, jika pada akhirnya menempati 2,15 liter.
V1 = 2,4 l
T1 = 10 ° C = 283 K
V2 = 2,15 l
T2 = ?
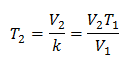
Mengganti nilai:
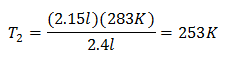
Suhu baru adalah 253 K, yang sama dengan -20 ° C.
Contoh 3. Kami memiliki gas yang suhu awalnya adalah 328 K, volume akhirnya adalah 3,75 l, dan konstanta rasionya adalah 0,00885.
V1 = ?
T1 = 328 K
V2 = 3,75 l
T2 = ?
k = 0,00885
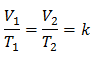
Mengganti nilai:
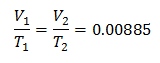
Untuk mengetahui Volume Awal:
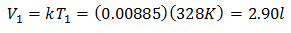
Volume awalnya adalah 2,90 liter.
Untuk mengetahui suhu akhir:
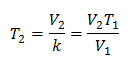
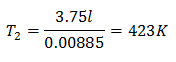
Suhu akhir akan menjadi 423 K, yang sama dengan 150 ° C.



