25 Contoh Halida
Contoh / / November 09, 2023
A halida atau halida itu sebuah senyawa kimia biner yang terdiri dari a atom halogen dan unsur atau kation yang mempunyai keelektronegatifan lebih rendah dibandingkan halogen. Misalnya:
- Natrium klorida (NaCl)
- Kalsium fluorida (CaF2)
- Kalium bromida (KBr)
- Hidrogen klorida (HCl(G))
Halogen adalah unsur kimia yang membentuk kelompok 17 dari Tabel periodik. Unsur-unsur halogen adalah: Fluor (F), Klorin (Cl), Brom (Br), Yodium (I), Astatin (At), Teneso (Ts).
- Lihat juga: Aldehida dan keton
Jenis halida
Tergantung pada komposisinya, halida dapat berupa:
- Halida anorganik. Mereka adalah senyawa kimia anorganik yang mengandung satu atau lebih atom halogen. Dapat berupa garam anorganik, hidrogen halida, atau kompleks logam. Misalnya: natrium klorida (NaCl) dan anion tetraiodomerkurat HgI42-.
- Halida organik. Mereka adalah senyawa kimia organik yang mengandung satu atau lebih atom halogen yang terikat pada atom karbon dari senyawa organik. Misalnya: metil klorida (CH3 – Cl) dan triklorometana (CH – Cl3).
Contoh halida
- Natrium klorida (NaCl)
- Kalsium klorida (CaCl2)
- Perak fluorida (AgF)
- Litium fluorida (LiF)
- Kalium iodida (KI)
- Kalium bromida (KBr)
- Tembaga(II) klorida (CuCl2)
- Besi(III) klorida (FeCl3)
- Kromium(III) bromida (CrBr3)
- Aluminium klorida (AlCl3)
- Amonium klorida ((NH4)Cl)
- Timbal(II) iodida (PbI2)
- Magnesium iodida (MgI2)
- Berilium fluorida (BeF2)
- Aluminium fluorida (AlF3)
- Bromometana (CH3 – Br)
- Iodoform (CHI3)
- Metil klorida (CH3 –Cl)
- Bromoetana (CH3 – CH2 – Br)
- Dikloroetana (Cl – CH2 – CH2 –Cl)
- Perak bromida (AgBr)
- Timah(IV) klorida (SnCl4)
- Titanium(IV) klorida (TiCl4)
- Hidrogen klorida (HCl(G))
- Hidrogen bromida (HBr(G))
Sifat fisik halida
Beberapa sifat fisik halida adalah:
- Alkil halida (halida organik) memiliki kepadatan dan titik didih yang lebih tinggi dibandingkan alkana sejenisnya. Hal ini terjadi karena atom halogen yang menggantikan atom hidrogen di dalamnya hidrokarbon dari mana halida itu berasal.
- Fluorida dan klorida organik memiliki kepadatan yang lebih kecil dibandingkan air, sedangkan bromida dan iodida organik lebih padat daripada air.
- Alkil halida tidak larut dalam air dan larut dalam pelarut organik.
- Hidrogen halida adalah gas dengan bau menyengat pada suhu kamar.
- Halida yang terbentuk dengan atom unsur-unsur golongan 1 Tabel Periodik berbentuk padatan berwarna putih.
Sifat kimia halida
- Alkil halida mengalami reaksi substitusi nukleofilik alifatik. Ini adalah reaksi di mana atom nukleofilik (kaya elektron) menggantikan atom (gugus kiri) yang terikat pada atom elektrofilik (kekurangan elektron).
Misalnya: dalam reaksi metil bromida (CH3 – Br) dengan natrium hidroksida (NaOH), brom (gugus pergi) digantikan oleh ion hidroksida (nukleofil) dalam metil bromida, dengan karbon sebagai elektrofilnya.
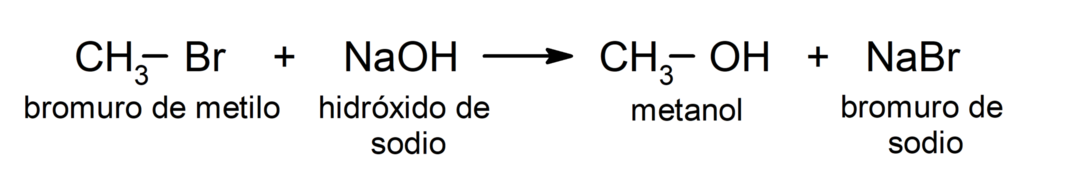
- Beberapa alkil halida bereaksi dengan magnesium dalam pelarut seperti eter atau tetrahidrofuran, dan produk yang dihasilkan adalah senyawa organologam yang disebut “reagen Grignard”. Misalnya: etil bromida (CH3 – CH2 – Br) dengan magnesium (Mg) bereaksi dalam media kering menghasilkan etilmagnesium bromida (CH3 – CH2 – MgBr).

- Alkil halida primer mengalami reaksi dengan alkoksida atau alkohol dalam medium dasar untuk menghasilkan eter. Reaksi ini dikenal sebagai “sintesis Williamson.” Misalnya: reaksi antara metil bromida (CH3Br) dan natrium metoksida (CH3ONa) menghasilkan dimetil eter (CH3OCH3).
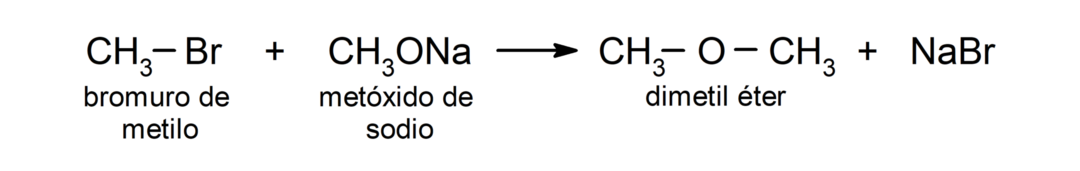
Kegunaan halida
Halida atau halida memiliki berbagai kegunaan dalam industri, kedokteran, dan kehidupan sehari-hari. Beberapa aplikasi tersebut adalah:
- Mereka digunakan sebagai pelarut bagi banyak orang senyawa organik.
- Mereka digunakan sebagai desinfektan dan antiseptik.
- Mereka telah digunakan sebagai pendingin.
- Mereka digunakan dalam pembuatan polimer berfluorinasi. Misalnya teflon.
- Mereka digunakan sebagai garam yang dapat dimakan atau tincture dalam pengobatan.
- Mereka digunakan dalam pengolahan dan pemurnian air.
- Logam halida digunakan dalam pembuatan lampu.
- Mereka digunakan untuk membersihkan komponen elektronik.
- Mereka digunakan sebagai bahan kimia awal untuk mensintesis senyawa organik yang lebih kompleks.
- Beberapa diantaranya, seperti perak bromida (AgBr), digunakan dalam pengembangan pelat fotografi.
Bahaya halida
Alkil halida yang digunakan sebagai pelarut bereaksi hebat dengan basa kuat dan oksidan kuat, yang dapat menyebabkan ledakan dan kebakaran.
Selain itu, klorofluorokarbon (CFC) adalah alkil halida yang telah digunakan selama beberapa dekade sebagai zat pendingin, namun kandungannya Pekerjaan telah dilarang oleh entitas internasional karena merekalah yang paling bertanggung jawab atas lubang di lapisan tersebut ozon.
Di sisi lain, hidrogen halida mengiritasi mata, kulit, dan selaput lendir.
Ikuti dengan:
- Kamu keluar
- garam asam
- garam netral
Referensi
- SALOMON, T. G. (1996). Dasar-dasar Kimia Organik. Wiley.
- Whitten, K. W., Gailey, K. D., Davis, R. E., de Sandoval, M. T. KE. O., & Muradás, R. M. G. (1992). Kimia umum (hal. 108-117). McGraw-Hill.
- sumur, A. F. (1978). Kimia anorganik struktural. Kembali.


