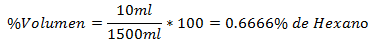Contoh Konsentrasi: Molaritas, Molalitas, Normalitas dan Persentase
Kimia / / July 04, 2021
Itu Konsentrasi didefinisikan sebagai Kuantitas atau Proporsi zat tertentu, hadir dalam Solusi. Solusinya adalah campuran homogen (fase tunggal terlihat) yang dapat padat, cair atau gas, sehingga Konsentrasi dapat diekspresikan dengan cara yang berbeda.
Perlu untuk mendefinisikan bahwa Solusi berisi dua komponen utama: zat terlarut dan pelarut, dan umumnya, Konsentrasi berfokus pada mengungkapkan berapa banyak Zat terlarut dicampur dalam Solusi Utuh. Namun, Konsentrasi dapat mengungkapkan kuantitas atau proporsi dari salah satu dari mereka.
Ekspresi Konsentrasi
Dalam Kimia, jumlah zat yang ada dalam larutan dapat dinyatakan dalam beberapa cara berbeda: Molaritas, Molalitas, Normalitas, Persentase berat, Persentase volume.
Dari lima unit ini, semuanya dapat diterapkan pada larutan padat, cair, dan gas. Tetapi Molalitas, misalnya, adalah yang paling banyak digunakan untuk larutan padat.
Contoh Molaritas
Itu Molaritas menunjukkan berapa mol zat dalam setiap Liter Larutan Lengkap. Ini adalah unit yang paling sering digunakan dalam kimia untuk larutan cair, saat melakukan Analisis Volumetrik. Dilambangkan dengan huruf "M".
Mengetahui gram zat terlarut, mereka dibagi dengan berat molekul zat terlarut. Dengan demikian, mol zat terlarut yang ada dalam larutan diperoleh.
Kemudian, Mol Solute dibagi dengan Liter of Solution, dan dengan demikian satuan Molaritas diperoleh: Mol of Solute / Liter of Dissolution.
1.- Untuk larutan 0,5 liter Magnesium Hidroksida [Mg(OH)2], dan jika Berat Molekul Magnesium Hidroksida adalah 58 g / mol. Anda memiliki 36 gram itu.
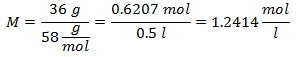
2.- Untuk 1 liter larutan Kalsium Hidroksida [Ca(OH)2], dan jika Berat Molekul Kalsium Hidroksida adalah 74 g / mol. Anda memiliki 42 gram itu.

3.- Untuk larutan 3 liter Natrium Klorida (NaCl), dan jika Berat Molekul Natrium Klorida adalah 58 g/mol. Anda memiliki 28 gram itu.
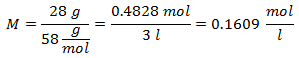
4.- Untuk larutan 5 liter Kalsium Klorida (CaCl2), dan jika Berat Molekul Kalsium Klorida adalah 110 g / mol. Anda memiliki 13 gram.
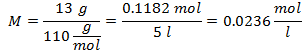
5.- Untuk larutan 10 liter Natrium Sulfat (Na2SW4), dan jika Berat Molekul Natrium Sulfat adalah 142 g / mol. Anda memiliki 96 gram itu.
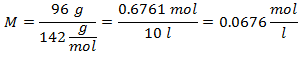
Contoh Molalitas
Itu Molalitas menunjukkan berapa mol zat terlarut per 1000 gram pelarut grams dalam Solusi. Ini adalah unit yang paling banyak digunakan dalam kimia untuk larutan padat. Dilambangkan dengan huruf "m".
Mengetahui gram zat terlarut, mereka dibagi dengan berat molekul zat terlarut. Dengan demikian, mol zat terlarut yang ada dalam larutan diperoleh.
Kemudian, mol zat terlarut disesuaikan untuk setiap 1000 gram larutan, yang terbentuk sebagai dasar perhitungan, dan dengan demikian diperoleh satuan molalitas: Mol zat terlarut / 1000g Pelarut
1.- Untuk larutan dengan 1000g pelarut Mineral dan 36 gram Magnesium Hidroksida [Mg (OH)2], dan jika Berat Molekul Magnesium Hidroksida adalah 58 g / mol.

2.- Untuk larutan 2000g pelarut Mineral dan 42 gram Kalsium Hidroksida [Ca(OH)2], dan jika Berat Molekul Kalsium Hidroksida adalah 74 g / mol.
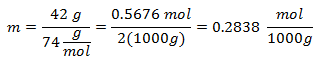
3.- Untuk larutan 3000g Pelarut Mineral dan 28 gram Natrium Klorida (NaCl), dan jika Berat Molekul Natrium Klorida adalah 58 g/mol.
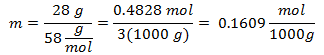
4.- Untuk larutan 5000g pelarut Mineral dan 13 gram Kalsium Klorida (CaCl2), dan jika Berat Molekul Kalsium Klorida adalah 110 g / mol.
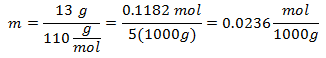
5.- Untuk larutan 10.000g pelarut Mineral dan 96 gram Natrium Sulfat (Na2SW4), dan jika Berat Molekul Natrium Sulfat adalah 142 g / mol.
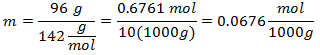
Jumlah pelarut ditangani sebagai kelipatan 1000g, meninggalkan 1000 gram sebagai referensi dan tidak memasukkannya, yang mempengaruhi perhitungan.
Contoh Normalitas
Itu Normalitas menunjukkan berapa banyak ekuivalen zat dalam setiap liter larutan lengkap. Normalitas adalah satuan lain yang paling sering digunakan dalam kimia untuk larutan cair, ketika melakukan Analisis Volumetrik. Dilambangkan dengan huruf "N".
Setara adalah satuan yang dihasilkan dari membagi gram Zat terlarut (g) dengan Berat Setara (Kecil). Berat Ekuivalen (Peq) dihasilkan dari membagi Berat Molekul (PM) dengan Valencia aktif (*), yang lebih mudah diamati dalam Asam dan Basa. Misalnya, Valencia dari Asam Hidroklorat (HCl) aktif adalah 1; Valencia dari Kalsium Hidroksida [Ca (OH) aktif2] adalah 2, karena ion Hidrogen (H +) dan Hidroksil (OH-) yang masing-masing hadir.
Kemudian, Setara Zat terlarut dibagi dengan Liter Larutan, sehingga diperoleh satuan Normalitas: Setara Zat terlarut / Liter Larutan.
1.- Untuk larutan 0,5 liter Magnesium Hidroksida [Mg(OH)2], dan jika Berat Molekul Magnesium Hidroksida adalah 58 g / mol. Anda memiliki 36 gram itu.
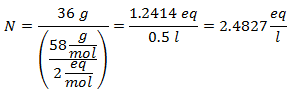
2.- Untuk 1 liter larutan Kalsium Hidroksida [Ca(OH)2], dan jika Berat Molekul Kalsium Hidroksida adalah 74 g / mol. Anda memiliki 42 gram itu.
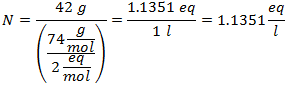
3.- Untuk larutan 3 liter Natrium Klorida (NaCl), dan jika Berat Molekul Natrium Klorida adalah 58 g/mol. Anda memiliki 28 gram itu.
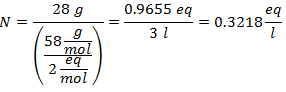
4.- Untuk larutan 5 liter Kalsium Klorida (CaCl2), dan jika Berat Molekul Kalsium Klorida adalah 110 g / mol. Anda memiliki 13 gram.
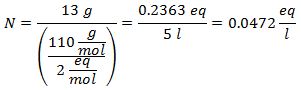
5.- Untuk larutan 10 liter Natrium Sulfat (Na2SW4), dan jika Berat Molekul Natrium Sulfat adalah 142 g / mol. Anda memiliki 96 gram itu.
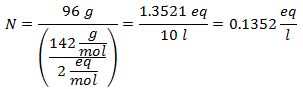
Contoh Persentase berdasarkan Berat
Itu Persentase Berat adalah ekspresi dari Konsentrasi yang dihasilkan dari membagi Jumlah dalam gram Solut antara gram Total Solution. Memperoleh kuantitas desimal, itu dikalikan dengan 100 dan dinyatakan dengan simbol "%". Unit ini umumnya digunakan untuk mengukur konsentrasi dalam campuran padat atau granular.
1.- Campuran total 1300g mengandung 13g Kalsium Karbonat. Persentase Beratnya adalah:
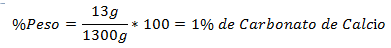
2.- Campuran 100g total mengandung 26g Gula. Persentase Beratnya adalah:
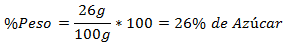
3.- Campuran total 250g mengandung 60g Natrium Klorida. Persentase Beratnya adalah:
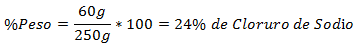
4.- Campuran total 800g mengandung 150g Kalsium Hidroksida. Persentase Beratnya adalah:
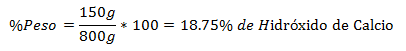
5.- Campuran 1500g total mengandung 10g Sodium Bicarbonate. Persentase Beratnya adalah:
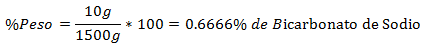
Contoh Persentase Volume
Itu Persentase dalam Volume adalah ekspresi dari Konsentrasi yang dihasilkan dari membagi kuantitas dalam satuan Volume Zat terlarut dibagi dengan Volume Solusi Total. Memperoleh kuantitas desimal, itu dikalikan dengan 100 dan dinyatakan dengan simbol "%". Satuan ini umumnya digunakan untuk mengukur konsentrasi dalam campuran komponen cair atau gas.
1.- Campuran total 1300ml mengandung 130ml Etanol. Persentase Volume adalah:
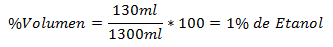
2.- Campuran 100ml total mengandung 26ml Gliserin. Persentase Volume adalah:
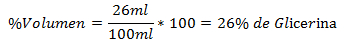
3.- Campuran 250ml total mengandung 60ml Ethyl Ether. Persentase Volume adalah:
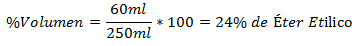
4.- Campuran total 800ml mengandung 150ml Glycol. Persentase Volume adalah:
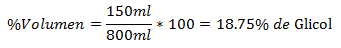
5.- Campuran 1500ml total mengandung 10ml Heksana. Persentase Volume adalah: