10 esempi di miscele di gas
Varie / / July 04, 2021
Miscele di sostanze gassose Sono tra i più facili da ottenere, poiché è molto probabile che le sostanze che si trovano in questo stato di aggregazione siano mescolate. Per esempio: Neon, miscela di argon e xeno, insetticida aerosol, aria ed elio.
Praticamente tutti i gas possono essere combinati illimitatamente, ovviamente condizionati da alcuni chimiche, fisiche e fondamentalmente legate agli aspetti di sicurezza dell'utente che manipola. Come i diversi tipi di miscele che si stabiliscono tra le sostanze, le miscele di gas hanno anche proprietà che sono uniche per loro.
Lo studio di miscele frizzanti è di solito utile quanto quella dei gas allo stato puro: la stessa conoscenza dell'aria che è presente in l'atmosfera sarebbe impossibile se non fosse per la conoscenza delle proporzioni e dei comportamenti dei gas misti.
In questo modo, è essenziale conoscerne un po' Caratteristiche di miscele di gas, come la proprietà della pressione parziale (quella esercitata da ciascuno dei gas all'interno del miscela) e quello della frazione molare (rapporto tra il numero di moli di un componente gassoso con quello della miscela totale bibita). Le moli esprimono la quantità di gas nella miscela.
Il La legge di Dalton afferma che la pressione totale di una miscela di gas è uguale alla somma delle pressioni parziali di ciascuna uno dei singoli gas che vi partecipano (questo è soggetto al fatto che i gas non reagiscano tra Sì). La pressione parziale è qui intesa come quella che eserciterebbe ciascuno dei gas se si trovasse solo nello stesso recipiente e nelle stesse condizioni di temperatura. R) Sì:
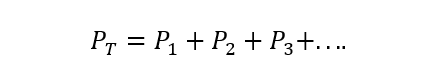
Dove PT è la pressione totale e P1, P2 E p3 sono le pressioni parziali degli ipotetici gas 1, 2 e 3 nella miscela di gas.
Utilizzando la legge di Dalton, è stata sviluppata un'espressione per calcolare il pressione parziale di un gas in una miscela gassosa se conosciamo la sua pressione totale e la sua frazione molare.
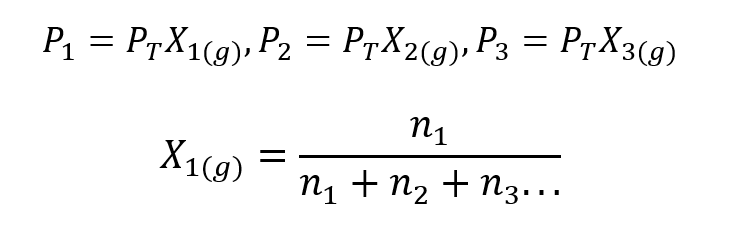
Dove X1, X2 sì X3 sono le frazioni molari dei gas ipotetici 1, 2 e 3 nella miscela di gas, e n1, n2 sì n3 sono le quantità di sostanza di ciascuno di questi gas nella stessa miscela.
Uno di proprietà principali dei componenti nelle miscele è la concentrazione, che può essere espressa in diverse unità. Nel caso delle miscele di gas, la concentrazione dei suoi componenti può essere espressa in ppm (parti per milione), unità riferita al suo volume. Cioè, una certa quantità di ppm di un componente in una miscela di gas è il rapporto tra il volume di quella certa quantità e il volume di ogni milione di unità di miscela.
È importante notare che ppm di un gas dipendono dalla temperatura e dalla pressione del gas. Per questo motivo, per calcolare i ppm di un gas, vengono solitamente utilizzate condizioni normali di pressione e temperatura. (CNPT), che danno uno stato normale a 0 gradi Celsius di temperatura e 1013 ettopascal (1 bar) di Pressione. Se queste condizioni non vengono utilizzate, è necessario specificare quali verranno utilizzate.
Ti può servire:
Esempi di miscele di gas
Il seguente elenco contiene miscele di gas, specificando gli elementi che compaiono nella miscela:
- Aria (miscela di 21% di ossigeno e 79% di azoto, più altri gas in piccole proporzioni)
- Cronigón (miscela di 99% di argon e 1% di ossigeno)
- Trimix (miscela di ossigeno, azoto ed elio)
- Mix di neon, argon e xeno
- Miscela di 85% metano, 9% etano, 4% propano e 2% butano.
- Esafluoruro di zolfo e aria
- Insetticida aerosol
- Aria ed elio
- Nitrox (miscela d'aria, arricchita in ossigeno e azoto)
Segui con:
