50 Esempi di soluzioni
Varie / / July 04, 2021
Il soluzioni sono uno dei tipi di miscele che esistono. I componenti che compongono una soluzione non reagiscono chimicamente, sebbene le proprietà fisiche di questi componenti possano essere modificate quando diventano parte della soluzione. Per esempio: fumo, amalgama, caffè con latte.
Perché una miscela sia una soluzione, deve essere must omogeneo sì uniforme, vale a dire che i componenti misti non sono distinguibili ad occhio nudo e che, inoltre, la proporzione tra il soluto (sostanza che compare in quantità minore) e il solvente (sostanza che compare in maggiore quantità) rimane pressoché invariata qualunque sia il volume prelevato dalla soluzione. La proporzione del soluto nella soluzione o nel solvente è quella che viene chiamata "concentrazione" e solitamente la stessa soluzione può essere preparata utilizzando varie concentrazioni di soluto.
Si possono formare soluzioni tra sostanze che, prima di essere miscelate, si trovano in una delle diverse stati di aggregazione. Esistono soluzioni praticamente in tutti gli stati di aggregazione. Generalmente lo stato di aggregazione della soluzione è determinato dallo stato di aggregazione del solvente. Per esempio:
È comune per presenza di molecole di soluto all'interno di un solvente alterano le proprietà del solvente stesso. Ad esempio, i punti di fusione e di ebollizione di due composti cambiano quando questi composti vengono miscelati, così come la loro composizione. densità e colori.
Lo scienziato francese Roult studiato questo comportamento dei componenti nelle soluzioni e proposto anche la sua legge principale (legge di Roult), che afferma che la pressione di vapore parziale di ciascun componente nella miscela di vapore che circonda una soluzione ideale a partire dal liquidi è uguale alla pressione parziale di ciascun componente puro moltiplicato per la sua frazione molare nella soluzione. Una soluzione ideale è considerata una soluzione in cui le specie chimiche sono molto simili, quindi non viene considerata alcuna variazione nell'energia delle interazioni tra di esse. L'equazione fondamentale della legge di Roult è:
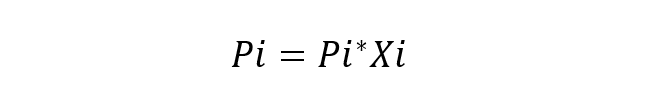
Dove:
- Pi è la pressione parziale del componente io nella miscela gassosa che circonda la soluzione.
- Pi* è la pressione del componente io
- Xi è la frazione molare del componente io in dissoluzione.
Ovviamente, le persone sono costantemente in contatto con le soluzioni. Il aria è una dissoluzione di elementi in stato gassoso: la sua composizione maggioritaria è data dal azoto (78%) e il resto è occupato dal 21% di ossigeno e l'1% di altri componenti, sebbene queste proporzioni possano variare leggermente.
Esempi di soluzioni
L'elenco che segue comprende quaranta esempi di soluzioni, evidenziando lo stato di aggregazione in cui si trova ciascuna, un soluto in un rispettivo solvente.
- Aria (gas nel gas). Una composizione di gas, dove l'azoto è il più abbondante.
- Fumo (solido nel gas). L'aria è viziata dalla comparsa di fumo dal fuoco. È una soluzione in cui l'aria funge da solvente.
- Leghe tra metalli (solido in solido). Il duralluminio è una lega composta da alluminio, rame, manganese, magnesio e silicio.
- Polvere d'aria atmosferica (solido nel gas). La presenza di solidi (decomposti quasi a unità indivisibile ma infine solidi) nel gas è un esempio di dissoluzione in questo senso.
- Acciaio (solido in solido). Lega tra ferro e carbonio, con una proporzione molto più elevata del primo.
- Bevande gassate (gas in liquido). Le bevande gassate hanno una dissoluzione dei gas in un liquido.
- Amalgama (liquido in solido). Sono leghe di mercurio disciolte in certi metalli come oro o argento.
- Petrolio raffinato (liquido in liquido). La combinazione degli elementi che lo compongono (la maggioranza è carbonio) dà luogo ad una dissoluzione tra liquidi.
- Butano in aria (gas nel gas). Il butano è un composto chimico gassoso che può essere stoccato in tubi, pronto per essere utilizzato come combustibile.
- Ossigeno nell'acqua dell'oceano (gas in liquido). L'ossigenazione dell'acqua di mare permette lo sviluppo della vita acquatica.
- Bevande con una gradazione alcolica (liquido in liquido). Sono molto consumati dagli umani durante le celebrazioni. Solitamente sono soluzioni di etanolo e succhi di frutta in concentrazioni controllate del alcol.
- Caffèlatte (liquido in liquido). Un liquido con un contenuto più elevato riceve un po' da un altro, che rappresenta una trasformazione del suo colore e sapore.
- Smog (gas in gas). L'introduzione di gas non tipici dell'atmosfera induce una trasformazione dell'aria, che ha effetti negativi sulle società che lo respirano: più è concentrato, più sarà dannoso.
- Sale in acqua (solido in liquido). Ampiamente usato per cucinare.
- Sangue (liquido in liquido). Il componente maggioritario è il plasma (liquido) e al suo interno compaiono altri elementi, tra i quali spiccano i globuli rossi.
- ammoniaca in acqua (liquido in liquido). Questa soluzione (che può anche essere trasformata da gas a liquido) è funzionale a molti prodotti per la pulizia.
- Aria con tracce di umidità (liquido in gas). Il vapore acqueo è presente nell'aria a causa dell'aumento temperatura.
- Succhi in polvere (solido in liquido). La polvere si dissolve in acqua e produce una soluzione del colore del succo in polvere.
- Idrogeno in palladio (gas solido). L'idrogeno si dissolve molto bene in alcuni metalli.
- Virus nell'aria (solido nel gas). Come la polvere atmosferica, sono unità molto piccole di un solido trasportate da un gas.
- Mercurio in argento (liquido in solido). È uno dei cosiddetti “amalgami”.
- Il tè (solido in liquido). Un solido di dimensioni molto ridotte (i graniti dell'involucro) si dissolve nell'acqua.
- Acqua reale (liquido in liquido). È una composizione di acidi che permette di dissolvere diversi metalli, tra cui compare l'oro.
- Bronzo (solido in solido). È la lega tra rame e stagno.
- Limonata (liquido in liquido. Sebbene molte volte la miscela sia tra un solido e un liquido, in realtà è un liquido presente in quel solido, come il succo di limone.
- Perossido (liquido in liquido). È una soluzione di acqua ossigenata (H2O2) in acqua. È usato per disinfettare le ferite e nell'industria cosmetica.
- Ottone (solido in solido). È la lega tra il rame solido e lo zinco.
- Raffreddamento con ghiaccio (solido in liquido). Il ghiaccio entra nel liquido e lo raffredda, dissolvendosi. Se viene introdotto in acqua, è il caso particolare in cui è la stessa sostanza.
- Soluzione fisiologica (liquido in liquido). L'acqua agisce come un solvente e molte sostanze liquide agiscono come un soluto.
- Frullati (solidi nei liquidi). Attraverso un processo di macinazione, viene indotta una combinazione di solidi a liquidi.
Segui con:
