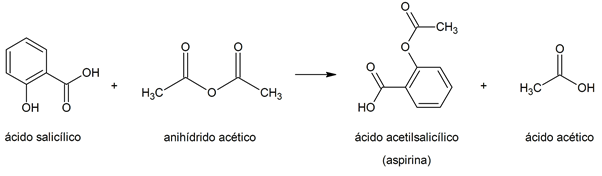20 esempi di reazioni chimiche
Varie / / July 04, 2021
È chiamato reazione chimica al processo mediante il quale uno o più sostanze chimiche (detti "reagenti") si trasformano e danno origine ad altri (detti "prodotti"). Pertanto, affinché i reagenti generino prodotti attraverso una reazione chimica, un riarrangiamento di atomi sì molecole in cui avviene uno scambio di energia. Per esempio: combustione, ossidazione, reazioni acido-base.
Il composti chimici avere energia chimica nei legami tra gli atomi che li compongono. Le reazioni chimiche sono solitamente espresse tramite equazioni, dove i reagenti sono indicati a sinistra e i prodotti a destra, collegando entrambe le parti con una freccia destra se la reazione è reversibile o una freccia avanti e indietro se si tratta di una reazione reversibile.
Quando si indicano le quantità o le proporzioni in cui reagiscono i reagenti e si ottengono i prodotti, si parla di reazioni stechiometriche.
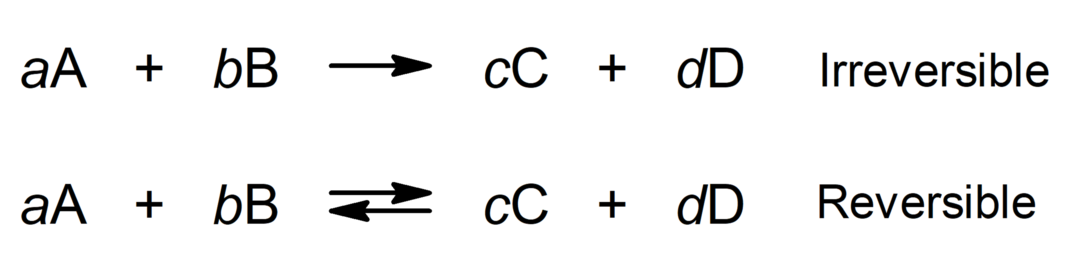
Dove:
- A e B sono i reagenti.
- C e D sono i prodotti.
- a, b, c, d sono i coefficienti stechiometrici (numero di molecole o atomi di un certo tipo che partecipano a un'equazione chimica).
Reazioni chimiche può essere classificato a seconda del tipo di energia che rilasciano o assorbono. In questo senso possono essere esotermici o endotermici (se rilasciano o assorbono caldo), esoluminose o endoluminose (se rilasciano o assorbono luce), esoelettriche o endoelettriche (se producono o necessitano elettricità).
Le leggi delle reazioni chimiche
Nelle reazioni chimiche le leggi sono soddisfatte. Il più importante è il legge di conservazione della massa o legge di Lavoisier, formulata da questo chimico nel 1774, la quale postula che in ogni reazione chimica la massa dei reagenti sia uguale alla massa dei prodotti.
Era Dalton che alcuni anni dopo completò la spiegazione di questa legge, indicando che in una reazione chimica il numero di gli atomi non variano quando si confrontano i reagenti con i prodotti, cambia solo la loro organizzazione, quindi la massa di se conserva.
Un altro parametro importante nelle reazioni chimiche è il loro velocità di reazione poiché non tutti impiegano lo stesso tempo per produrre. La velocità di reazione è definita come la quantità di prodotto che appare per unità di tempo o la quantità di reagente che scompare per unità di tempo.
Sebbene ogni reazione abbia una velocità diversa, alcuni fattori possono farla tendere ad aumentare o diminuzione: la superficie di contatto tra le particelle reagenti e la temperatura sono alcune delle essi.
Il catalizzatori Sono sostanze che aumentano la velocità di una reazione, senza modificarne la struttura. Spesso questo ruolo è svolto da alcuni metalli.
Esempi di reazioni chimiche
Le reazioni chimiche si verificano continuamente in natura, nel corpo umano, nelle fabbriche, negli impianti di trattamento degli effluenti, ecc. Alcuni esempi sono:
-
Combustione
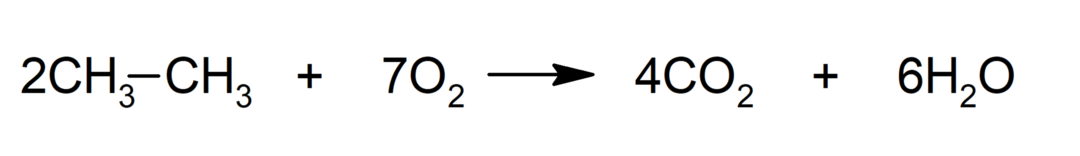
-
Sostituzione
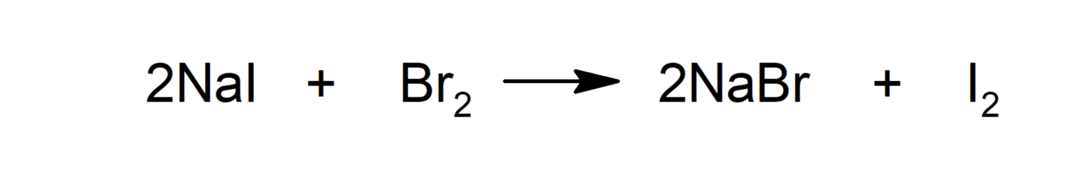
-
aggiunta
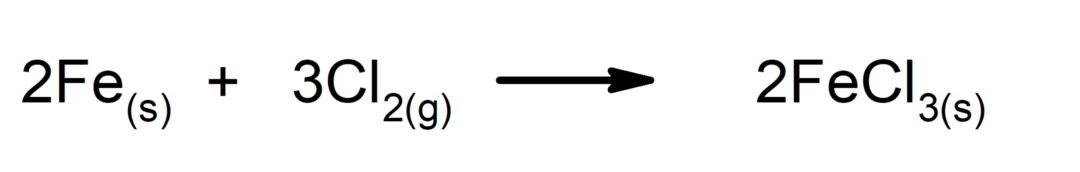
-
Eliminazione
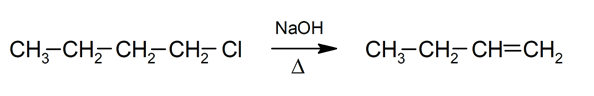
-
Ossidazione
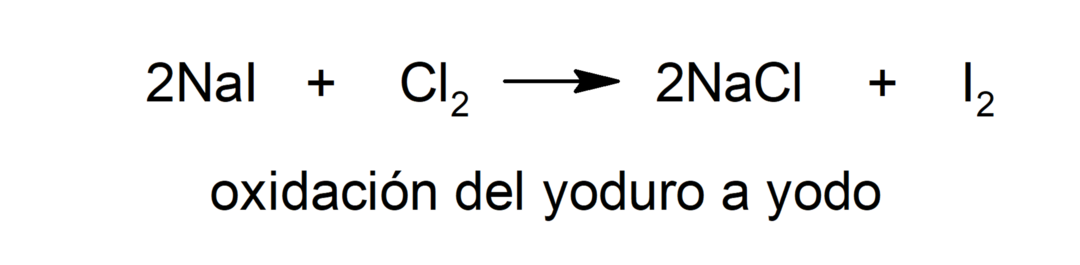
-
Riduzione
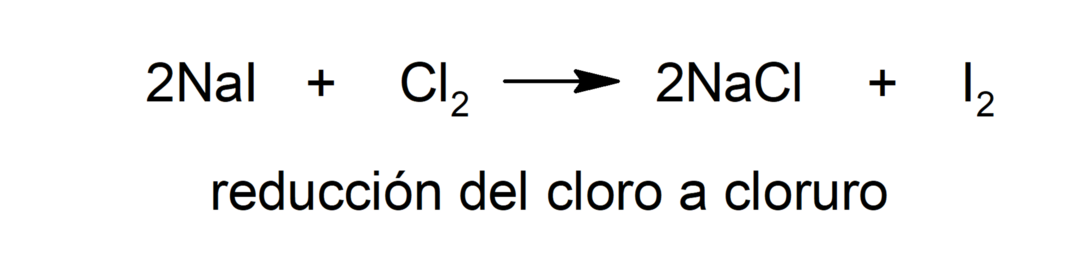
-
Reazioni acido-base
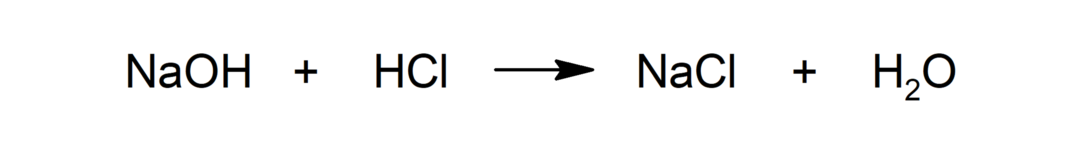
-
Ossigenazione
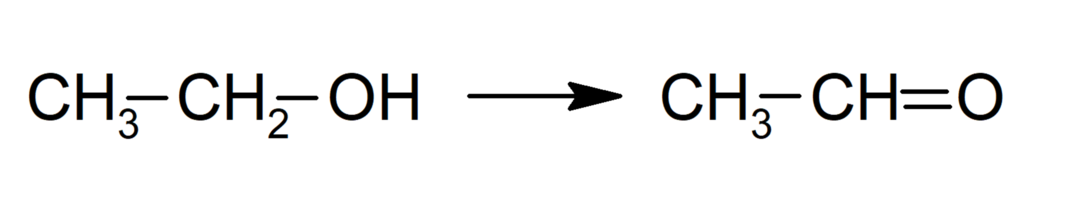
-
Transaminazione

-
Clorazione
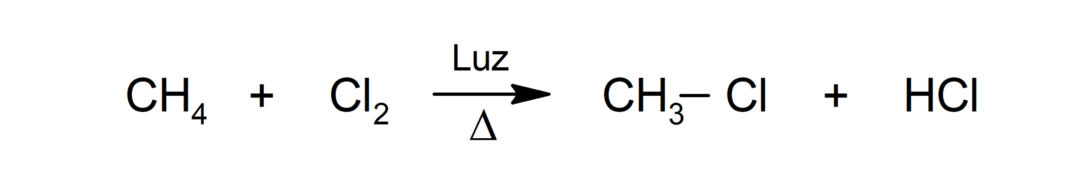
-
carbonilazione

-
Nitrosilazione. È una reazione in cui un gruppo nitrosile è attaccato a una proteina, dopo che è stata sintetizzata dai ribosomi.

-
perossidazione
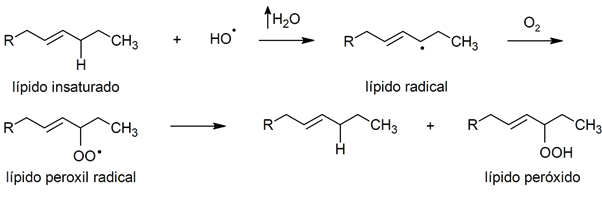
-
Fotolisi dell'acqua
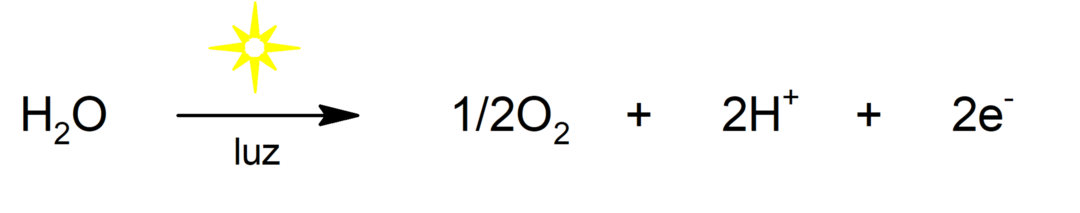
-
solfatazione
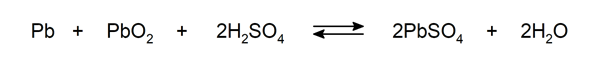
-
carbonatazione
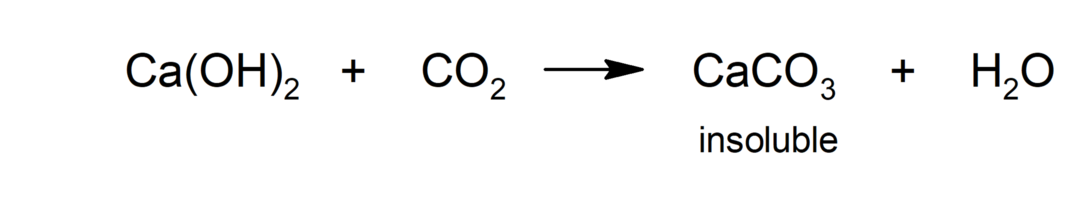
- Ozonizzazione. È una reazione alternativa alla clorazione per decontaminare l'acqua.
-
esterificazione
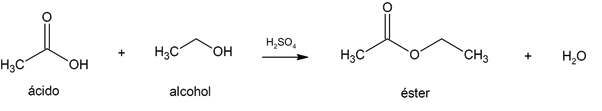
-
Idrogenazione degli alcheni
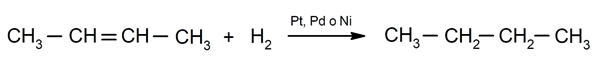
-
acetilazione