20 esempi di legami covalenti
Varie / / July 04, 2021
un sacco di composti chimici sono costituiti da molecole che, a loro volta, sono composti da atomi. Per formare molecole, gli atomi si uniscono formando collegamenti chimici.
I legami chimici non sono tutti uguali: dipendono fondamentalmente dalle caratteristiche elettroniche degli atomi coinvolti, dai loro valori di elettronegatività, tra gli altri fattori. I tipi più comuni di collegamento sono: legami ionici e il legami covalenti.
Si formano legami covalenti tra atomi non metallici dello stesso elemento chimico, tra atomi non metallici di elementi diversi con una differenza di elettronegatività minore o uguale a 1,7 e tra un metalloide e idrogeno. Per esempio: dicloro, ossigeno molecolare, acqua.
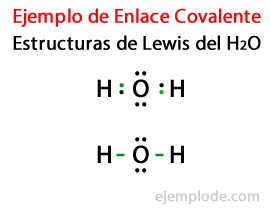
Il legame covalente si forma quando due di questi atomi condividono gli elettroni del loro ultimo livello energetico per soddisfare il Regola dell'ottetto, che stabilisce che gli ioni dei diversi elementi chimici presenti nella Tavola periodica tendono a completare i loro ultimi livelli energetici con 8 elettroni, in modo che le molecole possano acquisire una stabilità simile a quella del
gas nobili.Pertanto, il modo in cui queste sostanze o composti chimici raggiungono la stabilità è condividendo una coppia di elettroni (uno per ciascun atomo). In questo modo la coppia di elettroni condivisa è comune ai due atomi e allo stesso tempo li tiene insieme.
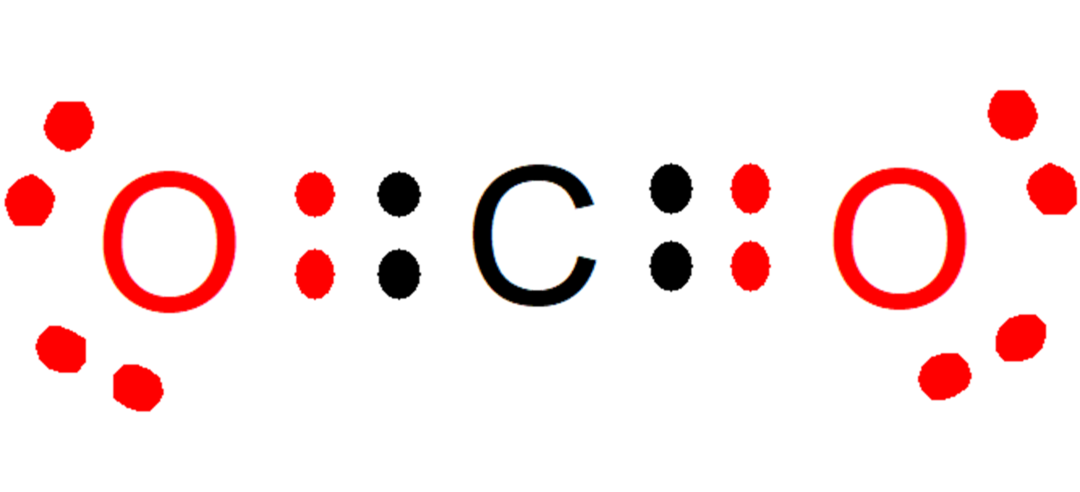
Ad esempio, in anidride carbonica (CO2), ogni ossigeno contribuisce con due elettroni (colore rosso) al legame con il carbonio, mentre il carbonio contribuisce con due elettroni (colore nero) a ciascun legame con ciascun ossigeno. Nel composto formato rimangono 8 elettroni su ogni atomo, e così la Regola dell'Ottetto è soddisfatta.
Tipi di link
Ci sono fondamentalmente tre tipi di legami covalenti, sebbene sia importante chiarire che nessun legame è assolutamente covalente o assolutamente ionico. Tutti i legami hanno una certa percentuale di covalente e ionico, infatti, il legame ionico è talvolta considerato come una "sovrastima" del legame covalente. In questo senso, possono verificarsi i seguenti tipi di legame covalente:
Sostanze composte da molecole covalenti
Il sostanze che contengono molecole covalenti può verificarsi in qualsiasi stato della materia (solido, liquido o gassoso) e, in generale, sono cattivi conduttori di caldo e del elettricità.
Esistono sostanze covalenti molecolari e sostanze covalenti reticolari. Il covalenti molecolari hanno basso punto di ebollizione e di fusione, sono solubili in solventi non polari (come il benzene o il tetracloruro di carbonio) e sono morbidi allo stato solido. Il covalenti reticolari Formano reticoli cristallini, quindi hanno punti di fusione e di ebollizione più elevati e sono solidi duri e insolubili.
Esempi di legami covalenti
Si possono fornire numerosi esempi di composti o sostanze contenenti legami covalenti:
- difluoro
- Dibromo
- dicloro
- fai da te
- Ossigeno molecolare
- acqua
- Ammoniaca
- Diossido di carbonio
- Metano
- Propano
- Glucosio
- Azoto molecolare
- Quarzo
- Paraffina
- diesel

Segui con: