30 esempi di aldeidi
Esempi / / November 06, 2023
IL aldeidi Sono composti organici che sono formati da una catena di carbonio a cui è attaccato un gruppo carbonilico terminale (= C = O) (situato a un'estremità della molecola), che a sua volta è legato ad un atomo di idrogeno.
Le aldeidi molto comuni sono il metanale (formaldeide), l'etanale (acetaldeide) e il propanale (propaldeide).

Alcuni di questi composti sono presenti in natura, ad esempio la vanillina o vanillina è un'aldeide naturale che costituisce l'aroma principale della vaniglia.
- Vedi anche: Aldeidi e chetoni
Nomenclatura delle aldeidi
Le aldeidi possono essere denominate utilizzando le regole di nomenclatura stabilite dall'Unione Internazionale di Chimica Pura e Applicata (IUPAC).
Per denominare un'aldeide si utilizzano prefissi che indicano il numero di atomi di carbonio che la catena del carbonio ha attaccato al gruppo carbonilico. Il gruppo carbonilico si trova sempre ad un'estremità della catena del carbonio, il che significa che avrà sempre la posizione uno e non è necessario indicare la sua posizione nella catena. Inoltre, il suffisso -al è posto alla fine del nome dell'aldeide. Alcuni esempi sono:
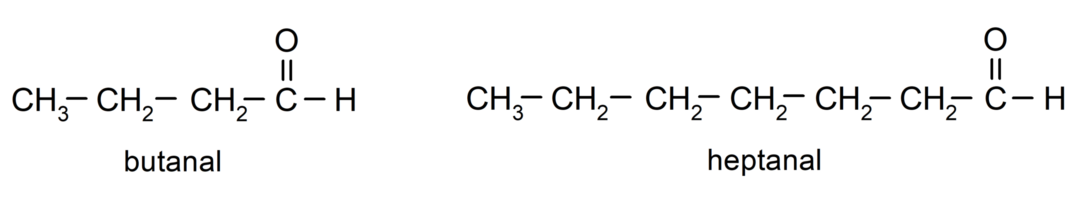
Se l'aldeide è ramificata, cioè è composta da più catene di carbonio, la catena principale come catena che ha il maggior numero di atomi di carbonio e che contiene anche il gruppo carbonile. Il resto delle catene sono denominate gruppi sostituenti.
Inoltre, ciascun gruppo sostituente deve essere scelto in modo che la sua posizione occupi la numerazione più bassa possibile nella catena principale del carbonio. D'altra parte, gli atomi di carbonio della catena principale iniziano a essere contati dall'estremità che contiene il gruppo carbonilico. Alcuni esempi sono:
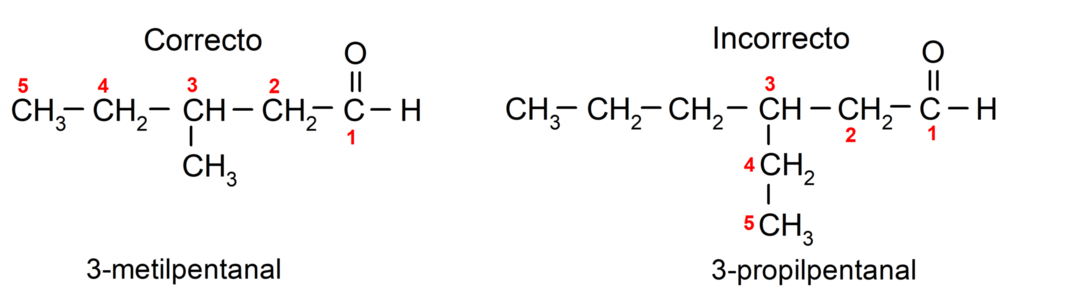
Se l'aldeide agisce come sostituente nella molecola, perché anch'essa è costituita da gruppi funzionali con priorità più alta, come acidi ed esteri, il gruppo aldeidico viene chiamato come -osso. Per esempio:

Se un'aldeide ha più gruppi carbonilici, viene denominata utilizzando prefissi che indicano il numero di questi gruppi, dial (due gruppi carbonilici), trial (tre gruppi carbonilici), ecc. Per esempio:
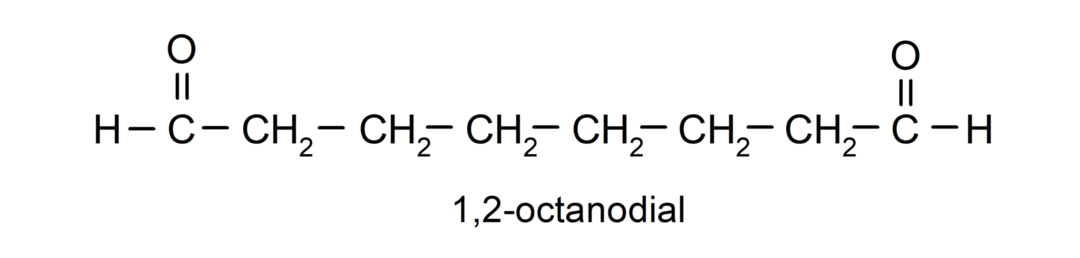
Quando il gruppo carbonilico è legato ad un ciclo, le aldeidi vengono denominate utilizzando il termine carbaldeide. Per esempio:

Proprietà fisiche delle aldeidi
Le aldeidi solitamente presentano qualche variazione della stessa proprietà fisica. Ciò si verifica perché le proprietà fisiche delle aldeidi dipendono da come si forma la catena di carbonio attaccata al gruppo carbonilico.
Alcune proprietà fisiche delle aldeidi sono:
- Solubilità. La solubilità in acqua delle aldeidi dipende dalla quantità di atomi che ha la catena del carbonio. Le aldeidi con catene di carbonio più corte (fino a circa cinque atomi di carbonio) sono solubili in acqua. Le aldeidi con catene di carbonio costituite da molti atomi di carbonio non sono solubili in acqua. Il metanale e l'etanale sono molto solubili in acqua.
- Densità. In generale, le aldeidi sono composti meno densi dell'acqua.
- Stati di aggregazione. Le aldeidi sono costituite da uno e due atomi di carbonio gas, sono quelli contenenti da tre a dodici atomi di carbonio liquidi, e quelli costituiti da più di dodici atomi di carbonio sono solidi.
- Odore. Alcune aldeidi hanno odori irritanti, mentre altre hanno odori gradevoli.
- Polarità. Il gruppo carbonilico conferisce loro la polarità.
- Punto di ebollizione. Hanno punti di ebollizione più elevati rispetto agli alcani di peso molecolare simile e hanno punti di ebollizione inferiori rispetto agli acidi carbossilici e agli alcoli di peso molecolare comparabile.
Proprietà chimiche delle aldeidi
Alcune delle proprietà chimiche delle aldeidi sono:
Le aldeidi vengono ossidate quando reagiscono con i reagenti di Tollens, Benedict e Fehling. per formare il corrispondente acido carbossilico. L'acido formato avrà nella catena del carbonio lo stesso numero di atomi di carbonio dell'aldeide da cui si è formato. Per esempio:
- Ossidazione con reagente di Tollens (complesso argento ammoniacale in soluzione basica, [Ag (NH3)2]+). Questa reazione produce l'acido corrispondente e l'argento metallico.

- Ossidazione con il reagente Benedict e Fehling (soluzioni alcaline di solfato di rame (II) (CuSO4) con composizioni diverse). Questa reazione produce il corrispondente acido e ossido rameoso (Cu2O).

Subiscono reazioni di addizione nucleofila, dove i nucleofili vengono aggiunti al gruppo carbonilico delle aldeidi. Alcuni esempi sono:
- reazioni di addizione alcoli al gruppo carbonilico delle aldeidi per formare acetali ed emiacetali.
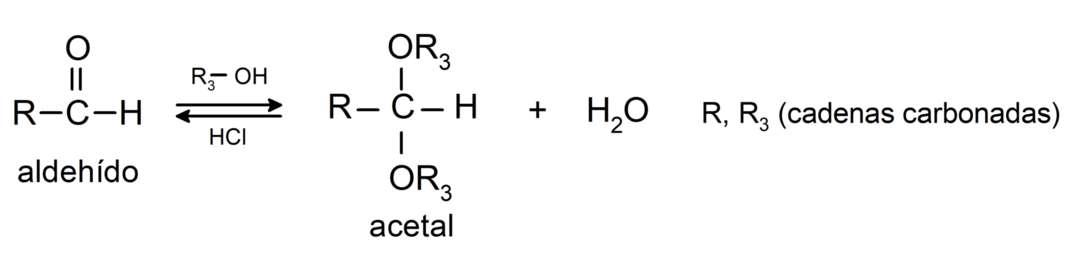
- reazioni di addizione ammine primario al gruppo carbonilico.

- Reazioni di addizione dell'acido cianidrico (HCN), dove si formano cianoidrine o cianoidrine.

Subiscono reazioni di condensazione aldolica. In questo tipo di reazione, due aldeidi si condensano per formare un aldolico. Sono reazioni che avvengono con l'idrossido di sodio (NaOH). Per esempio:
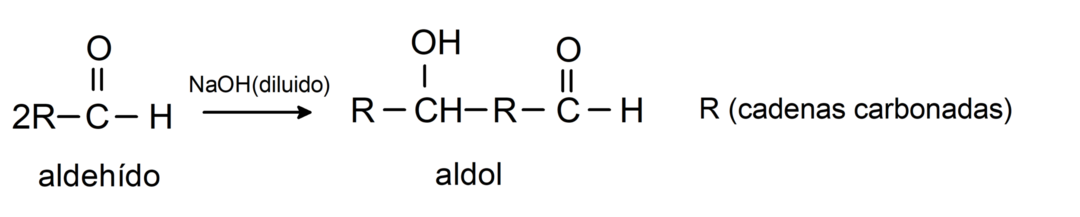
Subiscono reazioni di riduzione agli alcoli primari. In presenza di boroidruro di sodio (NaBH4) e idruro di litio alluminio (LiAlH4) o mediante idrogenazione catalitica, vengono ridotti ad alcoli primari. Per esempio:
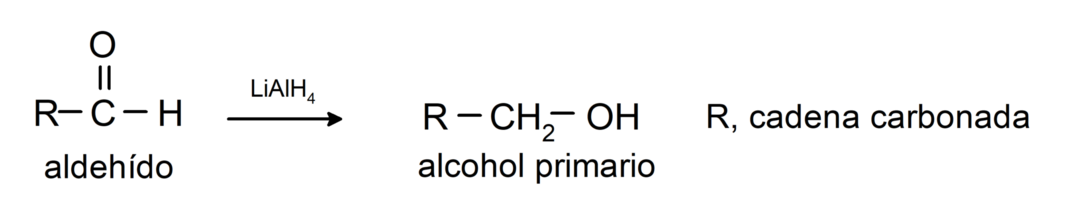
Esempi di aldeidi
- metanale (formaldeide)
- etanale (acetaldeide)
- propanale (propaldeide)
- butanale
- pentanale
- vanillina
- cinnamaldeide
- propenale
- benzaldeide
- esanale
- 3-bromociclopentanocarbaldeide
- cicloesanocarbaldeide
- 4,4-dimetilpentanale
- 2-idrossi-butanale
- 2-idrossi-2-metil-butanale
- 2,3-dimetilpentanale
- pentanediale
- ciclopentanocarbaldeide
- isobutanale
- 2-cloro-butanale

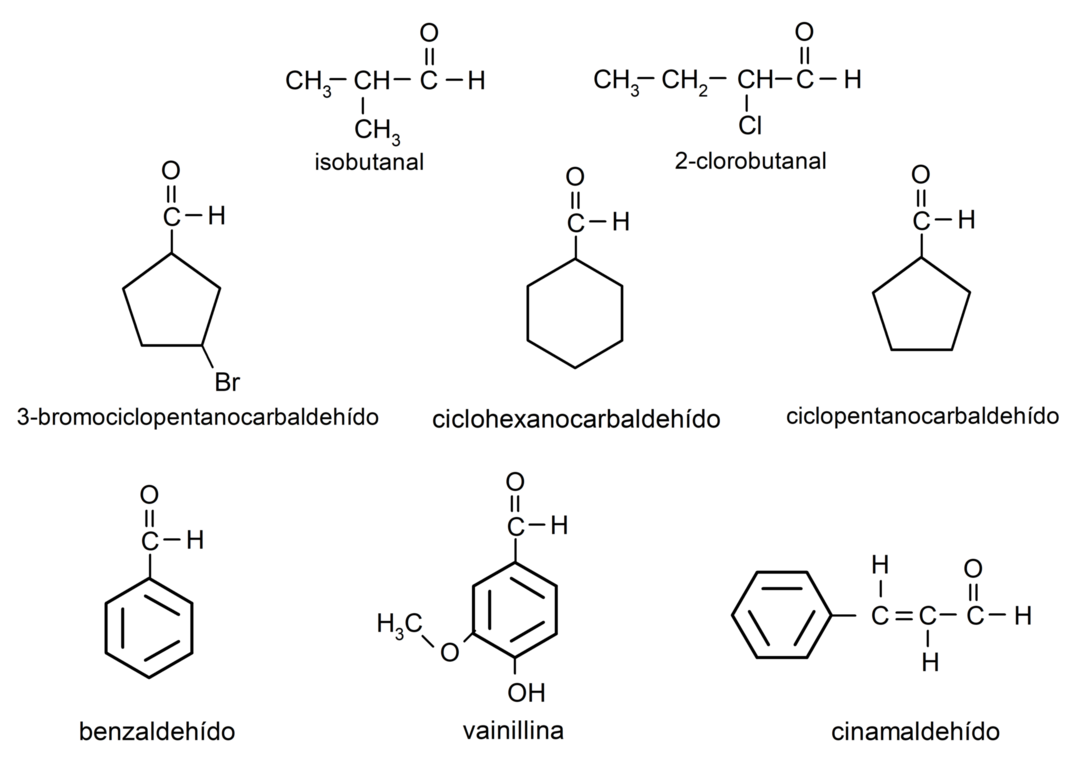
Aldeidi in natura
Alcune aldeidi presenti in natura sono:
- Benzaldeide, un componente delle mandorle.
- Cinnamaldeide, il componente che conferisce il suo odore all'essenza di cannella.
- Vanillina, il componente che conferisce alla vaniglia il suo sapore.
D'altra parte, una delle forme di glucosio, la forma aperta, ha un gruppo funzionale aldeidico.
Si ritiene che l'acetaldeide, che si forma come intermedio nella metabolizzazione dell'alcol, causi sintomi di postumi di una sbornia quando intossicati dall'alcol.
Usi delle aldeidi
Alcuni degli usi principali delle aldeidi sono:
- Vengono utilizzati nella produzione di solventi, vernici, prodotti cosmetici ed essenze.
- Sono utilizzati nella produzione di resine. La bachelite è realizzata con formaldeide ed è una resina che funziona molto bene come isolante elettrico.
- Sono stati usati come sedativi. La paraldeide è stata utilizzata come sedativo e ipnotico, anche se ora è fuori uso a causa del suo odore sgradevole.
- Sono usati come conservanti per campioni biologici e cadaveri. La formaldeide è ampiamente utilizzata in questo senso.
- Sono usati come aromi alimentari. Un esempio è la vanillina, che viene utilizzata per conferire ai dolci un aroma di vaniglia.
- Sono usati come agenti disinfettanti.
Pericoli delle aldeidi
Diverse aldeidi sono state considerate cancerogene, ad esempio la formaldeide è stata dichiarata un composto cancerogeno secondo l'OMS (Organizzazione Mondiale della Sanità).
L'esposizione e il contatto con molte aldeidi provoca irritazione alla pelle, agli occhi e alle vie respiratorie. D’altro canto provoca dermatiti da contatto e malattie del fegato.
Riferimenti
- Salomone, T.W. Graham e María Cristina Sangines Franchini (1985). “chimica organica" Messico, D.F.: Limusa.
- Whitten, K. W., Gailey, K. D., Davis, R. E., de Sandoval, M. T. A. O., & Muradás, R. M. G. (1992). “Chimica generale" (pagg. 108-117). McGraw-Hill.
- Arteaga, P. M. (2017). “Chetoni e aldeidi” Bollettino scientifico Con-Science della Scuola preparatoria n. 3, 4(8).
Segui con:
- Zuccheri
- Idracidi
- Alcol etilico
- Composti organici ed inorganici
