30 esempi di vendite binarie
Esempi / / November 09, 2023
IL sali binari (sali neutri) si formano quando un metallo e un non metallo si combinano. Sono composti chimici composto da soli due elementi chimici. Per esempio: cloruro di sodio (NaCl) e bromuro di potassio (KBr).
- Guarda anche: Metalli e non metalli
Esempi di sali binari
- Cloruro di sodio (NaCl)
- Cloruro di ferro (II) (FeCl2)
- Cloruro di ferro (III) (FeCl3)
- Solfuro di cobalto(II) (CoS)
- Solfuro di cobalto (III) (Co2SÌ3)
- Solfuro di piombo(II) (PbS)
- Solfuro di piombo (IV) (PbS2)
- Cloruro di calcio (CaCl2)
- Fluoruro di sodio (NaF)
- Cloruro di litio (LiCl)
- Cloruro di stronzio (SrCl2)
- Cloruro di bario (BaCl2)
- Cloruro di alluminio (AlCl3)
- Solfuro di magnesio (MgS)
- Cloruro di rubidio (RbCl)
- Bromuro di calcio (CaBr2)
- Solfuro di potassio (K2S)
- Bromuro di magnesio (MgBr2)
- Solfuro di zinco (Zn2S)
- Bromuro di litio (LiBr)
- Cloruro di nichel (NiCl2)
- Cloruro di uranio(III) (UCl3)
- Bromuro d'argento (AgBr)
- Ioduro d'argento (AgI)
- Bromuro di potassio (KBr)
Nomenclatura dei sali binari
Secondo la nomenclatura tradizionale, i sali binari vengono nominati scrivendo il nome dell'elemento non metallico con la desinenza -ide. Il nome dell'elemento metallico, invece, si scrive in base al suo stato di ossidazione:
- Per lo stato di ossidazione più basso si scrive con la desinenza -oso. Per esempio: cloruro ferroso (FeCl2), dove il ferro ha uno stato di ossidazione pari a 2+.
- Per lo stato di ossidazione più elevato si scrive con la desinenza -ico. Per esempio: cloruro ferrico (FeCl3), dove il ferro ha uno stato di ossidazione pari a 3+.
Secondo la Nomenclatura Sistematica i sali binari si chiamano scrivendo il nome dell’elemento non metallico con un prefisso che indica la quantità di atomi di questo elemento nel composto. Inoltre, nel nome dell'elemento non metallico viene inserita la desinenza -uro. Quindi viene inserito il nome dell'elemento metallico. Per esempio: cloruro di magnesio (MgCl2) e tricloruro di ferro (FeCl3).
Secondo la nomenclatura di Stock, i sali binari vengono denominati scrivendo il nome dell'elemento non metallico con la desinenza -ide. Successivamente viene posto il nome dell'elemento metallico seguito dal suo stato di ossidazione scritto in numeri romani e tra parentesi. Per esempio: cloruro di ferro (II) (FeCl2) e solfuro di cobalto (III) (Co2SÌ3).
Applicazioni dei sali binari
- Sono utilizzati come refrigeranti nell'industria alimentare e farmaceutica. Per esempio: cloruro di calcio (CaCl2).
- Sono usati per trattare le superfici metalliche contro la corrosione. Per esempio: fluoruro di sodio (NaF).
- Sono utilizzati per regolare l'umidità nell'industria della carta e dell'edilizia. Per esempio: cloruro di calcio (CaCl2).
- Vengono utilizzati nell'industria del vetro per eliminare le impurità. Per esempio: tetracloruro di silicio (SiCl4).
- Sono usati come ingredienti da cucina. Per esempio: cloruro di sodio (NaCl).
Proprietà fisiche dei sali binari
- Hanno punti di fusione elevati perché sono costituiti da legami ionici.
- Conducono corrente elettrica quando disciolti o fusi.
- I sali più comuni hanno una bassa durezza.
- Non sono comprimibili.
- La maggior parte può dissolversi in acqua.
Come si ottengono i sali binari?
I sali binari possono essere ottenuti attraverso alcune delle seguenti reazioni chimiche:
Reazione tra un metallo e un non metallo. Per esempio: la reazione tra sodio (Na) e dicloruro (Cl2) produce cloruro di sodio (NaCl).
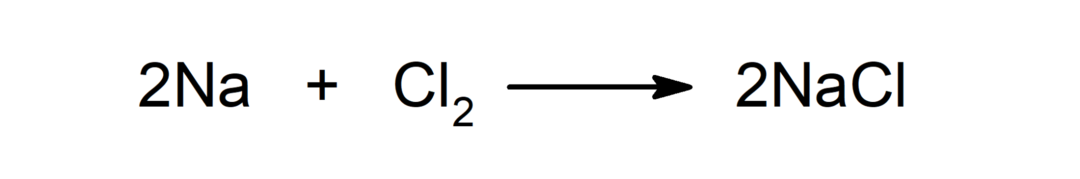
Reazione tra un metallo e un acido. Per esempio: La reazione tra potassio (K) e acido cloridrico (HCl) produce cloruro di potassio (KCl) e diidrogeno (H2).
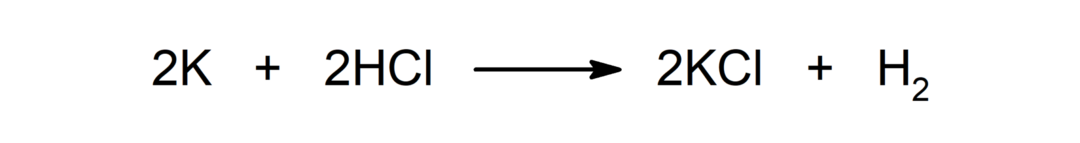
Reazione tra un acido e una base. Per esempio: La reazione tra acido cloridrico (HCl) e idrossido di sodio (NaOH) produce cloruro di sodio (NaCl) e acqua (H2O).
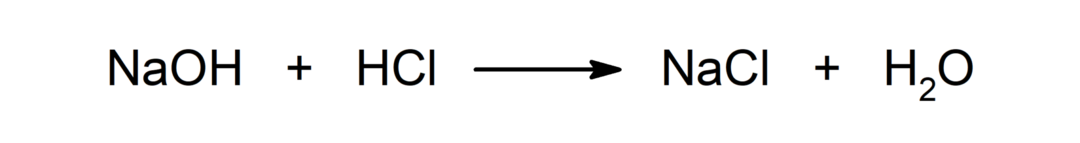
Segui con:
- ossisali
- sali neutri
- sali acidi
Riferimenti
- Cerón Villalba, A., Novoa Ramírez, C. S., & Alpizar Juárez, E. (2020). Video sulla nomenclatura 1: sali binari e reazione chimica.
- Acurio Arias, M. V., & Delgado Méndez, M. E. (2022). Guida all'apprendimento basato sul gioco dei "composti binari" nella chimica delle scuole superiori presso l'Unità Formativa "Herlinda Toral" (Tesi di laurea, Università Nazionale dell'Educazione).
- Cabrera, M. J. H. (2005). Studio dai principi primi delle proprietà elettroniche e strutturali di composti binari e ternari (Tesi di dottorato, Università di La Laguna).



