25 Esempi di alogenuri
Esempi / / November 09, 2023
UN alogenuro o alogenuro è un composto chimico binario composto da a atomo di un alogeno e un elemento o catione che ha un'elettronegatività inferiore a quella dell'alogeno. Per esempio:
- Cloruro di sodio (NaCl)
- Fluoruro di calcio (CaF2)
- Bromuro di potassio (KBr)
- Cloruro di idrogeno (HCl(G))
Gli alogeni lo sono elementi chimici che compongono il gruppo 17 del Tavola periodica. Gli alogeni sono: Fluoro (F), Cloro (Cl), Bromo (Br), Iodio (I), Astato (At), Teneso (Ts).
- Guarda anche: Aldeidi e chetoni
Tipi di alogenuri
A seconda della loro composizione, gli alogenuri possono essere:
- Alogenuri inorganici. Sono composti chimici inorganici che contengono uno o più atomi di un alogeno. Possono essere sali inorganici, alogenuri di idrogeno o complessi metallici. Per esempio: cloruro di sodio (NaCl) e l'anione tetraiodomercurato HgI42-.
- Alogenuri organici. Sono composti chimici organici che contengono uno o più atomi di un alogeno legati a un atomo di carbonio di un composto organico. Per esempio: cloruro di metile (CH3 – Cl) e triclorometano (CH – Cl3).
Esempi di alogenuri
- Cloruro di sodio (NaCl)
- Cloruro di calcio (CaCl2)
- Fluoruro d'argento (AgF)
- Fluoruro di litio (LiF)
- Ioduro di potassio (KI)
- Bromuro di potassio (KBr)
- Cloruro di rame(II) (CuCl2)
- Cloruro di ferro (III) (FeCl3)
- Bromuro di cromo (III) (CrBr3)
- Cloruro di alluminio (AlCl3)
- Cloruro di ammonio ((NH4)Cl)
- Ioduro di piombo(II) (PbI2)
- Ioduro di magnesio (MgI2)
- Fluoruro di berillio (BeF2)
- Fluoruro di alluminio (AlF3)
- Bromometano (CH3 – Br)
- Iodoformio (CHI3)
- Cloruro di metile (CH3 –Cl)
- Bromoetano (CH3 – CH2 – Br)
- Dicloroetano (Cl – CH2 – CH2 –Cl)
- Bromuro d'argento (AgBr)
- Cloruro di stagno (IV) (SnCl4)
- Cloruro di titanio (IV) (TiCl4)
- Cloruro di idrogeno (HCl(G))
- Bromuro di idrogeno (HBr(G))
Proprietà fisiche degli alogenuri
Alcune delle proprietà fisiche degli alogenuri sono:
- Gli alogenuri alchilici (alogenuri organici) hanno densità e punti di ebollizione più elevati rispetto ai loro corrispondenti alcani. Ciò si verifica perché l'atomo di alogeno che ha sostituito un atomo di idrogeno nel idrocarburo da cui proviene l'alogenuro.
- I fluoruri e i cloruri organici sono meno densi dell'acqua, mentre i bromuri e gli ioduri organici sono più densi dell'acqua.
- Gli alogenuri alchilici sono insolubili in acqua e solubili in solventi organici.
- Gli alogenuri di idrogeno sono gas con un odore intenso a temperatura ambiente.
- Gli alogenuri formati con gli atomi degli elementi del gruppo 1 della tavola periodica sono solidi bianchi.
Proprietà chimiche degli alogenuri
- Gli alogenuri alchilici subiscono reazioni di sostituzione nucleofila alifatica. Si tratta di reazioni in cui un atomo nucleofilo (ricco di elettroni) sostituisce un atomo (gruppo uscente) che è attaccato a un atomo elettrofilo (carente di elettroni).
Per esempio: nella reazione del bromuro di metile (CH3 – Br) con idrossido di sodio (NaOH), il bromo (gruppo uscente) è sostituito dallo ione idrossido (nucleofilo) nel bromuro di metile, dove il carbonio è l'elettrofilo.
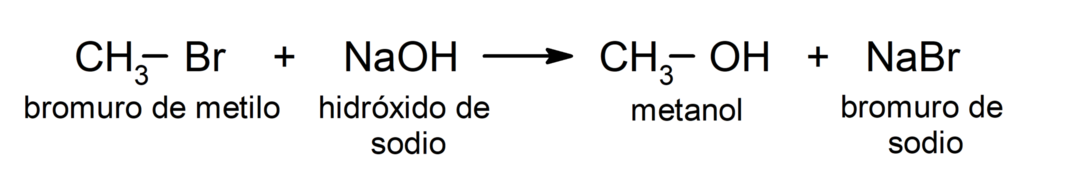
- Alcuni alogenuri alchilici reagiscono con il magnesio in solventi come etere o tetraidrofurano e il prodotto risultante è un composto organometallico chiamato “reagente di Grignard”. Per esempio: bromuro di etile (CH3 – CH2 – Br) con magnesio (Mg) reagisce in un mezzo secco per produrre bromuro di etilmagnesio (CH3 – CH2 – MgBr).

- Gli alogenuri alchilici primari subiscono reazioni con alcossidi o alcoli nel mezzo basico per produrre eteri. Queste reazioni sono conosciute come la “sintesi di Williamsson”. Per esempio: la reazione tra bromuro di metile (CH3Br) e metossido di sodio (CH3ONa) produce dimetil etere (CH3OH3).
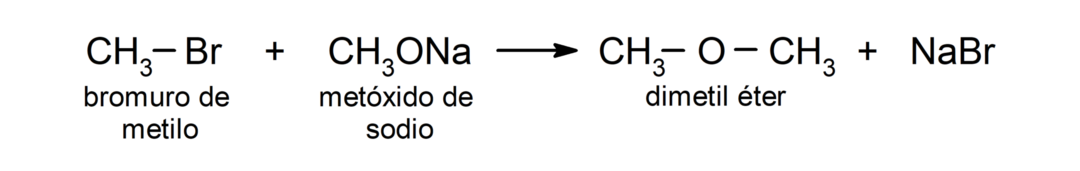
Usi degli alogenuri
Alogenuri o alogenuri hanno varie applicazioni nell'industria, nella medicina e nella vita di tutti i giorni. Alcune di queste applicazioni sono:
- Sono usati come solventi per molti composti organici.
- Sono usati come disinfettanti e antisettici.
- Sono stati usati come refrigeranti.
- Sono utilizzati nella produzione di polimeri fluorurati. Ad esempio, Teflon.
- Sono usati come sali commestibili o tinture in medicina.
- Sono utilizzati nel trattamento e nella purificazione dell'acqua.
- Gli alogenuri metallici sono utilizzati nella produzione di lampade.
- Sono utilizzati nella pulizia dei componenti elettronici.
- Sono usati come prodotti chimici di partenza per sintetizzare composti organici più complessi.
- Alcuni, come il bromuro d'argento (AgBr), vengono utilizzati nello sviluppo di lastre fotografiche.
Pericoli degli alogenuri
Gli alogenuri alchilici utilizzati come solventi reagiscono violentemente con basi forti e forti ossidanti, che possono causare esplosioni e incendi.
Inoltre, i clorofluorocarburi (CFC) sono alogenuri alchilici utilizzati da decenni come refrigeranti, ma la loro L'occupazione è stata vietata dagli enti internazionali perché sono i principali responsabili del buco nello strato di ozono.
D'altra parte, gli alogenuri di idrogeno sono irritanti per gli occhi, la pelle e le mucose.
Segui con:
- Esci
- sali acidi
- sali neutri
Riferimenti
- SALOMONI, T. G. (1996). Fondamenti di Chimica Organica. Wiley.
- Whitten, K. W., Gailey, K. D., Davis, R. E., de Sandoval, M. T. A. O., & Muradás, R. M. G. (1992). Chimica generale (pagg. 108-117). McGraw-Hill.
- Wells, A. F. (1978). Chimica inorganica strutturale. Ripristina.


