Esempio di legame peptidico
Chimica / / July 04, 2021
Il Legame peptidico è quello in cui due molecole di amminoacidi sono unite per condensazione.
Per comprendere meglio i legami peptidici, occorre prima definire gli amminoacidi:
Il Gli amminoacidi sono molecole organiche breve contenente almeno un gruppo amminico (-NH2), di natura alcalina, e un gruppo carbossilico (-COOH), di carattere acido.
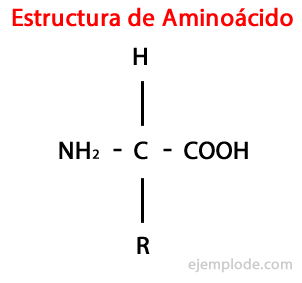
Sebbene gli esseri viventi sintetizzino, per scopi diversi, tipi molto diversi di amminoacidi, i più importanti sono quelli che fanno parte delle proteine, che appartengono tutti alla classe dei α-amminoacidi.
Gli α-amminoacidi sono caratterizzati dall'avere i gruppi acido e amminico attaccati allo stesso atomo di carbonio, chiamato α Carbon. Inoltre questo α-carbonio lega, come terzo sostituente, un atomo di idrogeno e, come quarto sostituente, un gruppo aggiuntivo di dimensioni e caratteristiche diverse, che differenzia ciascun amminoacido da altri.
Il quarto sostituente è chiamato Catena laterale di Aminoacido ed è spesso rappresentato in forma semplificata dalla lettera R.
Poiché i quattro sostituenti dell'α-carbonio sono diversi e adottano una disposizione tetraedrica attorno ad esso, gli α-amminoacidi presenti isomeria ottica, ovvero quando una molecola ha a forma alternativa che sembra un immagine riflessa la sua, che alla fine non è una molecola uguale. A queste due forme isomeriche della molecola vengono assegnate le lettere D o L, a seconda di come i sostituenti sono disposti nello spazio. Tutti gli amminoacidi presenti nelle proteine sono L.
Gli amminoacidi sono classificati in base al loro carattere chimico in Polare e Apolare. I Polari a loro volta si dividono in Neutro e carico (che può essere acido o basico). Il Non polare può essere alifatico o aromatico.
Peptidi e legame peptidico
I peptidi sono il prodotto dell'unione covalente di amminoacidi attraverso legami ammidici, formati da condensazione dell'estremità carbossilica dell'una e dell'estremità amminica dell'altra, rilasciando una molecola d'acqua nella reazione. Questa unione è chiamata Peptide Bond.
Il meccanismo di questa reazione è presentato di seguito, in cui il Gruppi amminici e carbossilici, e la condensazione delle molecole di amminoacidi avviene per formare il peptide.
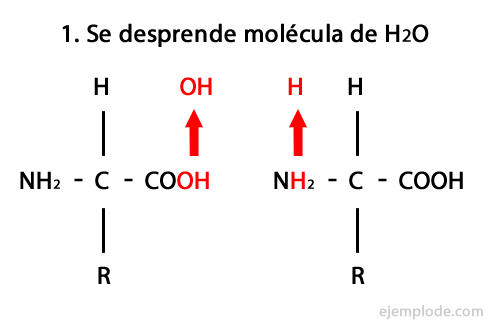
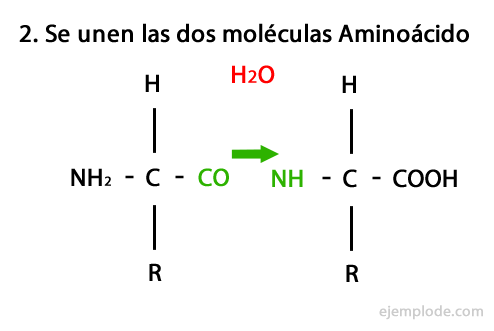

I peptidi, come gli amminoacidi e le proteine, hanno un gruppo amminico e un gruppo carbossilico alle loro estremità senza reagire.
Per specificare la formula di un semplice peptide, e anche di una proteina, basta elencare gli amminoacidi che lo compongono, a cominciare da quello con un gruppo Amino libero, e termina con quello con il suo gruppo carbossilico libero.
Alcuni peptidi trovati nel corpo sono i vasopressina, che aumenta la pressione sanguigna e aumenta il riassorbimento di acqua nel rene; il Encefalina, che riduce la sensazione di dolore; e il Ossitocina, che provoca la contrazione dell'utero.
Caratteristiche del legame peptidico
La condensazione del gruppo amminico di un amminoacido con il carbossile di un altro, avviene in solvente acquoso, così che non è spontaneo, e quindi la sintesi proteica richiede un apporto di energia.
Il legame peptidico, come in ogni legame ammidico, presenta risonanza tra due forme estreme: la forma neutra, con un singolo legame che unisce il carbonio carbonilico del primo amminoacido e l'azoto amminico del secondo (C-N), e la forma con separazione delle cariche in cui i due atomi sono legati da un doppio legame (C = N). In realtà il legame peptidico non adotta nessuna delle due situazioni estreme, ma è un ibrido risonante di entrambe.
C'è la chiamata Piano peptidico, consiste in tutti gli atomi coinvolti nel legame peptidico, che uniscono i due amminoacidi iniziali. Da un lato gli atomi di Azoto e Idrogeno, con il rispettivo Carbonio α nel primo amminoacido. Dall'altro il Carbonio α dell'altro amminoacido, con l'Ossigeno e il Carbonio del gruppo Carbonile.
Differenze tra peptidi e proteine
Il i peptidi hanno un basso numero di amminoacidi, che va da due a qualche decina di essi, e la loro conformazione in soluzione diventa flessibile.
Il piccole proteine, strutturalmente vicino ai grandi peptidi, hanno a conformazione definita e molto meno flessibile.
Ci sono proteine che, come i peptidi, hanno una conformazione disordinata e flessibile, ma quell'ordine quando interagiscono con altre macromolecole nella cellula.
20 esempi di aminoacidi che partecipano al legame peptidico
- Glicine
- Alla ragazza
- valina
- leucina
- isoleucina
- Proline
- metionina
- fenilalanina
- tirosina
- Triptofano
- Serina
- treonina
- cisteina
- Asparagina
- Glutammina
- Acido aspartico
- Acido glutammico
- lisina
- arginina
- istidina