15 דוגמאות לאג"ח פשוטות, כפולות ומשולשות
Miscellanea / / July 04, 2021
בכימיה, כשאנחנו מדברים על קשרים בודדים, כפולים ומשולשים אנו מתייחסים לשלוש הצורות הידועות של קשר קוולנטיכלומר של איגודים בין אטומים מתא האלקטרונים של רמות האנרגיה האחרונות שלהם. יש גם את הקשר הקוולנטי הדאטיבי, ובמקרה כזה האלקטרונים המשותפים תורמים רק על ידי אחד האטומים היוצרים את הקשר.
קשרים קוולנטיים מתרחשים כאשר שני אטומים קרובים מספיק כדי לחפוף חלקית שלהם מסלולים אטומיים (אזור החלל שבו עשוי להימצא אלקטרון סביב הגרעין), ובכך מפצה על כוחות המשיכה והדחייה בו זמנית הנובעים ממטעניו אלקטרונים (אלקטרונים שליליים דוחים זה את זה אך המטענים החיוביים של גרעיני האטום מושכים אותם) וקבלת יציבות מרבית המאפשרת להם להוות א מולקולה.
כשזה קורה, זוגות אלקטרונים המקיפים את השכבות החיצוניות ביותר של כל גרעין אטום נעים לעבר השני עד שלא מאפשרים לקבוע לאיזה גרעין אטום הם משתייכים.
הבדלים בין קשר קוולנטי, קשר יוני וקשר מתכתי
סוגי קשרים קוולנטיים
בהתאם למספר זוגות האלקטרונים המשותפים בין האטומים היוצרים את הקשר, הקשרים הקוולנטיים יהיו פשוטים (זוג אחד), כפול (שני זוגות) או משולש (שלושה זוגות). כל אחד מיוצג בדרך כלל על ידי שורה אחת, שתיים או שלוש בין הסמלים של כל אטום:
מספר הקשרים היחידים, הכפולים או המשולשים שאטום יכול ליצור תלוי ישירות בערכיותו, כלומר במספר האלקטרונים שהוא יכול לחלוק מהקליפה החיצונית ביותר שלו.
בנוסף, תלוי במידת המורכבות של הקשר, למולקולה יש פחות או יותר ניידות (פחות ניידות ככל שמורכבת יותר כיוון שהמרחק בין האטומים קטן יותר וקשה יותר לשבור את הקשר, כלומר יש ליישם יותר אנרגיה בכדי להשיג את מתנתק.
דוגמאות קשריות קוולנטיות פשוטות
- מולקולת מימן (H2)
- מולקולת כלור (Cl2)
- מולקולת מימן פלואוריד (HF)
- מולקולת מים (H2אוֹ)
- מולקולת חומצה הידרוכלורית (HCl)

דוגמאות לקשר קוולנטי כפול
- מולקולת חמצן (O2)
- מולקולת פחמן דו חמצני (CO2)
- מולקולת אתילן (ג2ה4)
- מולקולת פרופילן (ג3ה6)
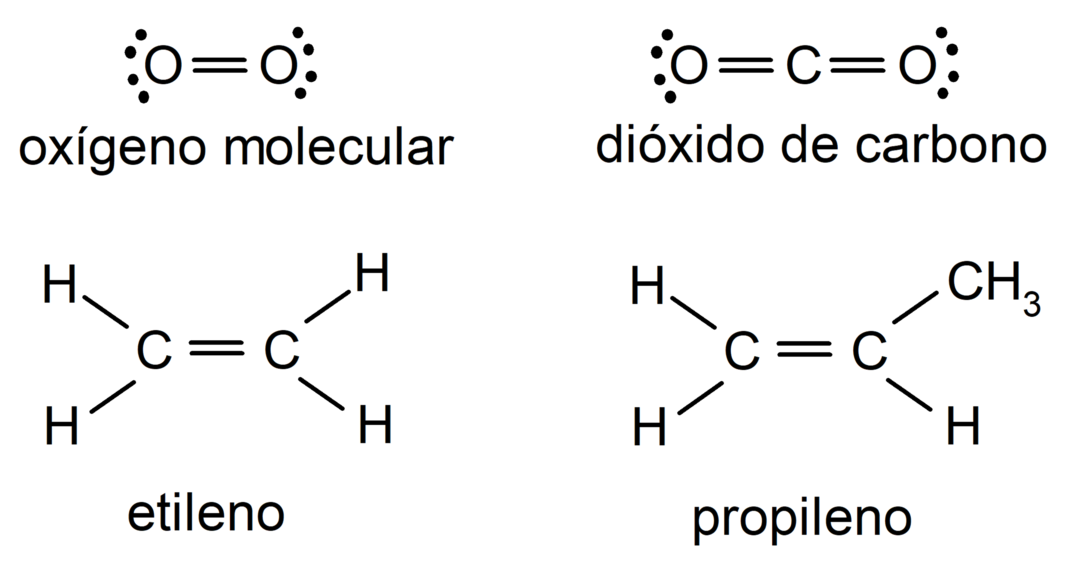
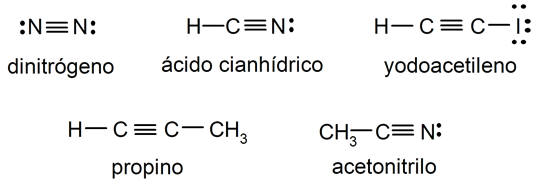
דוגמאות לקשר קוולנטי משולש
- מולקולת חנקן (N2)
- מולקולת מימן ציאניד (HCN)
- מולקולת יודואצטילן (HC2אני)
- מולקולת פרופין (ג3ה4)
- מולקולת אצטוניטריל (CH3CN)
לעקוב עם: