30 דוגמאות למכירות בינאריות
דוגמאות / / November 09, 2023
ה מלחים בינאריים (מלחים ניטרליים) נוצרים כאשר מתכת ובלתי מתכת משתלבים. האם תרכובות כימיות מורכב משניים בלבד יסודות כימיים. לדוגמה: נתרן כלורי (NaCl) ואשלגן ברומיד (KBr).
- ראה גם: מתכות ולא מתכות
דוגמאות למלחים בינאריים
- נתרן כלורי (NaCl)
- ברזל(II) כלוריד (FeCl2)
- ברזל(III) כלוריד (FeCl3)
- קובלט(II) גופרתי (CoS)
- Cobalt(III) sulfide (Co2כן3)
- עופרת (II) גופרית (PbS)
- עופרת (IV) גופרית (PbS2)
- סידן כלורי (CaCl2)
- נתרן פלואוריד (NaF)
- ליתיום כלוריד (LiCl)
- סטרונציום כלוריד (SrCl2)
- בריום כלוריד (BaCl2)
- אלומיניום כלוריד (AlCl3)
- מגנזיום גופרתי (MgS)
- רובידיום כלוריד (RbCl)
- סידן ברומיד (CaBr2)
- אשלגן גופרתי (K2S)
- מגנזיום ברומיד (MgBr2)
- אבץ גופרתי (Zn2S)
- ליתיום ברומיד (LiBr)
- ניקל כלוריד (NiCl2)
- אורניום(III) כלוריד (UCl3)
- ברומיד כסף (AgBr)
- יודיד כסף (AgI)
- אשלגן ברומיד (KBr)
המינוח של מלחים בינאריים
לפי המינוח המסורתי, מלחים בינאריים נקראים על ידי כתיבת השם של היסוד הלא מתכתי עם הסיומת -ide. מצד שני, שם היסוד המתכתי נכתב לפי מצב החמצון שלו:
- עבור מצב החמצון הנמוך ביותר, הוא כתוב עם הסיום -oso. לדוגמה: כלוריד ברזל (FeCl2), כאשר לברזל יש מצב חמצון של 2+.
- עבור מצב החמצון הגבוה ביותר, הוא כתוב עם הסיום -ico. לדוגמה: כלוריד ברזל (FeCl3), כאשר לברזל יש מצב חמצון של 3+.
לפי המינוח השיטתי, מלחים בינאריים נקראים על ידי כתיבת שם היסוד הלא מתכתי עם קידומת המציינת את כמות אטומים של יסוד זה במתחם. בנוסף, הסיום -uro ממוקם על שם האלמנט הלא מתכתי. לאחר מכן, שם האלמנט המתכתי ממוקם. לדוגמה: מגנזיום דיכלוריד (MgCl2) וטריכלוריד ברזל (FeCl3).
לפי המינוח של סטוק, מלחים בינאריים נקראים על ידי כתיבת השם של היסוד הלא מתכתי עם הסיומת -ide. לאחר מכן, שמו של היסוד המתכתי ממוקם ואחריו מצב החמצון שלו כתוב בספרות רומיות ובסוגריים. לדוגמה: ברזל(II) כלוריד (FeCl2) וקובלט(III) סולפיד (Co2כן3).
יישומים של מלחים בינאריים
- הם משמשים כחומרי קירור בתעשיית המזון והתרופות. לדוגמה: סידן כלורי (CaCl2).
- הם משמשים לטיפול במשטחי מתכת נגד קורוזיה. לדוגמה: נתרן פלואוריד (NaF).
- הם משמשים לוויסות הלחות בתעשיית הנייר והבנייה. לדוגמה: סידן כלורי (CaCl2).
- הם משמשים בתעשיית הזכוכית כדי לסלק זיהומים. לדוגמה: סיליקון טטרכלוריד (SiCl4).
- הם משמשים כמרכיבי בישול. לדוגמה: נתרן כלורי (NaCl).
תכונות פיזיקליות של מלחים בינאריים
- יש להם נקודות התכה גבוהות כי הם מורכבים קשרים יוניים.
- הם מוליכים זרם חשמלי כאשר הם מומסים או מותכים.
- למלחים הנפוצים ביותר יש קשיות נמוכה.
- הם אינם ניתנים לדחיסה.
- רובם יכולים להתמוסס במים.
כיצד מתקבלים מלחים בינאריים?
ניתן להשיג מלחים בינאריים באמצעות כמה מהתגובות הכימיות הבאות:
תגובה בין מתכת ללא מתכת. לדוגמה: התגובה בין נתרן (Na) ודיכלוריד (Cl2) מייצר נתרן כלורי (NaCl).
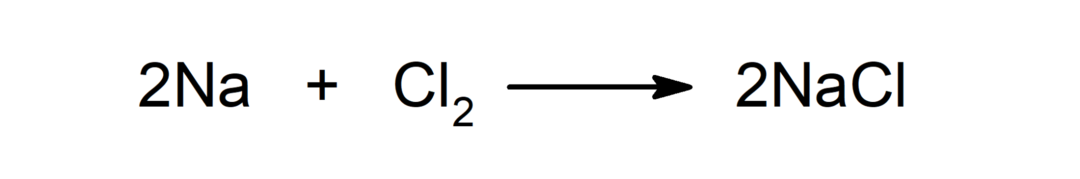
תגובה בין מתכת לחומצה. לדוגמה: התגובה בין אשלגן (K) לחומצה הידרוכלורית (HCl) מייצרת אשלגן כלורי (KCl) ודימימן (H2).
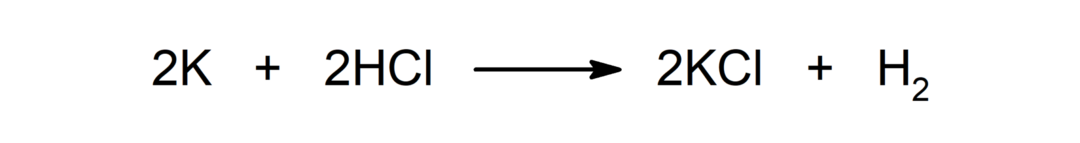
תגובה בין חומצה לבסיס. לדוגמה: התגובה בין חומצה הידרוכלורית (HCl) ונתרן הידרוקסיד (NaOH) מייצרת נתרן כלורי (NaCl) ומים (H2אוֹ).
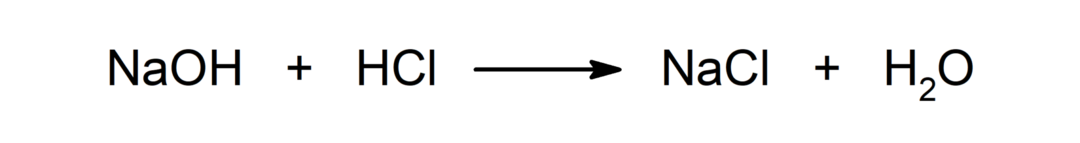
לעקוב עם:
- חמצן
- מלחים ניטרליים
- מלחי חומצה
הפניות
- Cerón Villalba, A., Novoa Ramírez, C. S., & Alpizar Juárez, E. (2020). סרטון נומנקלטורה 1: מלחים בינארים ותגובה כימית.
- אקוריו אריאס, מ. V., & Delgado Méndez, M. ו. (2022). מדריך למידה מבוסס משחק ל"תרכובות בינאריות" בכימיה של תיכון ביחידה החינוכית "הרלינדה טוראל" (תזה לתואר ראשון, האוניברסיטה הלאומית לחינוך).
- קבררה, מ. י. ח. (2005). לימוד מהעקרונות הראשונים של תכונות אלקטרוניות ומבניות של תרכובות בינאריות ושלישיות (עבודת דוקטורט, אוניברסיטת לה לגונה).



