דוגמא לבונד פפטיד
כִּימִיָה / / July 04, 2021
ה פפטיד בונד הוא זה שבו שתי מולקולות של חומצות אמיניות מחוברות על ידי עיבוי.
כדי להבין טוב יותר את קשרי הפפטיד, תחילה יש להגדיר חומצות אמינו:
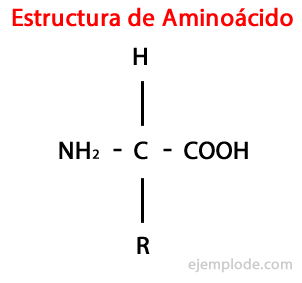
ה חומצות אמינו הן מולקולות אורגניות קצר המכיל לפחות קבוצת אמינו (-NH2), אלקליין בטבע, וקבוצת קרבוקסיל (-COOH), חומצי באופיו.
למרות שיצורים חיים מסנתזים, למטרות שונות, סוגים מגוונים מאוד של חומצות אמינו, החשובים ביותר הם אלה הם חלק מחלבונים, כל אלה שייכים למעמד של חומצות אמינו.
חומצות ה- α- אמיניות מאופיינות בכך שהחומצות וקבוצות האמינו מחוברות לאותו אטום פחמן, הנקרא α Carbon. יתר על כן, פחמן α זה נקשר, כתחליף שלישי, אטום מימן וכרביעי תחליף, קבוצה נוספת בגודל ומאפיינים מגוונים, המבדילה בין כל חומצת אמינו לבין אחרים.
המחליף הרביעי נקרא שרשרת צד חומצה אמינית והיא מיוצגת לעיתים קרובות בצורה פשוטה על ידי האות ר '.
מאחר שארבעת התחליפים של הפחמן α שונים, ומאמצים סביבו סידור טטראדרי, חומצות האמינו הקיימות איזומריזם אופטי, כאשר למולקולה יש צורה חלופית שנראה כמו א תמונת מראה שלו, שבסופו של דבר איננה מולקולה שווה. לשתי הצורות האיזומריות הללו של המולקולה מוקצות האותיות D או L, תלוי באופן שבו התחליפים מסודרים במרחב. כל חומצות האמינו שיש בחלבונים הם L.
חומצות אמינו מסווגות על פי אופיים הכימי ב קוטב ואפולאר. הקוטבים בתורם מחולקים ל ניטרלי ומוטען (שיכולים להיות חומציים או בסיסיים). ה לא קוטבי יכול להיות אליפטי או ארומטי.
פפטידים וקשר הפפטידים
פפטידים הם תוצר של איחוד קוולנטי של חומצות אמינו דרך קשרי אמיד, ויוצרים על ידי עיבוי של קצה הקרבוקסיל של הקצה וקצה האמינו של השני, שחרור מולקולת מים ב תְגוּבָה. האיחוד הזה נקרא פפטיד בונד.
להלן מוצג מנגנון התגובה הזו, בו ה קבוצות אמינו וקרבוקסיל, והעיבוי של מולקולות החומצות האמיניות מתרחש ליצירת הפפטיד.
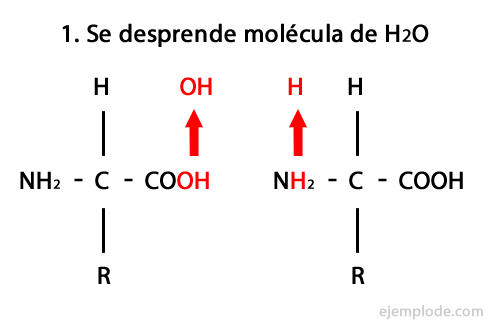
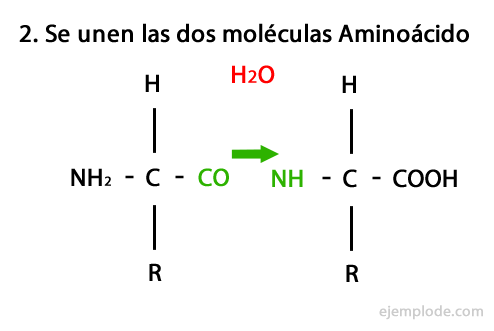

פפטידים, כמו חומצות אמינו וחלבונים, יש בקבוצתם קבוצת אמינו וקבוצת קרבוקסיל בלי להגיב.
כדי לציין את הנוסחה של פפטיד פשוט, ואפילו חלבון, מספיק לרשום את חומצות האמינו המרכיבות אותו, החל עם הקבוצה עם קבוצת אמינו בחינםוכלה בזה עם קבוצת הקארבוקסיל החינמית שלה.
כמה פפטידים שנמצאים בגוף הם וזופרסין, שמעלה את לחץ הדם ומגביר את ספיגת המים מחדש בכליה; ה אנצפלין, המפחית את תחושת הכאב; וה אוקסיטוצין, שגורם לרחם להתכווץ.
מאפייני אג"ח פפטיד
ההתעבות של קבוצת אמינו של חומצת אמינו אחת עם קרבוקסיל של אחרת, מתרחש בממיס מימי, אז זה זה לא ספונטניולכן סינתזת חלבונים דורשת אספקת אנרגיה.
אג"ח הפפטיד, כמו בכל קשר אמידי, מציג תהודה בין שתי צורות קיצוניות: הצורה הנייטרלית, עם קשר יחיד המצטרף לפחמן הקרבוניל של חומצת האמינו הראשונה ולחנקן האמינו של השני (C-N), ו הטופס עם הפרדת מטענים בו שני האטומים מקושרים על ידי קשר כפול (C = N). במציאות, קשר הפפטיד אינו מאמץ את שני המצבים הקיצוניים, אלא מהווה הכלאה מהדהדת של שניהם.
יש את השיחה מטוס פפטיד, המורכב מ כל האטומים המעורבים בקשר הפפטיד, המצטרפים לשתי חומצות האמינו הראשוניות. מצד אחד, אטומי החנקן והמימן, עם הפחמן α בהתאמה שלהם בחומצת האמינו הראשונה. מצד שני, הפחמן α של חומצת האמינו האחרת, עם החמצן והפחמן מקבוצת הקרבוניל.
הבדלים בין פפטידים וחלבונים
ה לפפטידים מספר נמוך של חומצות אמינו, שנע בין שניים לכמה עשרות מהם, והתאמה שלהם בתמיסה הופכת לגמישה.
ה חלבונים קטנים, קרוב מבנית לפפטידים גדולים, יש קונפורמציה מוגדרת והרבה פחות גמישה.
ישנם חלבונים שכמו פפטידים הם בעלי קונפורמציה לא מסודרת וגמישה, אך הם מסדרים כאשר הם מתקשרים עם מקרומולקולות אחרות בתא.
20 דוגמאות לחומצות אמינו המשתתפות במליטה פפטיד
- ויסטריה
- לילדה
- ואלין
- לאוצין
- איזולאוצין
- פרולין
- מתיונין
- פנילאלנין
- טירוזין
- טריפטופן
- סרין
- תראונין
- ציסטאין
- אספרגין
- גלוטמין
- חומצה אספרטית
- חומצה גלוטמית
- ליזין
- ארגינין
- היסטידין
