דוגמת החוק של בויל
פיזיקה / / July 04, 2021
כאשר בוחנים את תכונות הגזים, רוברט בויל, מצד אחד, ו אדם מריוטמצד שני, מבלי לדעת או לדעת את הניסויים שלהם, הם הבחינו כי ניתן לדחוס גזים, וכי נפחם משתנה ביחס ללחץ אליו הם נתונים.
כדי להבין את המחקר שלו, עלינו לזכור כי ישנם שלושה מאפיינים שיש לקחת בחשבון במחקר זה של גזים: טמפרטורה, נפח ולחץ.
טמפרטורה: זוהי הטמפרטורה בה נמצא גז בתנאי הניסוי. זה יכול לבוא לידי ביטוי במעלות צלזיוס (° C) או במעלות קלווין או באפס מוחלט (° K). במקרה של חוק בויל, רואים שהטמפרטורה לא משתנה, כלומר היא נשארת קבועה.
נפח: זהו החלל שגז תופס בתוך מיכל סגור. בכוונה ראשונה, נפח הגז הוא נפח המיכל. לייצוגו, נחשב כי המכולה סגורה ועם בוכנה, כגון מזרק.
לחץ: זהו הלחץ שיש לגז דרך הבוכנה. במיכל סגור, שעליו מונח הבוכנה כמכסה, ללא הפעלת לחץ, הוא נחשב ללחץ אטמוספרי (1 at).
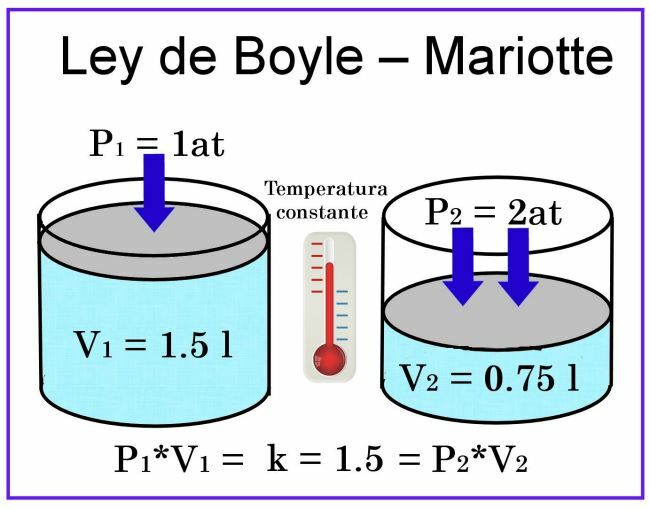
בתצפיות בויל ומריוט הטמפרטורה נחשבת קבועה, ולכן היא לא תשפיע על המדידה.
לגבי נפח, אם ניקח בחשבון, למשל, מיכל גלילי בנפח 1 ליטר, והמכסה שלו הוא בוכנה החלקה, כאשר מניחים אותה מכסה את המכולה המלאה באוויר, הלחץ יהיה 1 ב, ואילו הנפח יהיה 1 לִיטר. אם יופעל על הבוכנה לחץ של 2 אטמוספרות, נפח הגז יופחת בחצי, כלומר ל 0.5 ליטר או 500 מ"ל. אם הלחץ יגדל ל -4 אטמוספרות, הנפח יופחת לרבע, כלומר ל- 0.25 ליטר, או 250 מ"ל.
בהתבסס על תצפיות אלה, השיחה בוטלה חוק בויל: בטמפרטורה קבועה, נפח הגז ביחס הפוך ללחץ המופעל עליו.
משמעות הדבר היא שכאשר הלחץ עולה, הנפח יורד, וכאשר הלחץ יורד, הנפח עולה.
זה מוביל לקבוע כי קיים קשר בין לחץ הגז לנפחו, המשתנה אחד המרכיבים, השני משתנה באותו פרופורציה, הקשר נשאר קבוע, כלומר אמר:
P * V = k
P = לחץ
V = נפח
k = קבוע של יחסי לחץ-נפח
כדי להבין זאת, נניח שיש לנו מיכל 2.5 ליטר, שמלא באוויר והלחץ על הבוכנה הוא 1.5 ב. אז קבוע מערכת היחסים שלך הוא:
P * V = k = (2.5) (1.5) = 3.75
אם כעת נגדיל את הלחץ ל -3 אטמוספרות, נחלק את k בלחץ P, ויהיה לנו:
k / P = V.
3.75 / 3 = 1.25 ליטר
כפי שאנו רואים, בעת הפעלת לחץ כפול, הנפח הוא חצי מהמקור, ונשמר קבוע של יחס הלחץ-נפח. זה מתבטא באופן הבא:
ו1פ1 = V.2פ2 = k
כלומר, תוצר נפח 1 פעמים לחץ 1 שווה לתוצר נפח 2 פעמים לחץ 2, וקשר זה נשאר קבוע.
דוגמאות לחוק בויל-מריוט
דוגמה 1. חשב את הנפח שתופס גז, שתופס נפח של 3.75 ליטר, בלחץ של 2 אם מופעל עליו לחץ של 3.5 at.
ו1 = 3.75 ליטר
פ1 = 2 בשעה
ו2 = ?
פ2 = 3.5 בשעה
כמו וי1פ1 = V.2פ2 = k
אנו מחשבים את קבוע המערכת:
ו1פ1= k = (3.75) (2) = 7.5
אנחנו פותרים עבור V2:
ו2 = k / P2 = 7.5 / 3.5 = 2,143 ליטר
דוגמה 2. חישב את הלחץ המופעל על גז, אם הוא תופס נפח של 2.25 ליטר, אם בלחץ של 1.75 עליו הוא נפח של 3.25 ליטר.
ו1 = 3.25 ליטר
פ1 = 1.75 בשעה
ו2 = 2.25 ליטר
פ2 = ?
אנו מחשבים את קבוע המערכת:
ו1פ1= k = (3.25) (1.75) = 5.6875
אנו פותרים עבור P2:
פ2 = k / V2 = 5.6875 / 2.25 = 2.53 בשעה
דוגמה 3. חשב את הלחץ המקורי של גז, אם בעת הפעלת לחץ של 4.5 at הוא תופס נפח של 1.4 ליטר, ונפחו המקורי היה 2.2 ליטר.
ו1 = 2.2 ליטר
פ1 = ?
ו2 = 1.4 ליטר
פ2 = 4.5 בשעה
אנו מחשבים את קבוע המערכת:
ו2פ2= k = (1.4) (4.5) = 6.3
אנו פותרים עבור P2:
פ1 = k / V1 = 6.3 / 2.2 = 2.863 בשעה
