ハロゲンの特性
化学 / / July 04, 2021
ハロゲンは、周期表のグループVIIAまたはグループ17にある化学元素です。 これは、フッ素、塩素、臭素、ヨウ素、および状態の元素で構成されています。
ハロゲンという名前はギリシャ語に由来し、「塩の生産者」を意味します。これらの元素は、一般的な塩と同様の特性を持つナトリウムと塩を形成するためです。
ハロゲンの一般的な特性:
それらは一価の元素です。つまり、それらは1つの価数しか持っていません。 ハロゲンでは、原子価は-1です。
それらは水素に親和性があり、いわゆる水素酸を形成します。
それらは酸素との親和性がほとんどないため、酸化物を形成しませんが、非常に高温になります。
それらは金属と結合してハロゲン塩を形成します。
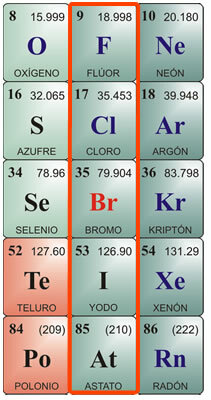
ハロゲンの個々の特性:
フッ素の特性:
化学記号F。 原子番号9、原子量19。 純粋な状態のフッ素は黄色のガスで、融点は-223°C、沸点は-187°Cです。 それは本質的に自由に存在しないので、隔離されなければなりません。 それは1886年に最初に分離されました。 その物理的特性は次のとおりです。緑がかった黄色のガス、非常に腐食性で刺激性があり、刺激臭があり、人や動物に有毒です。 液化が難しい。 化学的特性:非常に低温でも発熱反応を伴い、水素と結合します。 それは金属と結合して塩を形成します。 塩酸を分解して塩素を生成し、水を分解して酸素を放出します。 水素との親和性があるため、有機物質から取り出して炭化します。 その主な化合物の1つはフッ化水素酸であり、ガラス中のシリカを攻撃するため、プラチナまたはワックスジャーにのみ保管できます。 それは非常に揮発性で非常に腐食性です。 金属と組み合わせると、フッ化物を生成します。
塩素の特徴:
元素記号Cl。原子番号17、原子量35.5。 融点-102°C、沸点-37°C。 塩素は1774年に発見され、1811年に分離されました。 物理的性質:それは緑がかった黄色のガスであり、一般に塩に結合して見られるため、自然界では自由には存在しません。 息苦しくて有毒な臭いがします。 化学的性質:塩素は水素に非常に似ており、発熱反応で結合して塩酸を生成します。 塩酸または発煙塩とも呼ばれる塩酸は、古代ローマから知られていました。 それは火山でガス状の状態で発見され、火山の近くのいくつかの川の水に溶けました。 皮膚に非常に腐食性があり、摂取すると有毒です。 それは消化のために胃によって生成されます。 他の重要な塩素化合物は次亜塩素酸塩、特に次亜塩素酸ナトリウムであり、水に溶解すると、水漂白剤、消毒剤、および滅菌剤として使用されます。 酸を中和します。
臭素の特徴:
元素記号Br。原子番号35、原子量79.9。 融点-7.3°C、沸点58.8°C。 自然界では遊離していませんが、金属と結合して臭化物を形成します。 電気分解により分離されます。 物性:刺激臭のある暗赤色の液体です。 室温では、刺激性の濃いオレンジレッドの蒸気を放出し、咳や涙を引き起こします。 有毒です。 エーテルやクロロホルムに溶け、水にはほとんど溶けません。 化学的性質:臭素は有機物を攻撃します。 生き物では、それは皮膚を腐食し、治癒するのが難しい潰瘍を引き起こします。 その主な用途は、以前は写真で使用されていた臭化銀などの工業用途に使用される臭化物を形成する金属と組み合わされています。 それらはまた防腐剤として低濃度で使用されます。 水素と組み合わせると、臭化水素酸が生成されます。臭化水素酸は、刺激的な臭いと味のある無色のガスで、主に金属を攻撃して臭化物を得るのに使用されます。
の特徴 ヨウ素:
化学記号I。 原子番号53、原子量126.9。 融点113°C; 沸点184°C。 それは本質的に自由に存在するものではありません。 海藻床のヨウ化物として、またクレソン、タラ油、甲殻類などの一部の食品のミネラルの一部として含まれています。 物性:ヨウ素は固体の結晶体で、色は黒みがかった灰色で、金属光沢があり、強く不快な臭いがします。 水に溶けにくく、アルコールに非常に溶けやすい。 化学的性質:ヨウ化物を形成する金属と結合します。 硫黄やリンなどのメタロイドも含まれます。 それは他のハロゲンよりも酸素に対して高い親和性を持っています。 アンモニアと組み合わせると、爆発性ガスであるヨウ化窒素を生成します。 水素と結合すると、刺激的な臭いと味のある無色のガスであるヨウ化水素酸を生成し、空気の存在下で喫煙します。 水に溶け、光と熱の作用で分解します。 酸分子に酸素が含まれていると、酸化特性を持つ結晶性固体であるヨウ素酸が生成されます。 ヨウ素は、消毒剤および防腐剤としてアルコール溶液に使用されます。
の特徴 ステータス:
アットマーク。 原子番号85、原子量210。 それは本質的に自由に存在するものではありません。 融点254°C; 沸点962°C。 アスタチンは、アルファ線によるビスマス原子の分解から放出される元素であるため、1940年代に最初に合成されました。 寿命が非常に短い放射性元素です。 最も長持ちする同位体はAt210で、最大寿命は約8時間です。 その化学的性質はヨウ素の化学的性質と非常に似ていると考えられています。 物理的には、金属に似た外観と特性を持つ可能性があります。 放射性元素であるにもかかわらず、自然界では通常見られないため、健康に害を及ぼすことはありません。 それは、亜原子物質の研究における原子の標識のために、実験室でほんの少しの用途しかありません。



