25 ჰალიდების მაგალითები
მაგალითები / / November 09, 2023
ა ჰალოიდი ან ჰალიდი ეს არის ქიმიური ნაერთი ორობითი, რომელიც შედგება ა ატომი ჰალოგენისა და ელემენტის ან კატიონის, რომელსაც აქვს ჰალოგენზე დაბალი ელექტრონეგატიურობა. Მაგალითად:
- ნატრიუმის ქლორიდი (NaCl)
- კალციუმის ფტორიდი (CaF2)
- კალიუმის ბრომიდი (KBr)
- წყალბადის ქლორიდი (HCl(გ))
ჰალოგენები არიან ქიმიური ელემენტები რომლებიც ქმნიან მე-17 ჯგუფს Პერიოდული ცხრილი. ჰალოგენებია: ფტორი (F), ქლორი (Cl), ბრომი (Br), იოდი (I), ასტატინი (At), ტენესო (Ts).
- Იხილეთ ასევე: ალდეჰიდები და კეტონები
ჰალოიდების სახეები
მათი შემადგენლობიდან გამომდინარე, ჰალოიდები შეიძლება იყოს:
- არაორგანული ჰალოიდები. ეს არის არაორგანული ქიმიური ნაერთები, რომლებიც შეიცავს ჰალოგენის ერთ ან მეტ ატომს. ისინი შეიძლება იყოს არაორგანული მარილები, წყალბადის ჰალოგენები ან ლითონის კომპლექსები. Მაგალითად: ნატრიუმის ქლორიდი (NaCl) და ტეტრაიოდომერკური ანიონი HgI42-.
- ორგანული ჰალოიდები. ეს არის ორგანული ქიმიური ნაერთები, რომლებიც შეიცავს ჰალოგენის ერთ ან მეტ ატომს, რომელიც დაკავშირებულია ორგანული ნაერთის ნახშირბადის ატომთან. Მაგალითად: მეთილის ქლორიდი (CH3 – Cl) და ტრიქლორმეთანი (CH – Cl3).
ჰალოიდების მაგალითები
- ნატრიუმის ქლორიდი (NaCl)
- კალციუმის ქლორიდი (CaCl2)
- ვერცხლის ფტორი (AgF)
- ლითიუმის ფტორიდი (LiF)
- კალიუმის იოდიდი (KI)
- კალიუმის ბრომიდი (KBr)
- სპილენძის (II) ქლორიდი (CuCl2)
- რკინის (III) ქლორიდი (FeCl3)
- ქრომის(III) ბრომიდი (CrBr3)
- ალუმინის ქლორიდი (AlCl3)
- ამონიუმის ქლორიდი ((NH4)Cl)
- ტყვიის (II) იოდიდი (PbI2)
- მაგნიუმის იოდიდი (MgI2)
- ბერილიუმის ფტორიდი (BeF2)
- ალუმინის ფტორი (AlF3)
- ბრომმეთანი (CH3 - ძმ)
- იოდოფორმი (CHI3)
- მეთილის ქლორიდი (CH3 -Cl)
- ბრომოეთანი (CH3 – ჩვ2 - ძმ)
- დიქლორეთანი (Cl – CH2 – ჩვ2 -Cl)
- ვერცხლის ბრომიდი (AgBr)
- კალის(IV) ქლორიდი (SnCl4)
- ტიტანის (IV) ქლორიდი (TiCl4)
- წყალბადის ქლორიდი (HCl(გ))
- წყალბადის ბრომიდი (HBr(გ))
ჰალოიდების ფიზიკური თვისებები
ჰალოიდების ზოგიერთი ფიზიკური თვისებაა:
- ალკილის ჰალოიდებს (ორგანულ ჰალოგენებს) აქვთ უფრო მაღალი სიმკვრივე და დუღილის წერტილი, ვიდრე მათი შესაბამისი ალკანები. ეს ხდება იმის გამო, რომ ჰალოგენის ატომმა შეცვალა წყალბადის ატომი ნახშირწყალბადის საიდანაც მოდის ჰალოიდი.
- ორგანული ფტორიდები და ქლორიდები წყალზე ნაკლებად მკვრივია, ხოლო ორგანული ბრომიდები და იოდიდები უფრო მკვრივია ვიდრე წყალი.
- ალკილის ჰალოიდები წყალში უხსნადია და ორგანულ გამხსნელებში ხსნადი.
- წყალბადის ჰალოიდები არის აირები, რომლებსაც აქვთ მკვეთრი სუნი ოთახის ტემპერატურაზე.
- პერიოდული ცხრილის 1 ჯგუფის ელემენტების ატომებით წარმოქმნილი ჰალოიდები თეთრი მყარია.
ჰალოიდების ქიმიური თვისებები
- ალკილის ჰალოიდები განიცდიან ალიფატურ ნუკლეოფილურ ჩანაცვლების რეაქციებს. ეს არის რეაქციები, რომლებშიც ნუკლეოფილური ატომი (ელექტრონებით მდიდარი) ცვლის ატომს (გასასვლელ ჯგუფს), რომელიც მიმაგრებულია ელექტროფილ ატომზე (ელექტრონებით დეფიციტი).
Მაგალითად: მეთილის ბრომიდის რეაქციაში (CH3 - Br) ნატრიუმის ჰიდროქსიდით (NaOH), მეთილის ბრომიდში ბრომი (დამტოვებელი ჯგუფი) იცვლება ჰიდროქსიდის იონით (ნუკლეოფილი), სადაც ნახშირბადი არის ელექტროფილი.
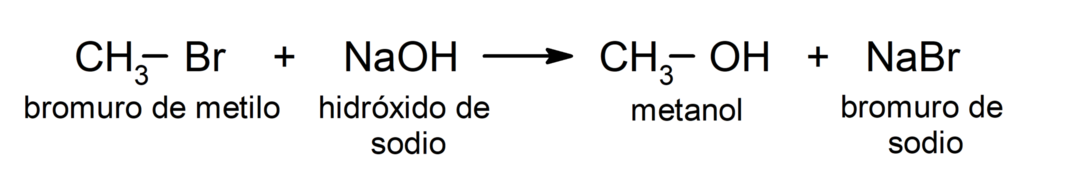
- ზოგიერთი ალკილის ჰალოიდი რეაგირებს მაგნიუმთან გამხსნელებში, როგორიცაა ეთერი ან ტეტრაჰიდროფურანი, და შედეგად მიღებული პროდუქტი არის ორგანომეტალური ნაერთი, რომელსაც ეწოდება "გრინიარდის რეაგენტი". Მაგალითად: ეთილის ბრომიდი (CH3 – ჩვ2 - Br) მაგნიუმით (მგ) რეაგირებს მშრალ გარემოში ეთილმაგნიუმის ბრომიდის წარმოქმნით (CH3 – ჩვ2 - MgBr).

- პირველადი ალკილის ჰალოიდები განიცდიან რეაქციას ალკოქსიდებთან ან ალკოჰოლები ძირითად გარემოში ეთერების წარმოებისთვის. ეს რეაქციები ცნობილია როგორც "ვილიამსონის სინთეზი". Მაგალითად: რეაქცია მეთილის ბრომიდს შორის (CH3Br) და ნატრიუმის მეთოქსიდი (CH3ONa) წარმოქმნის დიმეთილ ეთერს (CH3OCH3).
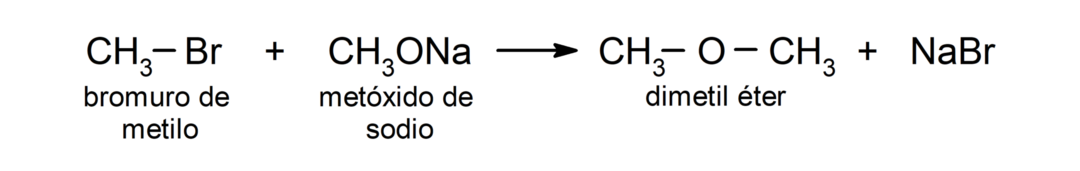
ჰალოიდების გამოყენება
ჰალოიდებს ან ჰალოიდებს აქვთ სხვადასხვა გამოყენება ინდუსტრიაში, მედიცინაში და ყოველდღიურ ცხოვრებაში. ამ აპლიკაციებიდან ზოგიერთია:
- ისინი გამოიყენება როგორც გამხსნელები ბევრისთვის ორგანული ნაერთები.
- ისინი გამოიყენება როგორც სადეზინფექციო და ანტისეპტიკები.
- ისინი გამოიყენებოდა როგორც გამაგრილებელი.
- ისინი გამოიყენება ფტორირებული პოლიმერების წარმოებაში. მაგალითად, ტეფლონი.
- მედიცინაში იყენებენ საკვებ მარილებს ან ნაყენს.
- ისინი გამოიყენება წყლის გაწმენდისა და გაწმენდისთვის.
- ლითონის ჰალოიდები გამოიყენება ნათურების წარმოებაში.
- ისინი გამოიყენება ელექტრონული კომპონენტების დასუფთავებაში.
- ისინი გამოიყენება როგორც საწყისი ქიმიკატები უფრო რთული ორგანული ნაერთების სინთეზისთვის.
- ზოგიერთი, როგორიცაა ვერცხლის ბრომიდი (AgBr), გამოიყენება ფოტოგრაფიული ფირფიტების შესაქმნელად.
ჰალოიდების საფრთხე
გამხსნელად გამოყენებული ალკილის ჰალოიდები ძალადობრივად რეაგირებენ ძლიერ ფუძეებთან და ძლიერ ოქსიდანტებთან, რამაც შეიძლება გამოიწვიოს აფეთქებები და ხანძარი.
გარდა ამისა, ქლოროფტორნახშირბადები (CFC) არის ალკილის ჰალოიდები, რომლებიც გამოიყენება ათწლეულების განმავლობაში, როგორც გამაგრილებელი, მაგრამ მათი დასაქმება აკრძალულია საერთაშორისო ორგანიზაციების მიერ, რადგან ისინი ძირითადად პასუხისმგებელნი არიან ფენის ხვრელზე ოზონი.
მეორეს მხრივ, წყალბადის ჰალოიდები აღიზიანებს თვალებს, კანს და ლორწოვან გარსებს.
მიჰყევით:
- შენ გამოდი
- მჟავა მარილები
- ნეიტრალური მარილები
ცნობები
- სალომონსი, ტ. გ. (1996). ორგანული ქიმიის საფუძვლები. უილი.
- უაიტენი, კ. ვ., გეილი, კ. დ., დევისი, რ. ე., დე სანდოვალი, მ. თ. TO. ო., და მურადასი, რ. მ. გ. (1992). ზოგადი ქიმია (გვ. 108-117). მაკგრაუ-ჰილი.
- უელსი, ა. ფ. (1978). სტრუქტურული არაორგანული ქიმია. დაბრუნება.

