ენდოთერმული რეაქციების მაგალითები
მაგალითები / / November 09, 2023
ა ენდოთერმული რეაქცია ეს არის რეაქცია, რომელიც შთანთქავს ენერგიას საშუალოდან სითბოს სახით. ამ რეაქციებში რეაქტიული ნივთიერებების პროდუქტებად გადაქცევისთვის აუცილებელია, რომ ისინი შთანთქას სითბოს, რაც იწვევს პროდუქტებს უფრო დიდი ენერგიის მქონე რეაქტორებთან შედარებით, რამაც გამოიწვია ისინი. ენდოთერმული რეაქციების რამდენიმე მაგალითია: ფოტოსინთეზი და წყლის ელექტროლიზი.
- Იხილეთ ასევე: Ქიმიური რეაქციები
ენდოთერმული რეაქციების მაგალითები ყოველდღიურ ცხოვრებაში
ზოგიერთი ძირითადი ენდოთერმული რეაქციაა:
ოზონის წარმოება ატმოსფეროში. ოზონი წარმოიქმნება ატმოსფეროში, როდესაც მოლეკულური ჟანგბადი (O2) შთანთქავს ულტრაიისფერ გამოსხივებას და იშლება. შემდეგ ჟანგბადის ატომს (O) შეუძლია ურთიერთქმედება სხვა ჟანგბადის მოლეკულასთან (O2) და ქმნის ოზონს (O3).

წყლის ელექტროლიზი. ეს არის პროცესი, რომლითაც იგი გამოიყენება ელექტროენერგიის წყალს, რათა გამოყოს იგი თავის ორ კომპონენტად, წყალბადად (H) და ჟანგბადად (O).
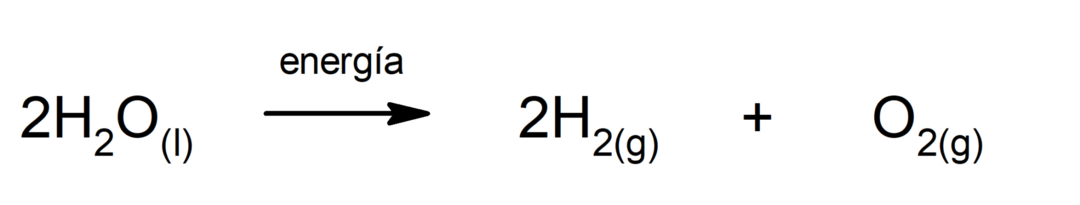
ფოტოსინთეზი. ეს არის ქიმიური რეაქცია, რომლითაც შთანთქავს მზის ენერგიანახშირორჟანგი (CO2) გარდაიქმნება გლუკოზად. ეს რეაქცია მცენარეთა კვების ძირითად გზას წარმოადგენს.
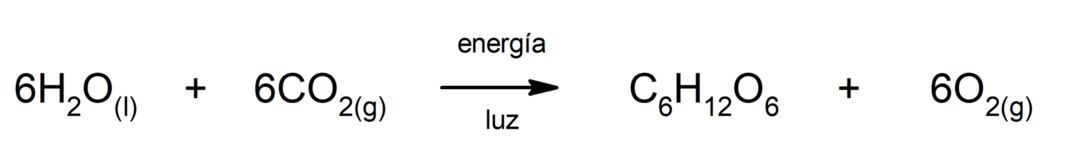
რკინის (II) სულფიდის წარმოება. გოგირდსა და რკინას შორის რეაქცია რომ მოხდეს, საჭიროა ენერგიის მიწოდება სითბოს სახით.
ნახშირორჟანგის დაშლა (CO2). CO-ს დაშლა2 მაღალ ტემპერატურაზე ის წარმოქმნის ნახშირბადის მონოქსიდს (CO) და ჟანგბადს (O2).
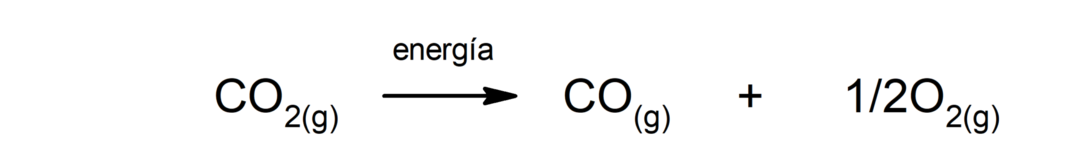
კალციუმის კარბონატის დაშლა (CaCO3). კალციუმის კარბონატი იშლება სითბოს შთანთქმით და წარმოქმნის კალციუმის ოქსიდს (CaO) და ნახშირორჟანგს (CO).2).
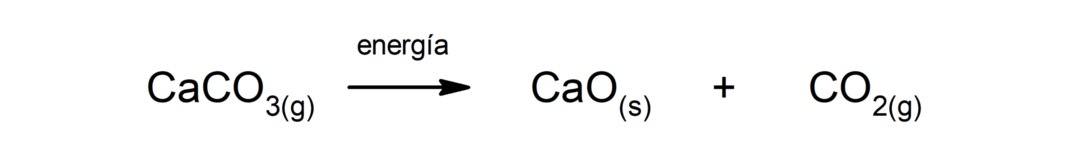
განსხვავება ენდოთერმულ და ეგზოთერმულ რეაქციას შორის
ენდოთერმული და ეგზოთერმული რეაქციების მთავარი განსხვავება ისაა, რომ ენდოთერმული რეაქციები შთანთქავს სითბოს, ხოლო ეგზოთერმული რეაქციები ათავისუფლებს სითბოს.
გარდა ამისა, ენდოთერმული რეაქციები ხასიათდება ენთალპიის ზრდით, ხოლო ეგზოთერმული რეაქციები დაკავშირებულია ენთალპიის შემცირებასთან.
ენთალპია არის თერმოდინამიკური სიდიდე, რომელიც განსაზღვრავს თერმული ენერგიის ნაკადს მუდმივი წნევის დროს ქიმიური რეაქციის დროს. იგი წარმოდგენილია ასო H-ით და მისი ცვალებადობა არის ერთ-ერთი მთავარი ინდიკატორი იმის დასადგენად, არის თუ არა ქიმიური რეაქცია ენდოთერმული თუ ეგზოთერმული.
- თუ ქიმიურ რეაქციას აქვს ენთალპიის ცვლილება ნულზე მეტი (ΔH > 0) არის ენდოთერმული.
- თუ ქიმიურ რეაქციას აქვს ენთალპიის ცვლილება ნულზე ნაკლები (ΔH <0) ეგზოთერმულია.
მიჰყევით:
- ფიზიკოქიმიური მოვლენები
- ქიმია ყოველდღიურ ცხოვრებაში
- ქიმია ყოველდღიურ ცხოვრებაში
- ორგანული და არაორგანული ქიმია
ცნობები
- სოტო-კორდობა, ს. (2016). ენდოთერმული რეაქციები. ტექნიკური საცავი კოსტა რიკის ტექნოლოგიური ინსტიტუტი.
- კორომინასი, ჯ. (2017). ყოველდღიური ცხოვრების ქიმიური რეაქციები. ალემბიკი, (90), 8-26.
- სანჩესი, მ. თ. მ., და სანჩესი, მ. მ. (2002). ენდოთერმული რეაქციების ექსპერიმენტული შესწავლა ESO სტუდენტებისთვის. RSEQ-ის ქიმიის ანალები, (4), 36-39.