ორგანული ქიმიის მაგალითი
Ქიმია / / July 04, 2021
Ორგანული ქიმია ეს არის ზოგადი ქიმიის ნაწილი, რომელიც პასუხისმგებელია ქიმიური ნაერთების შესწავლასა და ფუნქციონალურ კლასიფიკაციაზე, რომელთა სტრუქტურული ელემენტია Ნახშირბადის, უხვად იმყოფება ცოცხალი ნივთიერება; ეს ქმნის არაორგანული ქიმიის ძალიან დიფერენცირებულ სამყაროს, რომელიც ეძღვნება ქიმიურ ნაერთებს, რომლებიც კლასიფიცირდება როგორც მინერალები.
ნახშირბადის ატომს თავისი ელექტრონული კონფიგურაციის ბოლო გარსში აქვს ოთხი ელექტრონი. ეს მახასიათებელი, თავის ატომურ რადიუსთან ერთად, საშუალებას აძლევს მას შეუერთდეს კოვალენტური ბმები სხვასთან ერთი და იმავე ელემენტის ატომები, მრავალრიცხოვან ჯაჭვებში, ქმნიან მრავალფეროვან ქიმიურ ნაერთებს სტაბილური.
Შეგიძლია შეამოწმო კოვალენტური ობლიგაციები.
ასეთი ქიმიური ნაერთები, ნახშირბადის ატომების გარდა, რომლებიც მათ პირველყოფილ სტრუქტურას ანიჭებენ, შეიცავს წყალბადის ატომებს, როგორც ნახშირბადის ვალენტობის მთავარ კომპლემენტს. გარდა ამისა, ნაერთების ამ მრავალფეროვნებაში არსებობს ჟანგბადის ატომების ჩარევა, აზოტი, ჰალოგენები, გოგირდი და კიდევ ფოსფორი, ტუტე და ტუტე მიწის ელემენტები და ლითონები გარდამავალი. დამოკიდებულია იმაზე, თუ ვინ მონაწილეობს მოლეკულაში, ეს იქნება საბოლოო ნივთიერების ფიზიკური და ქიმიური თვისებები.
ორგანული ნაერთები იმყოფებიან მთელ საქართველოში ცოცხალი ნივთიერება; ხელი შეუწყოს და შეინარჩუნოს ყველა ბიოლოგიური ფუნქციებიარაორგანული ან მინერალური ნივთიერებებისგან განსხვავებით, რომლებსაც ადამიანები იყენებდნენ კომერციული მიზნებისთვის, ექსპერიმენტებისთვის ან გარკვეული საშინაო დავალებების შესასრულებლად.
ორგანული ქიმიის ისტორია
1828 წლამდე უკვე ხდებოდა განსხვავება ორგანულ ქიმიასა და არაორგანულ ქიმიას შორის. ორგანული ნივთიერებები ასოცირდება ქმნილებასთან მეშვეობით a "სასიცოცხლო ძალა"და არაორგანული არაცოცხალი, მინერალური. ამ კონცეფციების გათვალისწინებით, არ შეიძლება ველოდოთ ორგანული ნაერთების მიღებას არაორგანული მასალებისგან ლაბორატორიაში.
თუმცა, 1828 წელს ფრიდრიხ ვალერი (1800-1882) მოახერხა ორგანული ნივთიერების მომზადება, შარდოვანა CO (NH)2)2, ცხოველური ცვლის მნიშვნელოვანი პროდუქტია არაორგანული ნაერთებისგან. მკურნალობა ტყვიის ციანატის Pb (CNO)2 თან ამიაკი NH3 მიღება ამონიუმის ციანატი NH4CNO; ეს ნაერთი მართლაც წარმოიქმნა, მაგრამ როდესაც ამონიუმის ციანატის კრისტალების მიზნით ხსნარი ადუღეს, იგი შარდოვანად გადაიქცა.
ეს ქიმიური ცვლილება მაგალითია შიდა გადაჯგუფება, რომელშიც არ იცვლება ატომების რაოდენობა ან კლასი მოლეკულაში, არამედ მხოლოდ მათი რიგი მასში. ამ ტიპის გარდაქმნები ძალიან ხშირია ორგანულ ქიმიაში.
ვილერის აღმოჩენამ მოგვიანებით დაიწყო სიცოცხლის ძალის თეორიის მიტოვება მთლიანად გადააგდეს, რასაც მოჰყვა მრავალი სხვა ორგანული ნაერთის მომზადება ლაბორატორია ამის მიუხედავად, არაორგანული და ორგანული საკვალიფიკაციო პირობები არსებობს, ვინაიდან არაორგანული ნაერთები დაკავშირებულია მინერალურ პროდუქტებთან და ორგანული ნაერთები, რომლებიც სინამდვილეში ნახშირბადის და წყალბადის ნაერთებია და მათი წარმოებულები, ცოცხალი ორგანიზმების მიერ წარმოებული ტიპისაა.
მიუხედავად იმისა, რომ ზოგადი ქიმიის კანონები თანაბრად ვრცელდება ორივე ნაერთზე, სხვადასხვა მიზეზები ამართლებს და საჭიროებს ამ დაყოფას. ამრიგად, ორგანული და არაორგანული ნაერთები განსხვავდება სხვადასხვა თვისებებით, როგორიცაა: მათი ხსნადობა სასურველია ორგანულ გამხსნელებში (ეთერი, ალკოჰოლი, ქლოროფორმი და ა.შ.) და წყალში, შესაბამისად, მისი სტაბილურობა (ორგანული ნაერთები იშლება შედარებით დაბალ ტემპერატურაზე) და რეაქციების ხასიათი; არაორგანული ნაერთებისთვის ისინი არიან იონური, მარტივი და პრაქტიკულად მყისიერი, ხოლო ორგანული ნაერთებისთვის ისინი კოვალენტური, რთული და ნელი.
ორგანული ნაერთები
ცნობილია ნახშირბადის ნაერთები ოთხმოცდაათამდე ატომის ჯაჭვებით. ჯაჭვები ნახშირბადის ატომები შეიძლება იყოს ხაზოვანი და ტოტიანი და აქვთ ერთჯერადი კოვალენტური ობლიგაციები ან აქვთ ორმაგი ან სამმაგი ობლიგაციები. ცნობილია, რომ 2500-ზე მეტი ნაერთი შეიცავს მხოლოდ ნახშირბადს და წყალბადს (ნახშირწყალბადები).
ორგანული ნაერთების იზომერია
არაორგანულ ნაერთებში, ფორმულა ზოგადად წარმოადგენს ერთ ნაერთს; ამრიგად, H ფორმულის მხოლოდ ერთი ნივთიერებაა2SW4. გოგირდმჟავას მოლეკულა შეიცავს წყალბადის ორ ატომს, ერთს გოგირდისა და ოთხს ჟანგბადს, სპეციფიკური და უნიკალური შემადგენლობით. ორგანულ ნაერთებში ეს არის იშვიათია ეს რომ მოხდეს. ამრიგად, მაგალითად, არსებობს ორი ნაერთი, რომლებიც რეაგირებენ C ფორმულაზე2ჰ6ან, ეთილის სპირტი ან ეთანოლი და დიმეთილ ეთერი.

რაც უფრო რთულია მოლეკულა, ანუ რაც უფრო მეტია ნახშირბადის ატომების რაოდენობა, მით მეტია შესაძლო იზომერების რაოდენობა.
ორგანული ნაერთების ანალიზი
ორგანული ნაერთის ანალიზი მოიცავს თვისობრივი ანალიზი, რაოდენობრივი ანალიზი და ფუნქციური ანალიზი. იმ შემთხვევაში, თუ ივარაუდება, რომ ნაერთი არის უწმინდურ მდგომარეობაში, იგი ადრე იწმინდება კრისტალიზაცია, დისტილაცია, სუბლიმაცია, მოპოვებადა ა.შ. სიწმინდის კრიტერიუმის შეფასება შესაძლებელია მისი ფიზიკური მუდმივების საფუძველზე, როგორიცაა დნობის წერტილი, დუღილის წერტილი, სიმკვრივე, ხსნადობა, კრისტალური ფორმა, რეფრაქციის ინდექსი და ა.შ.
თვისობრივი ანალიზი იგი გადამოწმებულია ნაერთის შემადგენელი ელემენტების, განსაკუთრებით ნახშირბადის, წყალბადის და აზოტის, ზოგჯერ ჰალოგენების, გოგირდისა და ფოსფორის არსებობის გამოკვლევით.
რაოდენობრივი ანალიზი იგი ხორციელდება თვისებრივი ანალიზისთვის გამოყენებული მეთოდების საფუძველზე. საწყისი წერტილი არის ნივთიერების გარკვეული რაოდენობა, რომელიც განიცდის წვას, ნახშირორჟანგი აგროვებენ და იწონიან. ნახშირბადი და წყლის ორთქლი წარმოიქმნა ნახშირბადის და წყალბადის პროცენტული გაანგარიშებისთვის რთული. რაოდენობრივი ანალიზის შედეგები ხელს უწყობს მონაცემთა გაანგარიშებას ემპირიული ფორმულა, თუმცა მოლეკულური ფორმულის პოვნა შესაძლებელია მხოლოდ ნივთიერების მოლეკულური წონის განსაზღვრის შემდეგ. მაგრამ პრობლემა ჯერ კიდევ არ არის მოგვარებული, რადგან იგივე მოლეკულური ფორმულა შეიძლება შეესაბამებოდეს სხვადასხვა იზომერებს.
ორგანული ნაერთების კლასიფიკაცია
მათი სტრუქტურის მიხედვით, ორგანული ნაერთები იყოფა ნაერთებად ალიფატური, არომატული ი ჰეტეროციკლური. ალიფატური ნაერთები დაკავშირებულია CH CH მეთანთან4, არის ღია ჯაჭვი, გარდა ციკლოპარაფინებისა, და თავიანთი სახელით ნიშნავენ იმას, რომ ცხოველური და მცენარეული ცხიმები ამ ჯგუფს მიეკუთვნება.
არომატული ნაერთები, დახურული ჯაჭვი, მჭიდროდ დაკავშირებული ბენზოლთან, C6ჰ6, და ისინი თავიანთი სახელით ვალდებული არიან იმით, რომ ბევრ მათგანს აქვს სურნელოვანი, სასიამოვნო სუნი.
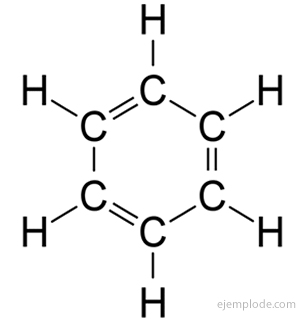
ბენზოლის ბეჭედი
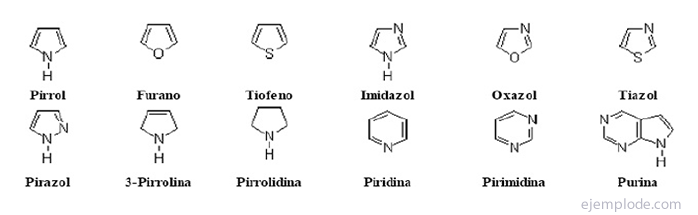
ჰეტეროციკლური ნაერთები ისინი დახურული ჯაჭვის ნაერთებია, რომელშიც ბეჭედში ნახშირბადის გარდა სხვა ელემენტია.
მათი კონსტიტუციით ისინი არიან:
ნახშირწყალბადები, რაც, თავის მხრივ, მისი ტიპის ბმულების გამო, კლასიფიცირდება როგორც ალკანები, ალკენები ი ალკინები. გარდა ამისა, ამ კატეგორიაში შედის ციკლოალკანები, ბენზოლი და მათი წარმოებულები მხოლოდ ნახშირბადის და წყალბადისგან.
ჰეტეროციკლური ნაერთები
ჰალოგენირებული წარმოებულები:R-X
ნიტრო ნაერთები:R-NO2
სულფონის მჟავები:R-SO3ჰ
ნიტრილები (ან ალკილ ციანიდები) და იზონიტრილები:R-CN და R-NC. ისინი განსხვავდებიან აზოტის ატომის შეკავშირებით მოლეკულაში.
ალკოჰოლი:R-OH
ფენოლები: ნაერთები დაფუძნებული ხერხემალზე, რომელიც შედგება ბენზოლის რგოლისაგან, დამატებული ჰიდროქსილის ჯგუფისგან.

ეთერები:რ-ო-რ
მერკაპტანები: R-SH
თიოეთერები:რ-ს-რ
თიოციდები:R-COSH
ალდეჰიდები:R-CHO
კეტონები:R-CO-R
კარბოქსილის მჟავები:R-COOH
გადიხარ:R-COOM (მ ლითონისთვის)
ეთერები: R-COO-R
ანჰიდრიდები: R-CO-O-OC-R
ამინები:R-NH2, R-NH-R, 2R-N-R
ალდოსას ტიპის ნახშირწყლები:-CHOH-CHOH-CHO
კეტოზის ტიპის ნახშირწყლები:-CHOH-CO-CH2ოჰ
ორგანომეტალური ნაერთები:რ-მ-რ
მეტალ-ალკილ ჰალიდები:R-MX (ასევე ცნობილია როგორც გრიგნარდი რეაგენტები)