알코올의 30가지 예
예 / / November 06, 2023
그만큼 알코올 ~이다 유기 화합물 구조상 탄소(-C)에 결합된 수산기 작용기(-OH)를 포함합니다. 그룹(-C – OH)을 "카르비놀"이라고 합니다. 알코올의 몇 가지 예는 다음과 같습니다. 메탄올, 에탄올 및 1-프로판올.
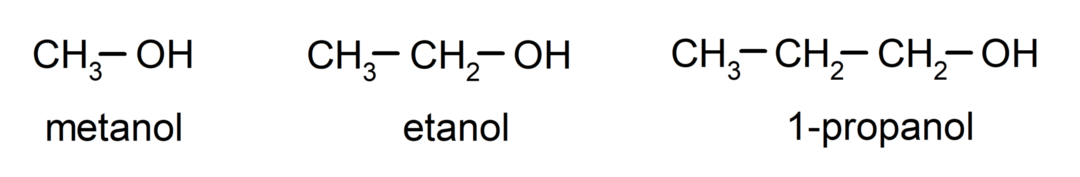
알코올은 항균, 방부 효과가 있어 일상생활에서 다양하게 활용되는 화합물입니다. 반면, 통제되지 않은 상태로 섭취하면 인체 건강에 위험할 수 있습니다.
마찬가지로 모든 알코올을 사람이 섭취할 수 있는 것은 아닙니다.
- 참조: 아민과 케톤
알코올의 종류
수산기가 부착된 탄소 원자가 부착된 탄소 원자의 수에 따라 알코올은 다음과 같을 수 있습니다.
- 1차 알코올. 하이드록실 그룹이 부착된 탄소 원자는 단일 탄소 원자에도 부착됩니다. 예를 들어:
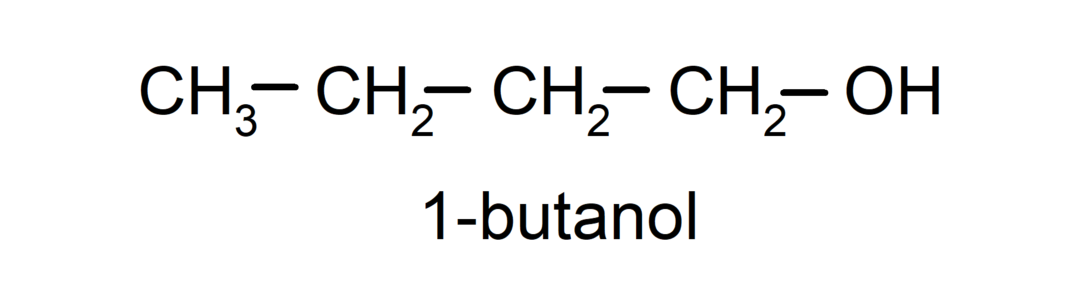
- 2차 알코올. 수산기가 부착된 탄소 원자는 두 개의 다른 탄소 원자에도 결합되어 있습니다. 예를 들어:
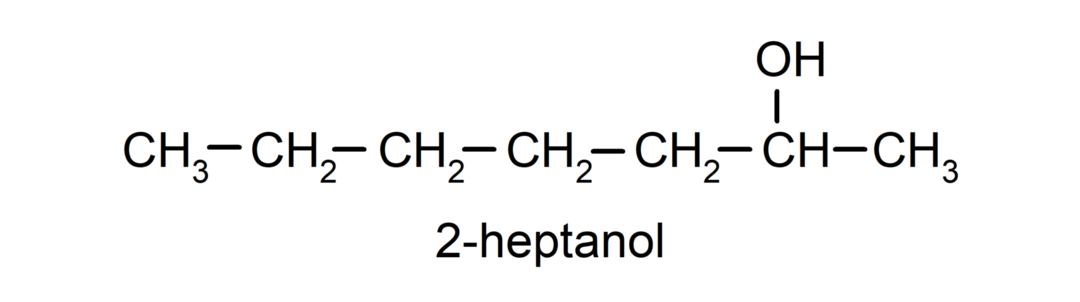
- 3차 알코올. 하이드록실 그룹이 부착된 탄소 원자는 세 개의 탄소 원자에도 부착되어 있습니다. 예를 들어:
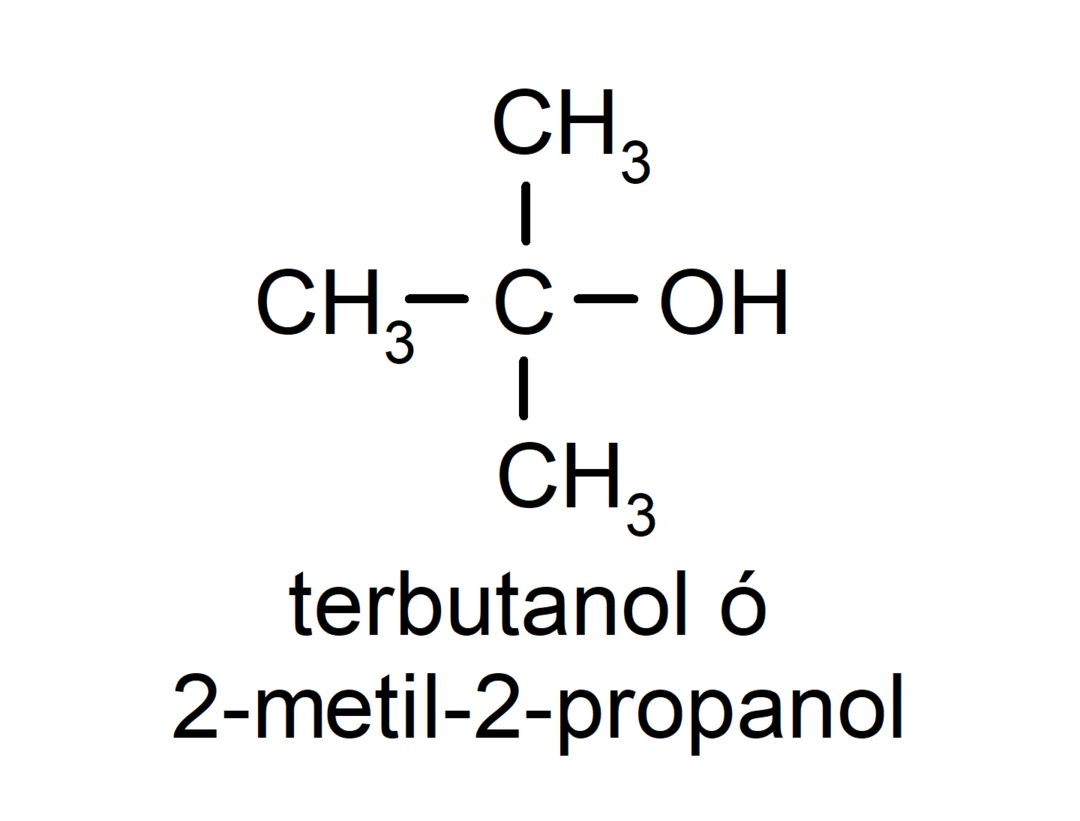
알코올은 수산기 수에 따라 다음과 같은 특성을 가질 수 있습니다.
- 디올. 구조에는 두 개의 수산기가 있습니다. 예를 들어:
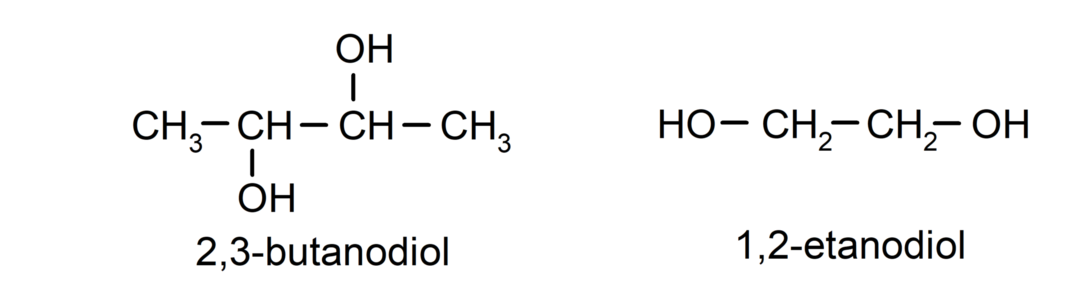
- 트리올. 구조에는 3개의 수산기가 있습니다. 예를 들어:
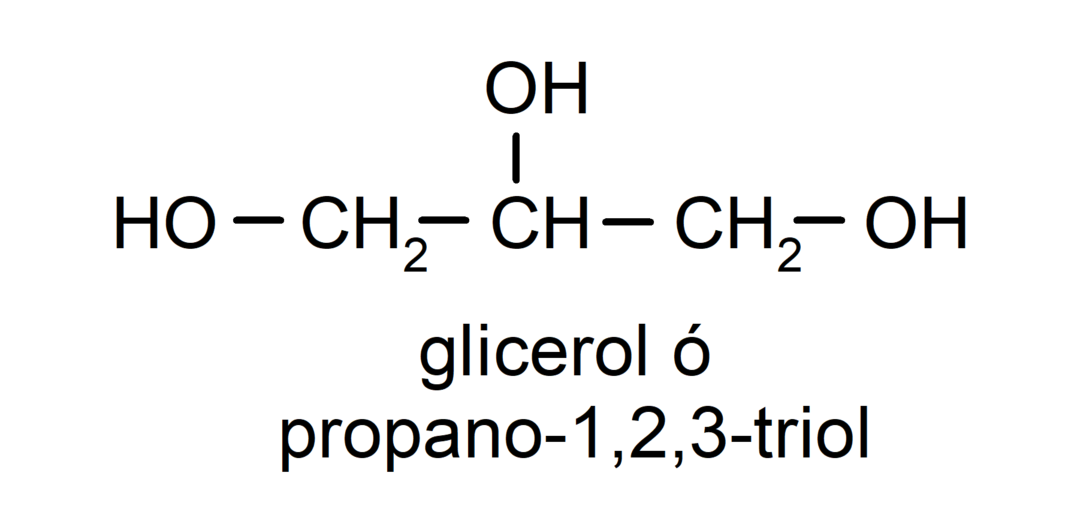
- 폴리알코올. 구조에는 많은 수산기가 있습니다. 예를 들어:
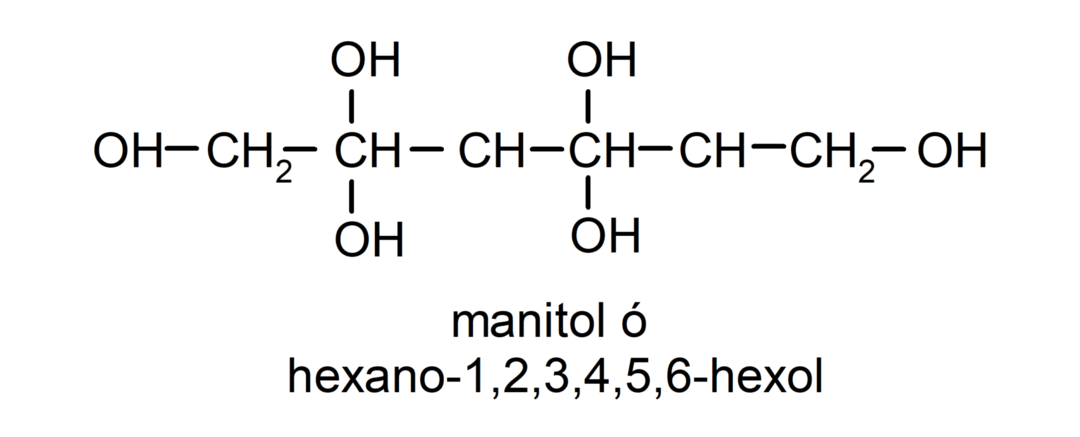
알코올의 물리적 특성
알코올의 물리적 특성 중 일부는 다음과 같습니다.
- 비점. 알코올의 끓는점은 수소 결합을 형성할 수 있는 수산기의 존재로 인해 상당히 높습니다. 또한, 탄소 사슬에 하이드록실 작용기가 더 많이 존재할수록, 비점 알코올의.
- 극성. 알코올은 극성이 매우 강한 화합물입니다.
- 용해도. 저분자량 알코올은 물에 용해됩니다. 반면, 알코올의 탄소 사슬이 클수록 물에 대한 용해도는 낮아집니다. 또한, 알코올의 수산기 그룹이 많을수록 물에 대한 용해도는 더 커집니다.
- 집계 상태. 대부분의 알코올은 실온(25°C)에서 액체이며 특유의 냄새가 있습니다.
알코올의 화학적 성질
알코올의 화학적 특성 중 일부는 다음과 같습니다.
- 알코올은 산과 염기처럼 행동합니다.. 산으로서의 이들의 거동은 활성 금속과의 반응에서 수소 가스를 방출하고 알콕사이드를 형성하는 것으로 볼 수 있습니다.

염기로서의 이들의 거동은 메틸옥소늄 브로마이드를 형성하기 위한 메탄올과 브롬화수소의 반응과 같은 반응에서 볼 수 있습니다.
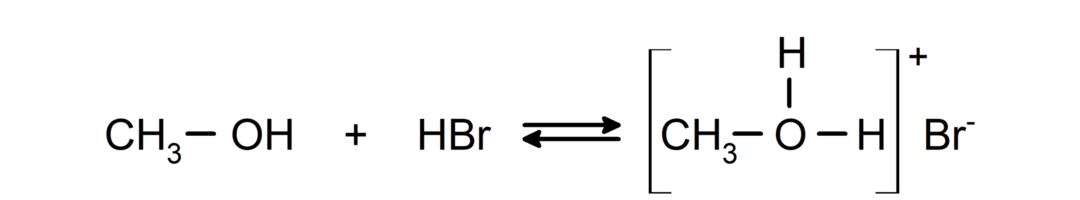
- 알코올은 할로겐화 반응을 겪습니다.. 할로겐화수소와 반응하여 할로겐화 알킬을 형성합니다.
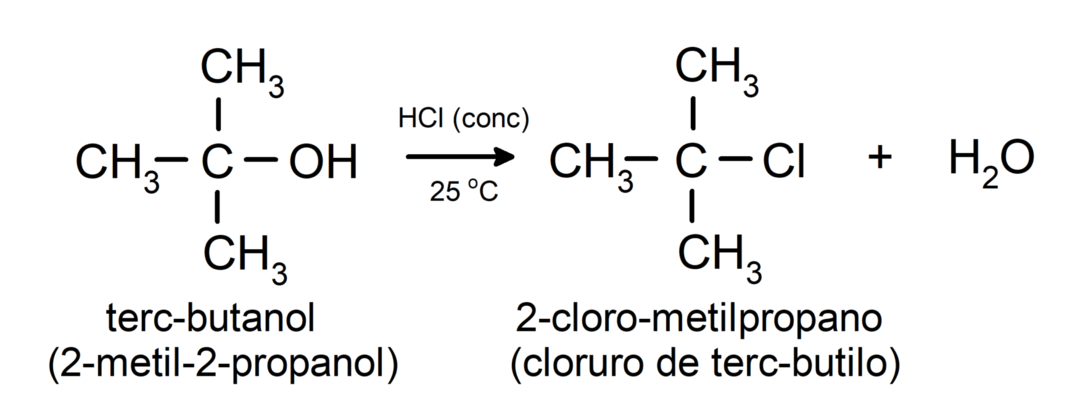
-
알코올은 산화 반응을 겪습니다. 특정 산화 화합물과 반응할 때. 산화 반응의 생성물은 반응하는 알코올의 유형, 즉 1차, 2차 또는 3차 알코올에 따라 달라집니다.
1차 알코올을 산화하여 알데히드 또는 카르복실산을 형성합니다.
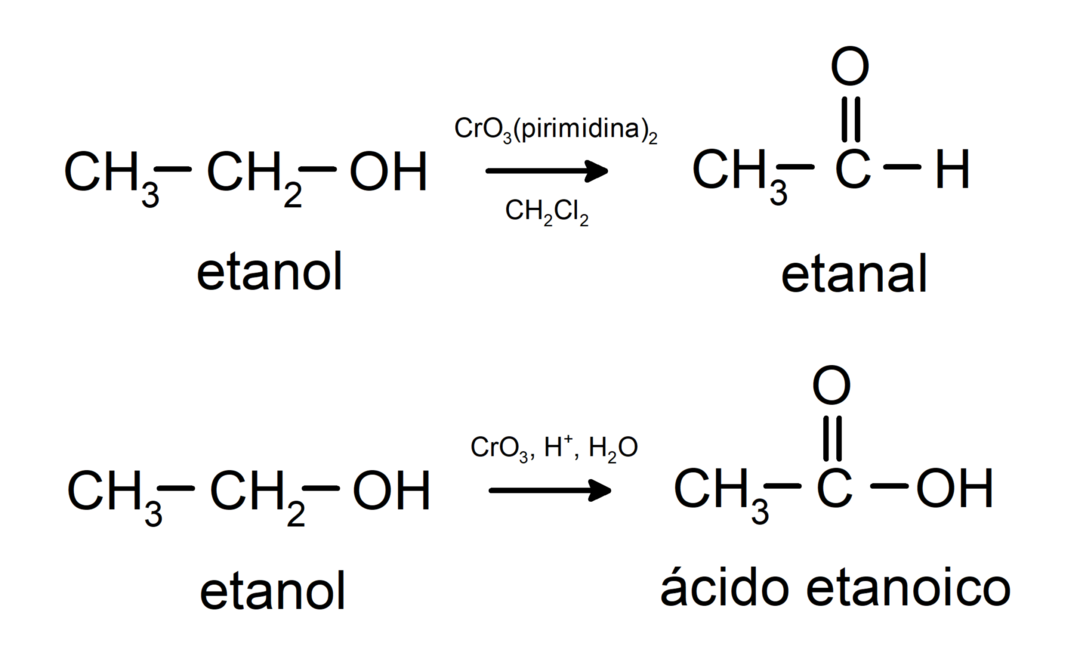
2차 알코올을 산화시켜 케톤을 형성합니다.
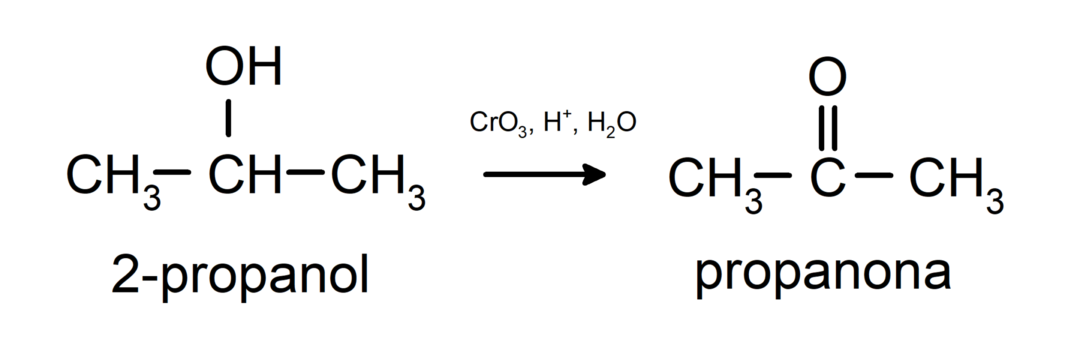
3차 알코올은 일반적인 산화제와 산화되지 않습니다. 매우 강한 산화제를 사용하면 알켄으로 변환되어 산화될 수 있습니다.
인접한 탄소에 두 개의 수산기를 갖는 알코올은 사아세트산납으로 산화되어 두 개의 케톤을 형성합니다.
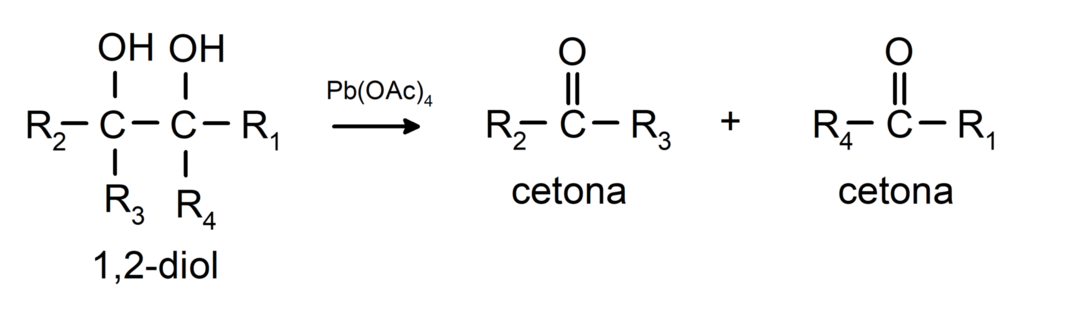
- 알코올은 탈수소화 반응을 겪습니다.. 이러한 반응은 1차 및 2차 알코올에서만 발생하며, 촉매 존재 하에 고온에 노출되면 수소를 방출합니다.
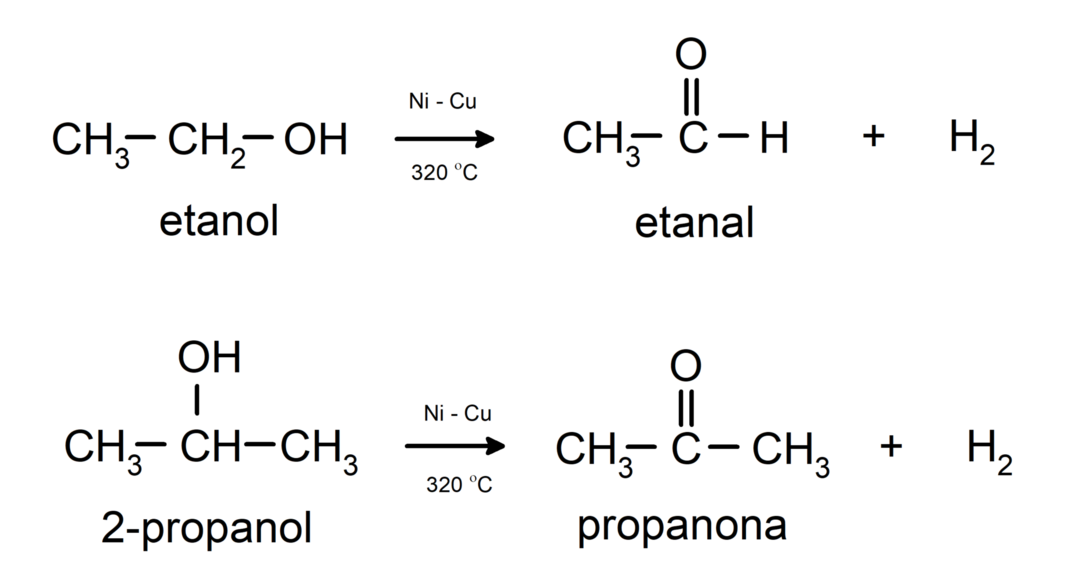
- 알코올은 탈수 반응을 겪습니다.. 알코올은 탈수되어 상응하는 알켄을 형성합니다. 이 반응은 산과 중간 온도에서 발생합니다.
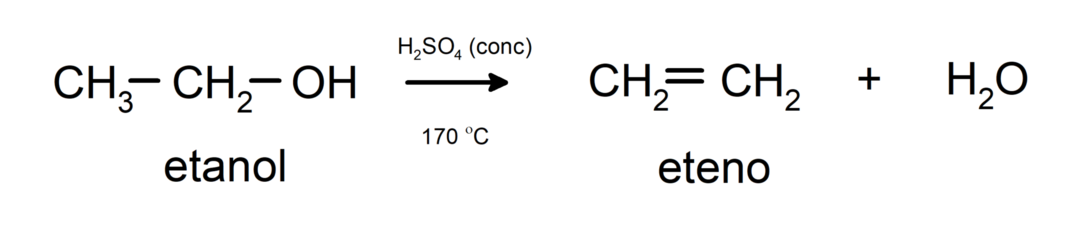
알코올 명명법
IUPAC(국제 순수 및 응용 화학 연합)이 정한 명명법에 따르면 알코올의 이름은 다음 규칙에 따라 지정됩니다.
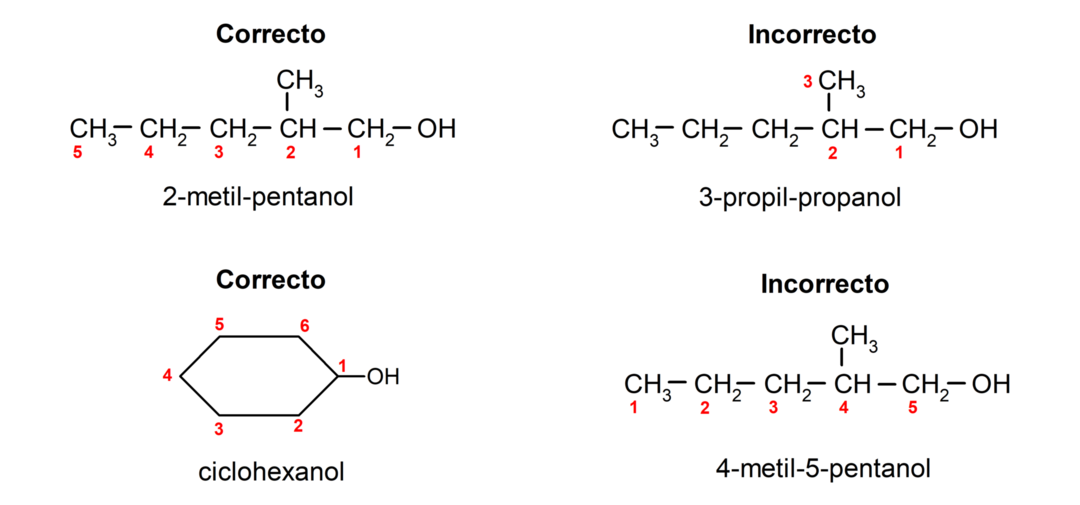
- 수산기의 위치는 탄소 사슬에서 가능한 가장 낮은 수를 차지한다는 점을 고려하여 선택됩니다. 알코올의 구조가 고리형인 경우, 수산기가 부착된 탄소의 1번 위치를 고려하여 접두사 cyclo-를 사용하여 이름을 지정합니다.
- 알코올의 이름은 탄소 사슬의 원자 수를 나타내는 접두사를 사용하고 접미사 -ol을 붙입니다.
- 알코올의 구조에 가지가 있는 경우 수산기를 포함하는 가장 긴 사슬이 주 탄소 사슬로 선택됩니다.
전통 명명법에 따르면 알코올의 이름은 "alcohol"이라는 단어를 쓴 다음 알코올의 이름을 써서 명명됩니다. 탄소 사슬에 해당하는 알칸, 그러나 알칸의 어미 -ane을 사용하는 대신, 어미 -일릭.
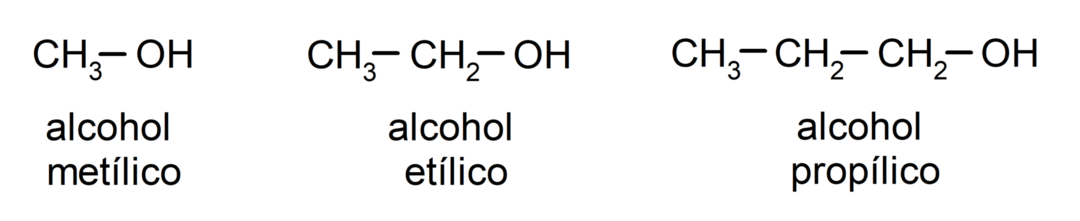
알코올의 예
- 메탄올
- 에탄올
- 1-프로판올
- 2-프로판올
- 1-부탄올
- 3-에틸헥산-2-올
- 글리세린
- 페놀
- 2-메틸-2-부탄올
- 1,2-에탄디올
- 1,5-헵타디엔-3-올
- 3-메틸-2-부탄올
- 벤질메탄올
- 3-펜탄올
- 2-메틸페놀
- 1,2-디히드록시페놀
- 사이클로헥스놀
- 1-페닐에탄올


알코올의 용도
알코올의 가장 일반적인 용도는 다음과 같습니다.
- 일부 세균의 성장을 멈추기 때문에 소독제와 방부제로 사용됩니다. 미생물 아니면 파괴하세요. 이러한 목적으로 에탄올과 이소프로필 알코올이 가장 많이 사용됩니다.
- 그들은 다양한 합성에 사용됩니다 화학물질. 예를 들어, 메탄올은 메탄알(포름알데히드)을 얻는 데 사용됩니다.
- 그들은 부동액을 생산하는 데 사용됩니다. 메탄올은 이러한 목적으로 가장 많이 사용되는 것 중 하나입니다.
- 이들은 제약 산업에서 용매로 사용됩니다. 에탄올은 이러한 의미에서 가장 많이 사용되는 것 중 하나입니다.
- 이들은 래커, 염료 및 잉크의 용매로 사용됩니다. 메탄올은 이러한 목적으로 널리 사용됩니다.
- 이들은 연료로 사용되며 부분적으로 연료 사용을 대체하는 중요한 경향이 있습니다. 화석 연료 바이오에탄올 연료를 사용하여
- 그들은 수지를 만드는 데 사용됩니다. 페놀은 이런 의미로 사용됩니다.
알코올 소비의 위험성
오늘날 알코올 소비는 사회적으로 용인되지만, 이 물질을 남용하면 의존성과 중독이 발생합니다.
에탄올은 알코올 음료에 존재하는 알코올로, 과도하게 섭취하면 영향을 미칩니다. 인지능력 저하로 심혈관 질환, 간경화, 암.
또한, 알코올 중독 정도, 즉 취한 상태에 이르렀을 때, 알코올 농도가 너무 높으면 알코올성 혼수상태가 발생하여 호흡 마비가 발생하고 심지어 사망에 이를 수도 있습니다. 죽음.
참고자료
- 티. 에게. 가이스만. (1974) "유기화학의 원리" 제2판. 편집 Reverté, S.A. ISBN: 8429171800
- 아후마다-코르테스, J. G., 가메즈-메디나, M. E., & 발데스-몬테로, C. (2017). 공중 보건 문제로서의 알코올 소비. 라심하이, 13(2), 13-24.
- 모리슨, R. T., & 보이드, R. N. (1998). 유기화학. 피어슨 교육.
- 웨닝거, S. J., & 스터미츠, F. 아르 자형. (1988). 유기화학. 나는 반대했다.
다음을 따르세요:
- 에틸 알코올
- 연료
- 유기화학