Charles의 법칙의 예
물리학 / / July 04, 2021
Charles의 가스 법칙 또는 일정한 압력의 법칙은 가스 법칙 중 하나입니다. Jacques Charles의 작품을 알려준 Gay-Lussac에 의해 발표 됨. 몇 년 전에.
Charles의 법칙은 압력이 일정하게 유지되고 온도와 부피가 변할 때 기체 질량의 거동을 예측합니다.
Charles의 법칙은 다음과 같이 명시됩니다.
일정한 압력에서 기체의 부피는 온도 변화에 정비례합니다.
일정한 압력: 가스가 컨테이너 벽에 가하는 압력이 경험 내내 변하지 않는다는 사실을 의미합니다.
음량: 가스가 차지하는 점유 공간으로 일반적으로 벽이 변형되지 않고 뚜껑이 플런저처럼 작동하는 용기로 간주됩니다.
온도: 실험 중에 가스가 겪는 열의 증가 또는 손실입니다. 온도가 상승하면 부피가 증가합니다. 온도가 감소하면 부피도 감소합니다.
대수적으로 Charles의 법칙은 다음 공식으로 표현됩니다.

어디:
V = 가스 부피
T = 가스 온도
k = 해당 기체 질량에 대한 비례 상수.
이것은 일정한 압력에서 주어진 가스 질량에 대해 부피와 가스 사이의 관계를 의미합니다. 온도 변화는 항상 동일한 비례 관계를 가지며 상수로 표현됩니다. 케이:

따라서 상수가 결정되면 다른 알려진 데이터에서 다른 값을 계산할 수 있습니다.
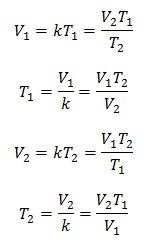
3 문제에 적용된 Charles의 법칙의 예 :
예 1: 용기에 280K의 온도에서 1.3 리터의 부피를 차지하는 가스 질량이있는 경우 새 부피를 계산합니다. 303K의 온도에 도달했을 때 부피를 계산하십시오.
V1 = 1.3 리터.
티1 = 280K
V2 = ?
티2 = 303K
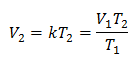
값 대체 :
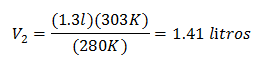
303K의 새 볼륨은 1.41 리터입니다.
예 2. 섭씨 10도에서 2.4 리터를 차지하는 가스가 있다면 최종 온도가 2.15 리터를 차지하면 최종 온도를 계산하십시오.
V1 = 2.4 리터
티1 = 10 ° C = 283K
V2 = 2.15 리터
티2 = ?
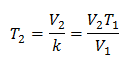
값 대체 :
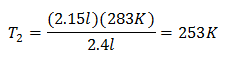
새로운 온도는 253K로 -20 ° C와 같습니다.
예제 3. 초기 온도가 328K이고 최종 부피가 3.75 l이고 비율 상수가 0.00885 인 가스가 있습니다.
V1 = ?
티1 = 328K
V2 = 3.75 리터
티2 = ?
k = 0.00885
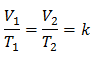
값 대체 :
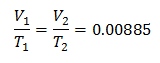
초기 볼륨을 확인하려면 :
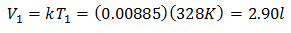
초기 부피는 2.90 l입니다.
최종 온도를 확인하려면 :
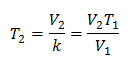
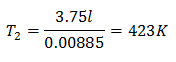
최종 온도는 423K로 150 ° C와 같습니다.



