20 Rūgščių druskų pavyzdžiai
Įvairios / / July 04, 2021
Viduje konors neorganinė chemija druskos vadinamos junginiais, kurie gaunami, kai a rūgštis jo vandenilio atomai pakeičiami metaliniais katijonais (nors kartais ir nemetaliniais katijonais, pavyzdžiui, amonio katijonu, NH4+). Konkrečiu atveju rūgštinės druskos, rūgšties vandeniliai yra iš dalies pakeisti, tai yra druskos dalimi lieka bent vienas nepakeistas vandenilis. Tuo jie skiriasi nuo neutralios druskos, kur rūgšties vandeniliai yra visiškai pakeisti.
The Tu išeini paprastai susidaro vykstant reakcijai tarp a rūgštis ir a hidroksidas (bazė). Šiose reakcijose bazė paprastai praranda hidroksilo grupes (-OH), o rūgštis - jas. atomai vandenilis (H), sudarantis neutralią druską; bet jei nagrinėjama rūgštis išsaugo bent vieną iš savo vandenilio atomų, pakeisdama reakcijos elektrinį krūvį, gausime rūgščią druską arba hidrintą druską.
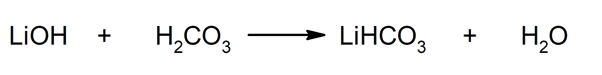
Taigi, pavyzdžiui, ličio bikarbonatas ir vanduo gaunami reakcijoje tarp ličio hidroksido ir anglies rūgšties:
Rūgščių druskų nomenklatūra
Rūgštines druskas galima pavadinti pagal trijų tipų dažniausiai naudojama nomenklatūra:
Rūgščių druskų pavyzdžiai
- Natrio bikarbonatas (NaHCO3). Taip pat vadinamas natrio vandenilio karbonatu (IV), jis yra balta kristalinė kieta medžiaga, tirpi vandenyje, kurios gamtoje gali būti mineralinis arba jis gali būti gaminamas laboratorijoje. Tai yra viena iš geriausiai žinomų rūgščių druskų ir yra plačiai naudojama konditerijos gaminiuose, farmakologijoje ar jogurto gamyboje.
- Ličio bikarbonatas (LiHCO3). Ši rūgšties druska buvo naudojama kaip CO sulaikanti priemonė2 situacijose, kai tokios dujos yra nepageidaujamos, kaip Šiaurės Amerikos „Apollo“ kosminėse misijose.
- Kalio divandenilio fosfatas (KH2PO4). Tai yra kristalinė kieta medžiaga, bekvapė, tirpi vandenyje, plačiai naudojama įvairiose pramonės šakose, tokiose kaip mielės maistas, chelatinis agentas, maistinis stipriklis ir fermentacijos procesų padėjėjas.
- Natrio bisulfatas (NaHSO4). Tai rūgšties druska, susidaranti neutralizuojant sieros rūgštį. Pramoniniu būdu jis plačiai naudojamas metalų ir valymo produktų valymui. Nors jis yra labai toksiškas kai kuriems dygiaodžiams, jis naudojamas kaip priedas naminių gyvūnėlių ėdalui ir papuošalų gamybai.
- Natrio vandenilio sulfidas (NaHS). Tai pavojingas junginys, kurį galima tvarkyti, nes jis yra labai ėsdinantis ir toksiškas. Tai gali sukelti sunkius odos nudegimus ir akių pažeidimus, nes taip pat yra degūs.
- Kalcio vandenilio fosfatas (CaHPO4). Jis naudojamas kaip maisto papildas javai galvijams. Tai yra vandenyje netirpi kieta medžiaga, bet hidratuota, galėdama kristalizuotis, suvartodama du molekulės vandens.
- Amonio vandenilio karbonatas ([NH4] HCO3). Taip pat žinomas kaip „amonio bikarbonatas“, jis naudojamas maisto pramonėje kaip mielės chemikalas, nors jo trūkumas yra sulaikyti amoniaką ir suteikti maistui blogą skonį, jei jis naudojamas perteklius. Jis taip pat naudojamas gesintuvuose, gaminant pigmentus ir plečiant gumą.
- Bario bikarbonatasarba (Ba [HCO3]2). Tai rūgštinė druska, kuri kaitinant gali pakeisti gamybos reakciją ir yra labai nestabili, išskyrus tirpalą. Jis plačiai naudojamas keramikos pramonėje.
- Natrio bisulfitas (NaHSO3). Ši druska yra labai nestabili ir esant deguoniui ji virsta natrio sulfatu (Na2SW4), todėl jis naudojamas maisto pramonėje kaip maisto konservantas ir sausiklis. Tai yra ypatingai redukuojanti medžiaga, dažniausiai naudojama žmogaus, taip pat naudojama tvirtinant spalvas.
- Kalcio citratas (AC3[C6H5ARBA7]2). Paprastai žinoma kaip karčioji druska, ji naudojama kaip maisto konservantas ir kaip maisto papildas, kai ji yra susijusi su amino rūgštimi lizinu. Tai balti bekvapiai kristaliniai milteliai.
- Monokalcio fosfatas (Ca [H2PO4]2). Tai yra bespalvė kieta medžiaga, gaunama reaguojant į kalcio hidroksidą ir fosforo rūgštį, plačiai naudojama kaip raugas arba kaip trąša žemės ūkio darbuose.
- Dikalcio fosfatas (CaHPO4). Taip pat žinomas kaip kalcio monohidrogenfosfatas, jis turi tris skirtingas kristalines formas, kurios naudojamos kaip maisto priedas ir yra dantų pastose. Be to, jis natūraliai susidaro inkstų akmenyse ir vadinamajame „inkstų akmenyje“.
- Monomagnio fosfatas (MgH4P2ARBA8). Tai balta, kristalinė ir bekvapė druska, iš dalies tirpi vandenyje. Jis naudojamas maistui konservuoti, kaip rūgštiklis, kaip rūgštingumo koregatorius arba agentas gydant miltus.
- Natrio diacetatas (NaH [C2H3ARBA2]2). Ši druska yra naudojama kaip kvapiosios ir konservuojančios medžiagos valgant, o tai užkerta kelią arba atitolina jos atsiradimą grybai ir mikobakterijos - tiek vakuume supakuotuose produktuose, kaip mėsos gaminiai, tiek miltų pramonėje.
- Kalcio bikarbonatas (Ca [HCO3]2). Tai yra hidrinta druska, gaunama iš kalcio karbonato, kurio yra mineraluose, tokiuose kaip kalkakmenis, marmuras ir kt. Ši reakcija apima vandens ir CO buvimą2, todėl savaime gali atsirasti urvuose ir urvuose, kuriuose gausu kalcio.
- Rubidžio rūgšties fluoridas (RbHF). Ši druska gaunama reaguojant vandenilio fluorido rūgščiai (vandeniliui ir fluorui) ir šarminio metalo rubidiui. Rezultatas yra toksinis ir ėsdinantis junginys, su kuriuo reikia elgtis atsargiai.
- Monoamonio fosfatas ([NH4] H2PO4). Tai vandenyje tirpi druska, gaunama reaguojant amoniakui ir fosforo rūgščiai. Paprastai jis naudojamas kaip trąša, nes jis suteikia dirvožemiui maistinių medžiagų azoto ir fosforo, būtino augalų augimui. Tai taip pat yra ABC miltelių dalis gesintuvuose.
- Cinko vandenilis ortoboratas (Zn [HBO3]). Tai druska, naudojama kaip antiseptikas ir kaip priedas keramikos gamybai.
- Natrio fosfatas (NaH2PO4). Jis dažniausiai naudojamas laboratorijose kaip „buferinis“ arba buferinis tirpalas, kuris apsaugo nuo staigių tirpalo pH pokyčių.
- Kalio vandenilio ftalatas (KHP). Taip pat vadinamas "kalio rūgšties ftalatu", tai yra kieta ir stabili druska įprastame ore, todėl ji dažnai naudojama kaip pagrindinis etalonas matuojant pH. Jis taip pat naudingas kaip buferio agentas cheminės reakcijos.
Sekite su:
