20 Rūgščių pavyzdžiai
Įvairios / / July 04, 2021
The rūgštys sudaro svarbią grupę cheminiai junginiai, labai platus. Rūgštys paprastai apibrėžiamos kaip junginiai, galintys paaukoti vieną ar daugiau katijonai vandenilis (H+) į kitą junginį, žinomą kaip bazė. Nors iš tikrųjų rūgštys apibrėžiamos pagal kelias teorijas:
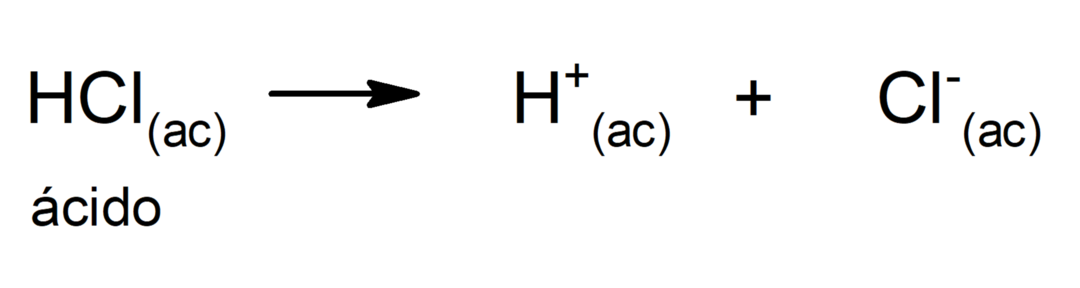 Šios teorijos apribojimas yra tas, kad rūgštys yra apibrėžtos tik vandeniniame tirpale.
Šios teorijos apribojimas yra tas, kad rūgštys yra apibrėžtos tik vandeniniame tirpale. 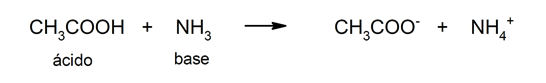

Išleidimo turtas vandenilio katijonai yra tai, dėl ko rūgštys gamina pH mažiau nei 7. Rūgštys, galinčios išskirti daugiau nei vieną protoną (naudojant šį pavadinimą H+) vadinamos poliprotinėmis arba daugiafunkcinėmis.
Rūgštinės savybės
Dėl jų savybes, rūgštys gali būti pateikiamos kaip skysčiai arba kaip dujos, rečiau kaip kietas. Rūgštinį skonį, kurį galime atpažinti ir kuris apibūdina šiuos junginius, randame, pavyzdžiui, citrusinių vaisių, kuriuose gausu citrinos rūgšties, arba acto, kuris yra rūgšties tirpalas acto. Tai yra organinės rūgštys.
egzistuoti organinės ir neorganinės rūgštys; stipriausi dažniausiai yra neorganiniai. Daugelis organinių rūgščių atlieka svarbų biologinį vaidmenį. Tarp neorganinių yra viena, druskos rūgštis, kuri vaidina labai svarbų vaidmenį virškinimo procese. The
nukleorūgštys Jie taip pat yra gyvybiškai svarbūs, nes yra genetinės medžiagos pagrindas ląstelių ir joje yra raktas į sintezę baltymas.Polinkis prarasti protonus lemia rūgšties stiprumą.
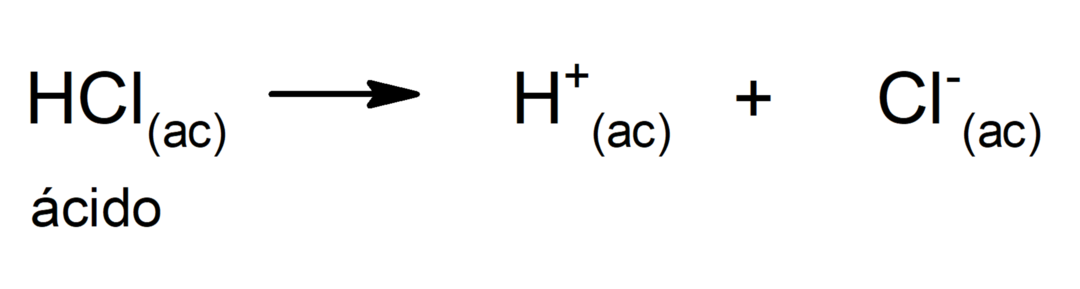
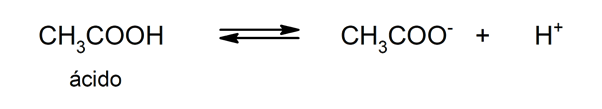
Rūgščių naudojimas
Rūgštys turi daugybė naudojimo būdų, tiek pramoniniu, tiek namų mastu. Jie dažnai naudojami kaip priedai ir konservantai maistas, kosmetika, gėrimai ir kt. Kai kurios rūgštinės kietosios medžiagos yra naudojamos kaip katalizatoriai (cheminių reakcijų greitintuvai) naftos chemijos ar popieriaus pramonėje.
Taip pat yra rūgščių, kurios naudojamos kaip dezinfekavimo priemonės (karbolio rūgštis, salicilo rūgštis). Be to, jie gali būti naudojami kaip elektrolitai automobilio akumuliatoriuose, kaip yra sieros rūgšties atveju. Pastaroji stiprioji rūgštis taip pat dažnai naudojama perdirbant mineralai, taip yra trąšų gamybai iš akmens fosfatų.
Verta paaiškinti, kad tam tikras medžiagas galima ištirpinti tik rūgštinėse terpėse, o tam tikros reakcijos vyksta tik tokiomis sąlygomis. Azoto rūgštis ir amoniakas sudaro amonio nitratą, kuris taip pat yra svarbus pasėlių trąša.
Rūgščių pavyzdžiai
Toliau pateikiamas pavyzdys: dvidešimt rūgščių:
- Perchloro rūgštis (HClO4). Tai stiprus rūgštus skystis a temperatūra aplinka, labai oksiduojantis.
- Azoto rūgštis (HNO3). Tai stipri ir intensyviai oksiduojanti rūgštis, naudojama tam tikroms sprogmenims ir azoto trąšoms gaminti.
- Askorbo rūgštis (C.6H8ARBA6). Tai vitaminas C, toks reikalingas sveikatai. Tai yra antioksidacinio poveikio apsauginė medžiaga.
- Druskos rūgštis (HClac)). Tai yra vienintelė stiprioji rūgštis, kurią sintetina žmogaus organizmas. Šis procesas vyksta skrandyje, siekiant maistas virškinimo procese.
- Vyno rūgštis (C.4H6ARBA6). Tai balti kristaliniai milteliai, jie naudojami gaminant putojančius gėrimus, kepyklų, vyno ir farmacijos pramonėje. Kai kurių receptų turimas dantų akmenų kremas yra vyno rūgštis.
- Fluorūgšties rūgštis (HFac)). Dėl savo sugebėjimo užpulti stiklą jis naudojamas drožiant ir graviruojant.
- Sieros rūgštis (H2SW4). Tai yra stipri rūgštis, nes ji yra daugybė įvairiausių pramonės šakose ir sintezės procesai.
- Trifluoracto rūgštis (C.2HF3ARBA2). Tai yra geras tirpiklis daugeliui organiniai junginiai.
- Fosforo rūgštis (H3PO4). Jo yra (mažomis koncentracijomis) įvairiuose kolos gėrimuose. Tai laikoma kenksminga sveikatai, nes skatina nukalkėjimą.
- Acto rūgštis (CH3COOH). Tai yra pagrindinis acto komponentas. Dėl jo sukurto rūgštingumo jis yra plačiai naudojamas maisto konservantas.
- Fluorantimono rūgštis (SbHF6). Tai stipriausias žinomas superrūgštis, viršijantis grynos sieros rūgšties rūgštingumą 1019.
- Chromo rūgštis (H2CrO4). Tai tamsiai raudoni milteliai, jie dalyvauja chromo dengimo procese. Jis taip pat naudojamas glazūruoti keramiką.
- Indolacto rūgštis (C.10H9NE2). Tai pagrindinis auksinų, svarbių augimo hormonų, atstovas augalų.
- Dezoksiribonukleino rūgštis (DNR). Tai yra tas, kuris turi gyvenimo raktą, nes jis sudaro genus, kurie valdo daugybės baltymų sintezę.
- Trikarboksirūgštys. Jie apima karboksirūgščių grupę, turinčią tris karboksirūgštis (-COOH). Citrinų rūgštis (C.6H8ARBA7) Tai vienas iš jų.
- Skruzdžių rūgštis (CH2ARBA2). Tai paprasčiausia iš organinių rūgščių. Ilgalaikis šios rūgšties poveikis gali sukelti kvėpavimo nepakankamumą ir mirtį.
- Gliukono rūgštis (C.6H12ARBA7). Šios rūgšties druskos plačiai naudojamos stiklo dirbinių valymo procesuose.
- Pieno rūgštis (C.3H6ARBA3). Tai svarbi biocheminių procesų dalis.
- Benzenkarboksirūgštis (C.7H6ARBA2). Tai yra būdingo kvapo rūgštis, plačiai naudojama norint išsaugoti maisto produktus, kuriems reikalingas a pH rūgštis.
- Obuolių rūgštis (C.4H6ARBA5). Jis plačiai naudojamas farmacijos pramonėje gaminant vidurius.
- Anglies rūgštis (H2CO3). Kai kuriose vietose tai yra urvų formavimosi dalis. Jo yra gazuotuose gėrimuose.

