Tūrinės analizės pavyzdys
Chemija / / July 04, 2021
Įjungta Analitinė chemija, Tūris yra analizės metodas, kurį sudaro Reagento, reikalingo stechiometriškai reaguoti su analitu, tūrio matavimas, kuri yra medžiaga, kurią reikia nustatyti.
Reaguokite stechiometriškai nurodo chemines medžiagas, sąveikaujančias chemikalais, teigia proporcija, žyminti cheminę lygtį jau subalansuotas.
Tiriama medžiaga vadinama Analitė. Iš šios medžiagos bus imamas žinomas ir tiksliai išmatuotas tūris, kurį mes pavadinsime Alikvotinė dalis, esančią Erlenmeyerio kolboje, kad būtų galima pradėti analizę.
Tūrinės analizės sampratos
Tūrinė analizė, būdama Cheminė analizė, nešiotis įvyko cheminė reakcija. Ši cheminė reakcija bus vykdoma tarp mėginio su nežinomu tiriamos medžiagos kiekiu ir žinomu kitos medžiagos kiekiu, galinčiu reaguoti su pirmuoju.
Reakcijos medžiagos bus vandeniniame tirpaleir bus išmatuoti tirpalų, kurie sąveikauja iki reakcijos pabaigos, tūriai, kurie bus matomi indikatoriaus, kuris kolbos viduje suteiks spalvą, dėka.
Atliekant tūrinę analizę, vandeninis
Žinoma koncentracija vadinama standartiniu sprendimu, Standartinis arba „Titrant“ir bus naudojamas kaip nuoroda baigiant reakciją, kad būtų galima atlikti skaičiavimą, kuris atskleistų tiriamos medžiagos kiekį.Vadinama ši abiejų sprendimų reakcijos procedūra Cheminis laipsnis o Vertinimas, kuris yra pagrindinė tūrinės analizės dalis. Susideda iš ėjimo palaipsniui pilant standartinį tirpalą (Titrantas) alikvotinėje dalyje (Pavyzdys), kol indikatorius rodo pokyčius su spalvų skirtumu.
A Rodiklis Tai yra cheminė medžiaga, kuri pridedama prie alikvoto, rodanti spalvą ir kuri, pasibaigus reakcijai, pakeis spalvą.
Tūrinė analizė susideda iš paprastos veiksmų sekos:
1.- Standartinio tirpalo paruošimas
2.- Mėginio arba alikvoto paruošimas
3.- Cheminis laipsnis
4.- Tūrio matavimas
5. - Tiriamos medžiagos apskaičiavimas.
Iki to taško, kur jie jau turi visiškai sureagavo dviejų medžiagų, jis vadinamas Ekvivalentiškumo taškas.
Kaip ir bet kuriame kitame cheminiame analizės metode, tūrio analizėje yra gerų rezultatų reikalavimai:
- Cheminė reakcija turi būti Atrankinis, tai yra, etaloninis tirpalas reaguos tik su mėginiu.
- Cheminė reakcija turi būti Stechiometrinė, tai yra, paklusti proporcijoms, pažymėtoms subalansuotoje cheminėje lygtyje.
- Cheminė reakcija turi būti Kiekybinis; reiškia 99,9% baigtį ekvivalentiškumo taške.
-Turi būti a nustatomas galutinis reakcijos taškas, kurį geriau patvirtins rodiklis.
Pirminis raštas
Pirminiai modeliai Tai labai grynos medžiagos, kurių koncentracija tirpale apskaičiuojama tiesiogiai iš pasverto kiekio ir sunaudoto vandens.
A) Taip, galima reaguoti su darbiniais tirpalais, žinoti pastarųjų koncentracijas ir paversti jas standartiniais tirpalais.
Pagrindinių modelių pavyzdžiai:
- Natrio karbonatas (Na2CO3): Naudojamas rūgštims, tokioms kaip sieros rūgštis, standartizuoti.
-Kalio biftalatas: Pirminis standartas yra paruošti bazinius tirpalus, tokius kaip natrio hidroksidas.
-Natrio chloridas (NaCl): jis naudojamas sidabro nitrato tirpalams standartizuoti.
-Kalcio karbonatas (CaCO3): Pirminis EDTA (etileno Diamino tetraacto rūgšties) standartas.
Pirminis raštas turi atitikti keletą pagrindinių savybių:
Turi turėti Labai grynas, Atmosferos stabilumas, Hidratacinio vandens nėra, Maža kaina ir lengva gauti, Y Didelis ekvivalentinis svoris.
Tūrinės analizės klasifikacija
Priklausomai nuo cheminių rūšių, su kuriomis naudojama analizė, tai bus tūrio tipas:
Rūgščių ir šarmų tūris: Analizuoti mėginius, kuriuose yra rūgščių arba bazių, veikia su rūgštimi arba su baze.
Kritulių tūris: Taip pat vadinamas argentometrija, jis naudoja standartinį sidabro nitrato tirpalą, kad nustatytų, kiek chloridų yra mėginyje.
Sudėtingumo tūris: Kietumo, ty kalcio ir magnio karbonatų koncentracijai vandenyje matuoti, naudojamas standartinis kompleksą sudarančio agento, pvz., EDTA, tirpalas.
REDOX tūris: Reakcija vyksta tarp oksiduojančios ir redukuojančios medžiagos.
Rodikliai
Iš daugybės „Volumetrics“ naudojamų rodiklių išsiskiria trys:
1.- Metilo apelsinas: Alikvotinėje dalyje reikia oranžinės spalvos, kuri bus titruojama rūgštimi. Pasiekus ekvivalentiškumo tašką, indikatorius taps geltonas.
2.- Fenolftaleinas: Pradžioje jis yra skaidrus alikvotinėje dalyje, kuri bus pavadinta pagrindu. Pasiekus ekvivalentiškumo tašką, indikatorius taps rausvas.
3.- Eriochromo juoda: Tai rodiklis, naudojamas kietumui vandenyje nustatyti. Iš pradžių alikvotinėje dalyje ji yra purpurinė, kol ji titruojama kompleksą sudarančia medžiaga. Reakcijos pabaigoje ji tampa mėlyna.

Instrumentai tūrinėje analizėje
Atliekant tūrinę analizę, bus naudojama keletas priemonių, kurių, jei jų nėra, negalima tinkamai sukurti:
1.- Tūrinė kolba: tai indas, kaip apatinėje dalyje esanti lemputė, išlyginta apačioje, turinti ploną koloną, į kurią įpilama skysčio. Jame yra ženklas, nurodantis, kur turi būti skysčio meniskas, kad jis padengtų tikslų kiekį. Jame naudojami standartiniai sprendimai; dėl jo tūrio tikslumo užtikrinama žinoma koncentracija.

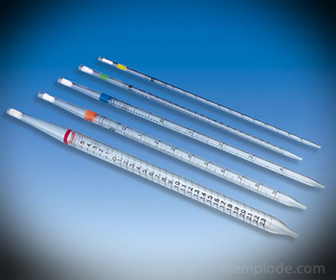
2. Pipetės: Tai yra ploni graduoti mėgintuvėliai, leidžiantys patikimai išmatuoti tikslius skysčio kiekius. Jie yra iki 25 mililitrų ir leidžia tiksliai imti mėginius.
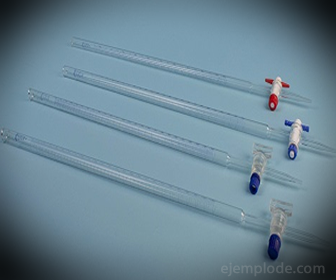
3. - biuretė: Tai pailgas 50 ml talpos mėgintuvėlis, kuriame bus standartinis tirpalas. Viename jo gale yra srauto reguliavimo vožtuvas, kuris nutekės tirpalą į alikvotinę dalį.
4. - Erlenmeyerio kolbos: tai talpyklos su plokščiu pagrindu, kūgio formos, kurios baigiasi cilindriniu kraštu. Dėl šios konstrukcijos jie tinka cheminiams titravimui, nes jie neleidžia purtant tirpalų jų perpildyti. Norint užtikrinti patikimą rezultatą, norint pakartoti bandymą reikės mažiausiai trijų.

Skaičiavimai atliekant tūrinę analizę
Tvarkant vandeninius tirpalus, tūrinei analizei svarbūs kiekiai yra koncentracija ir tūris.
Pagrindinė tūrio lygtis pagrįsta keturiais pagrindiniais duomenimis:
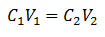
C1= Mėginio koncentracija (nežinoma)
V1= Alikvotinės dalies, su kuria buvo atlikta analizė, tūris
C2= Standartinio tirpalo koncentracija, naudojama ekvivalentiškumo taškui pasiekti
V2= Tūrio etaloninis tirpalas, reikalingas reakcijos pabaigai pasiekti
Duomenys pakeičiami lygtimi, paliekant nežinomą tik siekiamą koncentraciją. Žinoma, visi duomenys turi būti tuose pačiuose diskuose.
Tūrinės analizės pavyzdžiai
Chloridų (Cl-) nustatymas Argentometrijos metodu naudojant sidabro nitratą.
Bromidų (Br-) nustatymas Argentometrijos metodu naudojant sidabro nitratą.
Cianidų (CN-) nustatymas Argentometrijos metodu naudojant sidabro nitratą.
Magnio karbonato (MgCO) nustatymas3), taikant kompleksometriją, naudojant EDTA.
Kalcio karbonato (CaCO3), taikant kompleksometriją, naudojant EDTA.
Sieros rūgšties analizė (H2SW4) su natrio hidroksidu (NaOH).
Natrio hidroksido (NaOH) ir druskos rūgšties (HCl) analizė.
Stibio (III) nustatymas kalio permanganatu (KMnO4).
Arseno (III) nustatymas kalio permanganatu (KMnO4).
Titano (III) nustatymas kalio permanganatu (KMnO4).
Molibdeno (III) nustatymas kalio permanganatu (KMnO4).
Geležies (II) nustatymas kalio permanganatu (KMnO4).
Oksalato jono nustatymas kalio permanganatu (KMnO4).


