10 Gāzes maisījumu piemēri
Miscellanea / / July 04, 2021
Maisījumi gāzveida vielas Tie ir daži no visvieglāk sasniedzamajiem, jo ir ļoti iespējams, ka vielas, kas atrodas šajā agregācijas stāvoklī, tiek sajauktas. Piemēram: Neona, argona un ksenona maisījums, aerosola insekticīds, gaiss un hēlijs.
Praktiski visas gāzes var neierobežoti apvienot, protams, daži to kondicionē ķīmiski, fiziski un būtībā saistīti ar lietotāju drošības aspektiem manipulē. Tāpat kā dažāda veida maisījumi, kas izveidoti starp vielām, arī gāzes viņiem ir arī tikai viņiem raksturīgas īpašības.
Pētījums gāzētie maisījumi parasti ir tikpat noderīgas kā tīrā stāvoklī esošās gāzes: tās pašas zināšanas par gaisu, kas atrodas atmosfēra nebūtu iespējama, ja nebūtu zināšanu par jauktu gāzu proporcijām un uzvedību.
Tādā veidā ir svarīgi dažus zināt Iespējas gāzu maisījumu, piemēram, parciālā spiediena īpašība (tā, ko rada katra Gāzē esošā gāze) maisījuma) un molārās frakcijas (attiecība starp gāzveida komponenta un visa maisījuma molu skaitu) soda). Kurmji izsaka gāzes daudzumu maisījumā.
The Daltona likums norāda, ka gāzes maisījuma kopējais spiediens ir vienāds ar katra daļējā spiediena summu viena no atsevišķajām gāzēm, kas tajā piedalās (tas ir atkarīgs no tā, vai gāzes nereaģē starp Jā). Daļēju spiedienu šeit saprot kā tādu, kuru iedarbotos katra no gāzēm, ja tā atrastos tikai vienā un tajā pašā traukā un vienādos apstākļos. temperatūra. A) Jā:
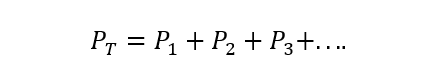
Kur PT ir kopējais spiediens un P1, P2 Un lpp3 ir hipotētisko gāzu 1., 2. un 3. daļējais spiediens gāzes maisījumā.
Izmantojot Daltona likumu, tika izstrādāta izteiksme, lai aprēķinātu daļējs spiediens gāzes gāzveida maisījumā, ja mēs zinām tās kopējo spiedienu un mola daļu.
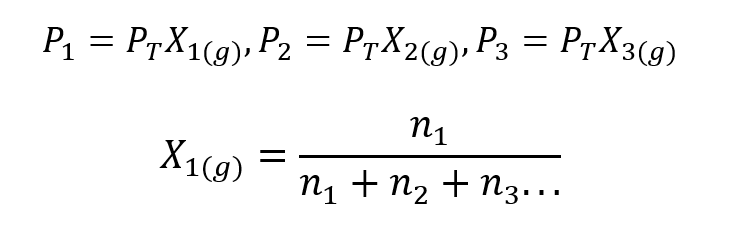
Kur X1, X2 Jā X3 ir hipotētisko gāzu 1, 2 un 3 molu daļas gāzes maisījumā un n1, n2 Jā n3 ir katras šīs gāzes vielas daudzums vienā maisījumā.
Viens no galvenās īpašības sastāvdaļu maisījumos ir koncentrācija, ko var izteikt dažādās vienībās. Gāzes maisījumu gadījumā tā sastāvdaļu koncentrāciju var izteikt ppm (milj. Daļas), kas ir vienība, kas attiecas uz tā tilpumu. Tas ir, noteikts ppm komponenta daudzums gāzes maisījumā ir attiecīgā daudzuma tilpuma attiecība pret katra miljona maisījuma vienību tilpumu.
Ir svarīgi to atzīmēt ppm gāzes temperatūra ir atkarīga no gāzes temperatūras un spiediena. Šī iemesla dēļ, lai aprēķinātu gāzes ppm, parasti izmanto normālus spiediena un temperatūras apstākļus. (CNPT), kas nodrošina normālu stāvokli līdz 0 grādiem pēc Celsija, un 1013 hektopaskālos (1 bārs) Spiediens. Ja šie nosacījumi netiek izmantoti, jums jānorāda, kuri no tiem tiks izmantoti.
Tas var kalpot jums:
Gāzu maisījumu piemēri
Šajā sarakstā ir gāzes maisījumi, norādot elementus, kas parādās maisījumā:
- Gaiss (21% skābekļa un 79% slāpekļa maisījums, kā arī citas gāzes nelielās proporcijās)
- Cronigón (99% argona un 1% skābekļa maisījums)
- Trimix (skābekļa, slāpekļa un hēlija maisījums)
- Neona, argona un ksenona maisījums
- 85% metāna, 9% etāna, 4% propāna un 2% butāna maisījums.
- Sēra heksafluorīds un gaiss
- Aerosola insekticīds
- Gaiss un hēlijs
- Nitroks (gaisa maisījums, bagātināts ar skābekli un slāpekli)
Sekojiet līdzi:

