Voorbeeld van chemische basen
Chemie / / July 04, 2021
In de algemene scheikunde, Basen zijn een categorie chemicaliën die meerdere functies vervullen:
-Reageren met zuren in een neutralisatie, het produceren van een Zout en Water.
-Regel het waterstofpotentieel, pH, waardoor de waarde stijgt, als ze in het midden worden gegoten waar een reactie wordt gevonden.
-Rennen als Chemische reagentia voor een groot aantal reacties.
De basen kunnen van verschillende soorten zijn, beide Anorganische scheikunde vanaf de Organische chemie, Zoals de Hydroxiden, de Aminen en de Alcoholen, bijvoorbeeld.
Om het gedrag van de basen te definiëren, worden de drie belangrijkste zuur-base-theorieën gebruikt: die van Arrhenius, Brönsted-Lowry en Lewis.
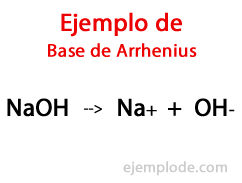
De bases volgens Arrhenius
Volgens de Zweedse scheikundige Svante Arrhenius, Basen zijn die chemische stoffen die zorgen voor hydroxylionen (OH-) aan een reagerend medium, vooral als het een waterige oplossing is. Met de beschikbare hydroxylionen zal er dus een Alkalische pH, dat wil zeggen met een waarde groter dan 7 en tot 14 afhankelijk van hoeveel Base er op het moment van de meting aanwezig is.
Dit is een van de eenvoudigste en meest praktische theorieën om toe te passen, omdat er geen complicaties zijn om de stoffen die bij de reactie betrokken zijn te onderscheiden. Het is algemeen bekend wat het zuur en wat de base is.
Binnen deze theorie zijn er onbetwistbaar anorganische hydroxiden, zoals natriumhydroxide (NaOH) en kaliumhydroxide (KOH).
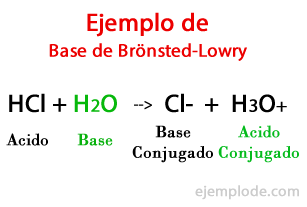
De bases volgens Brönsted-Lowry
Volgens de theorie geformuleerd door de Deense Johannes Bronsted en de Britten Thomas Martin Lowry, een basis is een chemische soort in staat om de protonen te ontvangen die een ander, het zuur, gaat geven tijdens een chemische reactie. Het proton is over het algemeen gerelateerd aan de positieve lading die het kenmerkt, dus we kunnen het weer associëren met waterstofionen (H+).
Wanneer de uitwisseling plaatsvindt in de chemische reactie, de producten heten: "Conjugated Acid Base" en "Conjugated Base Acid", gebaseerd op de reactanten die ze hebben gevormd.
Voor deze theorie is de Ammoniak (NH3) is het meest representatieve geval. Voor Brönsted en Lowry zijn de stoffen die waterstofionen (H+) kunnen vasthouden basen. In dit geval zal de ammoniak, door zich als een base te gedragen, een waterstof in zijn structuur krijgen en zichzelf consolideren als een ammoniumion (NH4+), met de overtollige positieve lading van waterstof. Ammonium is het geconjugeerde zuur van ammoniak.
Aminen, organische verbindingen afgeleid van ammoniak (NH3), zoals methylamine (CH3NH2), wanneer ze in oplossing zijn, gedragen ze zich als basen en kunnen ze positieve ladingen in hun structuur ontvangen, hetzij van waterstof of carbokation.
Een Carbokation is een organisch ion gevormd als een koolwaterstofketen, die bij afwezigheid van een negatief ion, dat Het kan de hydroxyl (OH-) of een halogeen (Cl-, Br-) zijn, het heeft de neiging te binden aan een plaats die het kan ontvangen, wat de Baseren.
De basen volgens Lewis
De Amerikaanse wetenschapper Gilbert Lewis wees er in zijn zuur-base-theorie op dat de basen zijn die stoffen die in staat zijn om hun paren vrije elektronen bij te dragen aan een ander om zijn octet te voltooien.
Deze zuur-base-theorie is een aanvulling om de geldigheid van de regel van het octet opnieuw te bevestigen, waarin wordt beschreven hoe atomen krijgen stabiliteit en bereiken een aantal van acht elektronen in hun laatste schil, met behulp van de Bond Covalent
Het Hydroxyl-ion is een goed voorbeeld van een Lewis-base. Het heeft een paar vrije elektronen waarop een waterstofion kan komen dat geen elektronen heeft. Er zal zich een molecuul water vormen. Zo zal het octet voor de zuurstof van het molecuul worden gevormd, en de waterstofatomen, die kleinere atomen zijn, zullen hun elektronenpaar hebben dat ze stabiel zal maken.

Gebruik van belangrijke bases
De Natriumhydroxide NaOH Het wordt over het algemeen gebruikt in een waterige oplossing om gestold vet in huishoudelijke en industriële kachels te reinigen en het effectief op te lossen. Het wordt ook gebruikt, in geconcentreerde oplossing, wanneer onvoorziene lozingen van een zure stof optreden, om het te neutraliseren.
De Magnesiumhydroxide Mg (OH)2 Het wordt gebruikt in een oplossing genaamd "Milk of Magnesia", om brandend maagzuur op te lossen en te neutraliseren. Het wordt verkocht in apotheken.
De Kaliumhydroxide KOH Het wordt gebruikt als reagens voor verzepingsprocessen, waarbij vetten worden omgezet in zeep.
De Ammoniak NH3 Het wordt in gasvorm gebruikt als industrieel koelmiddel, vooral in ijsmachines. Het is zeer gevaarlijk om te gebruiken, aangezien het inademen van een concentratie van 5 milligram per liter ervan in de lucht dodelijk kan zijn.
Voorbeelden van chemische basen
Water H2OF
Ammoniak NH3
Natriumhydroxide NaOH
Kaliumhydroxide KOH
Magnesiumhydroxide Mg (OH)2
Calciumhydroxide Ca (OH)2
Aluminiumhydroxide Al (OH)3
Ammoniumhydroxide NH4Oh
IJzerhydroxide Fe (OH)2
IJzerhydroxide Fe (OH)3
Hydroxylion (OH-)
Chloride-ion (Cl-)
Bromide Ion (Br-)

