30 Eksempler på aldehyder
Eksempler / / November 06, 2023
De aldehyder er organiske forbindelser som er dannet av en karbonkjede som har en terminal karbonylgruppe (= C = O) festet (plassert i den ene enden av molekyl), som igjen er bundet til et hydrogenatom.
Svært vanlige aldehyder er metanal (formaldehyd), etanal (acetaldehyd) og propanal (propaldehyd).

Noen av disse forbindelsene finnes i naturen, for eksempel er vanillin eller vanillin et naturlig aldehyd som utgjør hovedsmaksstoffet til vanilje.
- Se også: Aldehyder og ketoner
Nomenklatur for aldehyder
Aldehyder kan navngis ved å bruke nomenklaturreglene etablert av International Union of Pure and Applied Chemistry (IUPAC).
For å navngi et aldehyd brukes prefikser som indikerer antall karbonatomer som karbonkjeden har festet til karbonylgruppen. Karbonylgruppen er alltid plassert i den ene enden av karbonkjeden, noe som betyr at den alltid vil ha posisjon én og det er ikke nødvendig å angi dens plassering i kjeden. I tillegg er suffikset -al plassert på slutten av aldehydnavnet. Noen eksempler er:
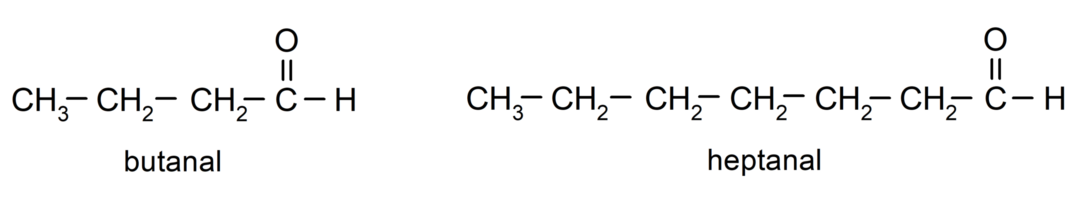
Hvis aldehydet er forgrenet, det vil si at det består av flere karbonkjeder, den hovedkjeden som den kjeden som har flest karbonatomer, og som også inneholder gruppen karbonyl. Resten av kjedene er navngitt som substituentgrupper.
Videre må hver substituentgruppe velges slik at dens posisjon opptar lavest mulig nummerering i hovedkarbonkjeden. På den annen side begynner karbonatomene i hovedkjeden å telles i enden som inneholder karbonylgruppen. Noen eksempler er:
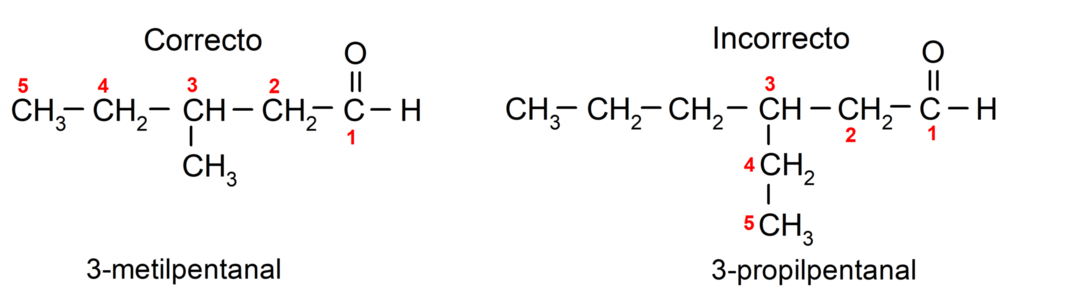
Hvis aldehydet fungerer som en substituent i molekylet, fordi det også består av grupper høyere prioriterte funksjoner, slik som syrer og estere, er aldehydgruppen navngitt som -oxo. For eksempel:

Hvis et aldehyd har flere karbonylgrupper, navngis det ved hjelp av prefikser som indikerer antallet av disse gruppene, dial (to karbonylgrupper), trial (tre karbonylgrupper), etc. For eksempel:
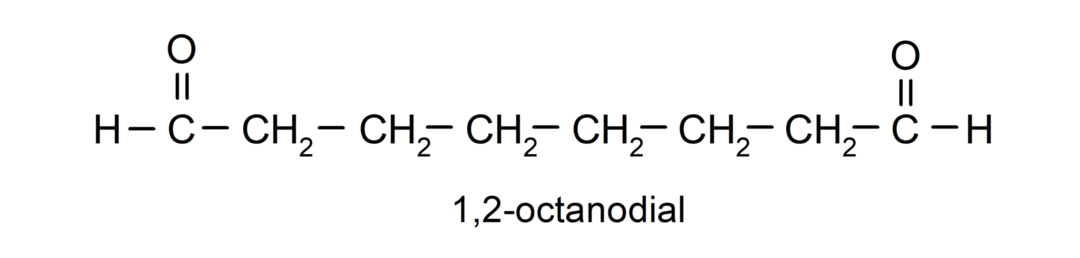
Når karbonylgruppen er knyttet til en syklus, er aldehyder navngitt ved å bruke begrepet karbaldehyd. For eksempel:

Fysiske egenskaper til aldehyder
Aldehyder har vanligvis en viss variasjon av den samme fysiske egenskapen. Dette skjer fordi de fysiske egenskapene til aldehyder avhenger av hvordan karbonkjeden som er festet til karbonylgruppen dannes.
Noen fysiske egenskaper til aldehyder er:
- Løselighet. Vannløseligheten til aldehyder avhenger av mengden av atomer som har karbonkjeden. Aldehyder med kortere karbonkjeder (opptil omtrent fem karbonatomer) er løselige i vann. Aldehyder med karbonkjeder med mange karbonatomer er ikke løselige i vann. Metanal og etanal er svært løselige i vann.
- Tetthet. Generelt er aldehyder forbindelser som har mindre tetthet enn vann.
- Aggregasjonsstater. Aldehyder som består av ett og to karbonatomer er gasser, er de som inneholder mellom tre og tolv karbonatomer væsker, og de som består av mer enn tolv karbonatomer er faste.
- Lukt. Noen aldehyder har irriterende lukt, mens andre har behagelig lukt.
- Polaritet. Karbonylgruppen gir dem polaritet.
- Kokepunkt. De har høyere kokepunkter enn alkaner med tilsvarende molekylvekt, og de har lavere kokepunkter enn karboksylsyrer og alkoholer med sammenlignbar molekylvekt.
Kjemiske egenskaper til aldehyder
Noen av de kjemiske egenskapene til aldehyder er:
Aldehyder oksideres når de reagerer med Tollens, Benedict og Fehling reagenser. for å danne den tilsvarende karboksylsyren. Syren som dannes vil ha samme antall karboner i karbonkjeden som aldehydet den ble dannet av. For eksempel:
- Oksidasjon med Tollens-reagens (ammoniakksølvkompleks i basisk løsning, [Ag (NH3)2]+). Denne reaksjonen produserer den tilsvarende syre og metallisk sølv.

- Oksidasjon med Benedict og Fehling reagens (alkaliske løsninger av kobber (II) sulfat (CuSO4) med forskjellige sammensetninger). Denne reaksjonen produserer den tilsvarende syre og kobber(II)oksid (Cu2ENTEN).

De gjennomgår nukleofile addisjonsreaksjoner, hvor nukleofiler er lagt til karbonylgruppen til aldehyder. Noen eksempler er:
- addisjonsreaksjoner alkoholer til karbonylgruppen til aldehyder for å danne acetaler og hemiacetaler.
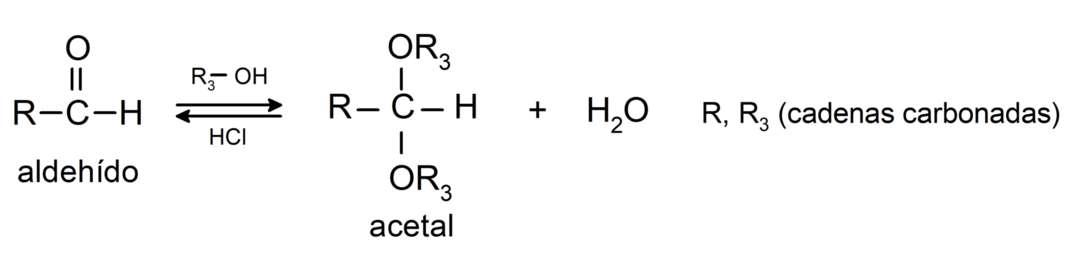
- addisjonsreaksjoner aminer primær til karbonylgruppen.

- Hydrocyanic acid (HCN) addisjonsreaksjoner, hvor cyanohydriner eller cyanohydriner dannes.

De gjennomgår aldol-kondensasjonsreaksjoner. I denne typen reaksjon kondenserer to aldehyder for å danne en aldol. De er reaksjoner som oppstår med natriumhydroksid (NaOH). For eksempel:
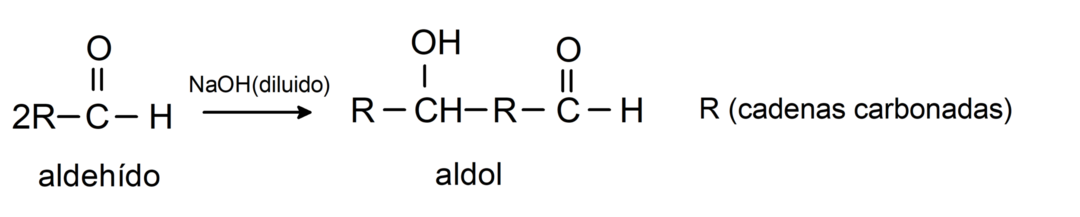
De gjennomgår reduksjonsreaksjoner på primære alkoholer. I nærvær av natriumborhydrid (NaBH4) og litiumaluminiumhydrid (LiAlH4) eller ved katalytisk hydrogenering, reduseres de til primære alkoholer. For eksempel:
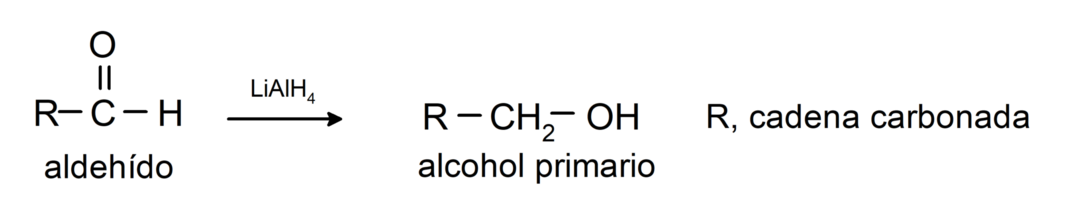
Eksempler på aldehyder
- metanal (formaldehyd)
- etanal (acetaldehyd)
- propanal (propaldehyd)
- butanal
- pentanal
- vanillin
- kanelaldehyd
- propenal
- benzaldehyd
- heksanal
- 3-bromcyklopentankarbaldehyd
- cykloheksankarbaldehyd
- 4,4-dimetylpentanal
- 2-hydroksy-butanal
- 2-hydroksy-2-metyl-butanal
- 2,3-dimetylpentanal
- pentanedial
- cyklopentankarbaldehyd
- isobutanal
- 2-klor-butanal

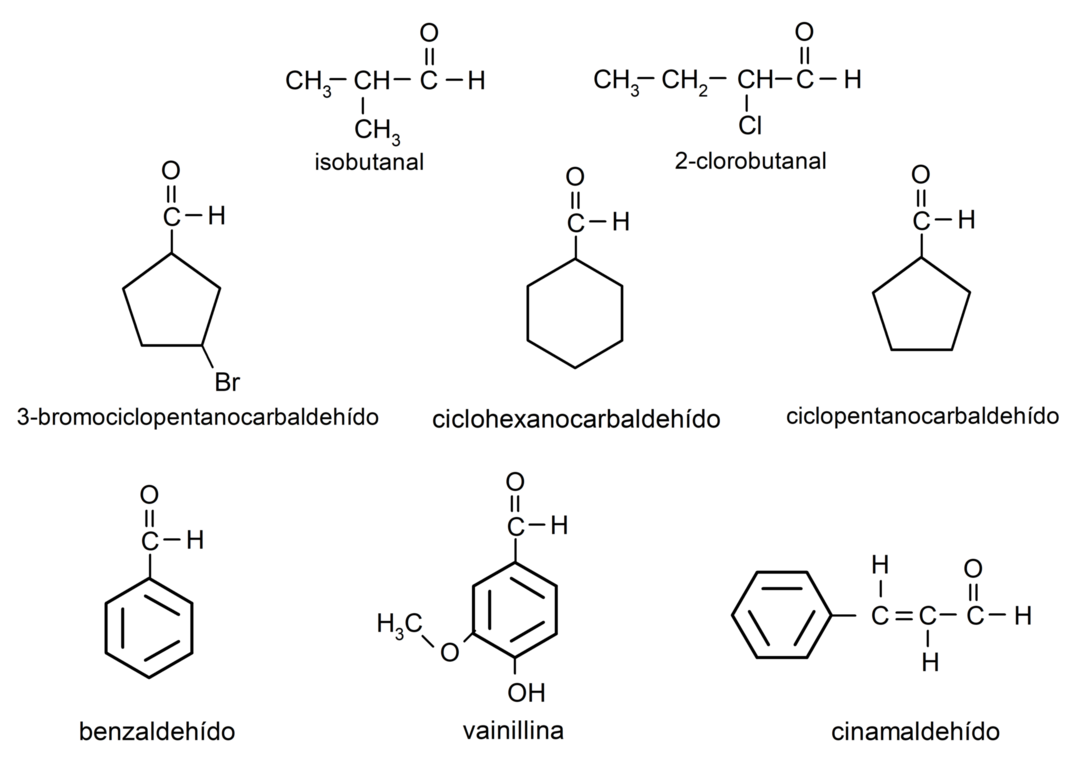
Aldehyder i naturen
Noen aldehyder som finnes i naturen er:
- Benzaldehyd, en komponent av mandler.
- Kanelaldehyd, komponenten som gir kanelessensen lukten.
- Vanillin, komponenten som gir vaniljen sin smak.
På den annen side har en av formene for glukose, den åpne formen, en aldehydfunksjonell gruppe.
Acetaldehyd, som dannes som et mellomprodukt i metaboliseringen av alkohol, antas å forårsake bakrussymptomer når det er beruset av alkohol.
Bruk av aldehyder
Noen av de viktigste bruksområdene for aldehyder er:
- De brukes i produksjon av løsemidler, maling, kosmetiske produkter og essenser.
- De brukes til fremstilling av harpikser. Bakelitt er laget med formaldehyd og er en harpiks som fungerer veldig bra som en elektrisk isolator.
- De har blitt brukt som beroligende midler. Paraldehyd har blitt brukt som et beroligende og hypnotisk middel, selv om det nå er ute av bruk på grunn av dens ubehagelige lukt.
- De brukes som konserveringsmidler for biologiske prøver og lik. Formaldehyd er mye brukt i denne forstand.
- De brukes som matsmak. Et eksempel er vanillin, som brukes for å gi desserter en vaniljearoma.
- De brukes som desinfeksjonsmidler.
Farer ved aldehyder
Flere aldehyder har blitt ansett som kreftfremkallende, for eksempel er formaldehyd erklært som en kreftfremkallende forbindelse ifølge WHO (Verdens helseorganisasjon).
Eksponering og kontakt med mange aldehyder forårsaker irritasjon av hud, øyne og luftveier. På den annen side forårsaker det kontakteksem og leversykdommer.
Referanser
- Solomons, T.W. Graham og María Cristina Sangines Franchini (1985). “organisk kjemiMexico, D.F.: Limusa.
- Whitten, K. W., Gailey, K. D., Davis, R. E., de Sandoval, M. T. TIL. O., & Muradás, R. M. g. (1992). “Generell kjemi" (s. 108-117). McGraw-Hill.
- Arteaga, P. M. (2017). “Ketoner og aldehyder” Con-Science Scientific Bulletin of the Preparatory School nr. 3, 4(8).
Følg med:
- Sukker
- Hydracider
- Etyl alkohol
- Organiske og uorganiske forbindelser