30 Eksempler på alkoholer
Eksempler / / November 06, 2023
De alkoholer er organiske kjemiske forbindelser som inneholder i sin struktur den funksjonelle hydroksylgruppen (-OH) festet til et karbon (- C). Gruppen (- C – OH) kalles "karbinol". Noen eksempler på alkoholer er: metanol, etanol og 1-propanol.
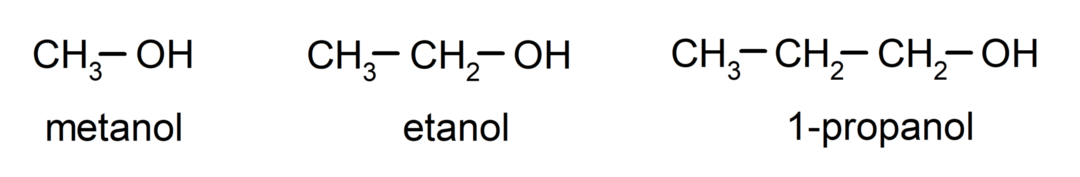
Alkoholer er kjemiske forbindelser med ulike bruksområder i hverdagen, da de har antibakterielle og antiseptiske egenskaper. På den annen side kan de være farlige for menneskers helse når de inntas ukontrollert.
På samme måte kan ikke alle alkoholer inntas av mennesker.
- Se også: Aminer og ketoner
Typer alkoholer
Avhengig av antall karbonatomer som karbonatomet som har hydroksylgruppen festet til, kan en alkohol være:
- Primær alkohol. Karbonatomet som har hydroksylgruppen festet er også festet til et enkelt karbonatom. For eksempel:
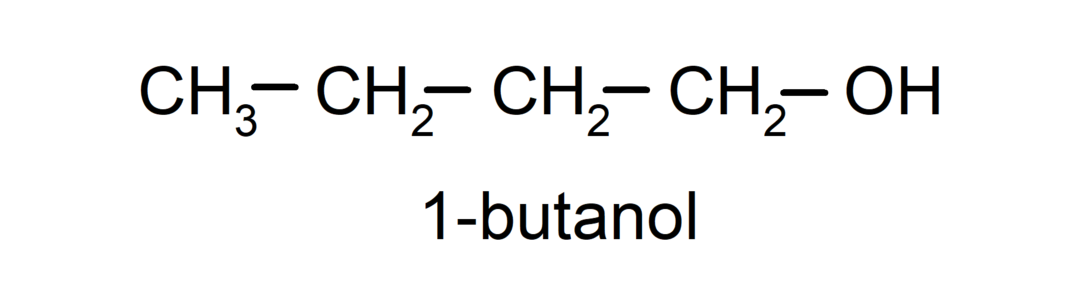
- Sekundær alkohol. Karbonatomet som har hydroksylgruppen festet er også bundet til to andre karbonatomer. For eksempel:
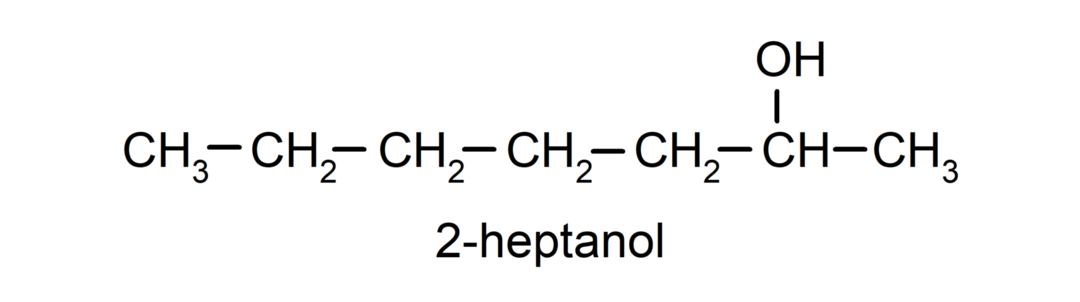
- Tertiær alkohol. Karbonatomet som har hydroksylgruppen festet er også festet til tre karbonatomer. For eksempel:
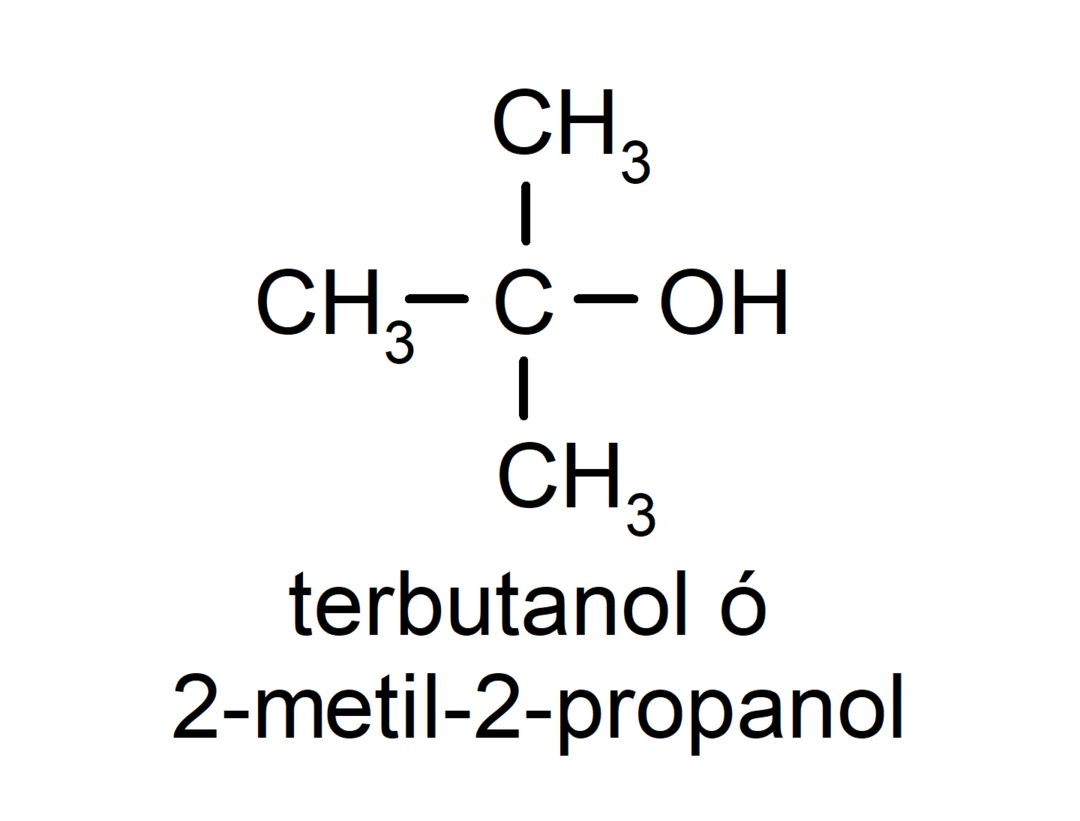
Avhengig av antall hydroksylgrupper den har, kan en alkohol være:
- Diol. Den har to hydroksylgrupper i strukturen. For eksempel:
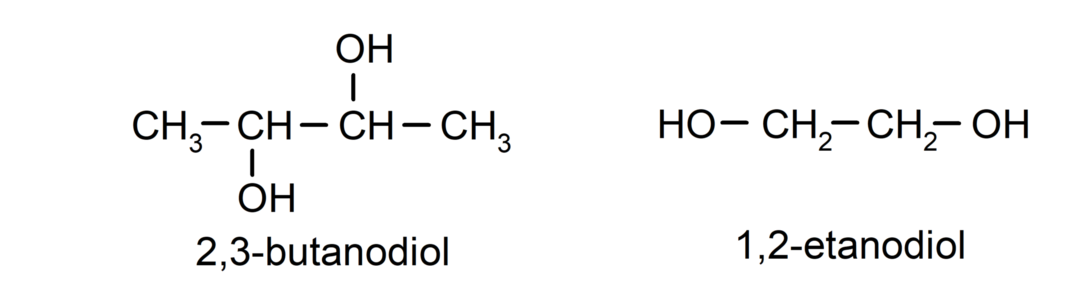
- Triol. Den har tre hydroksylgrupper i strukturen. For eksempel:
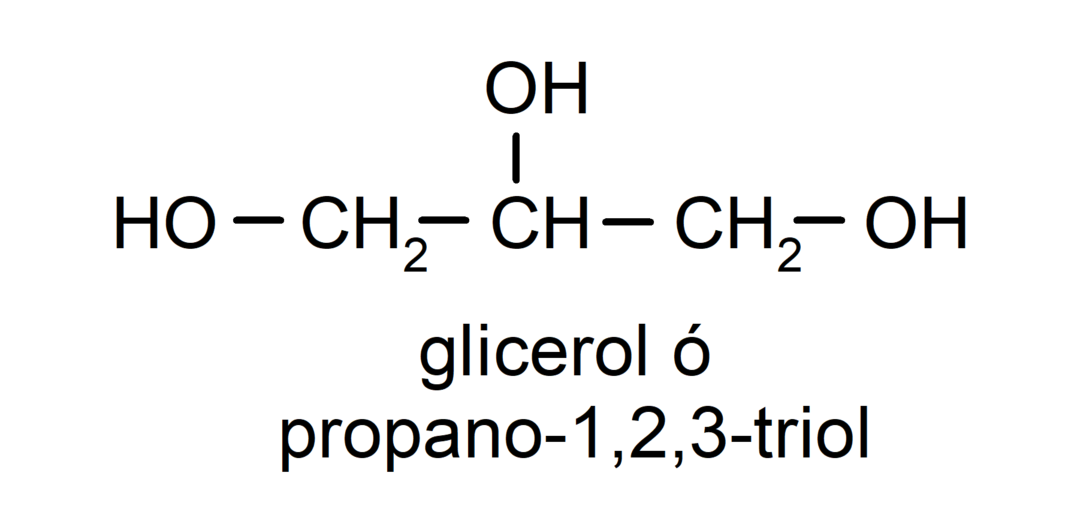
- Polyalkohol. Den har mange hydroksylgrupper i strukturen. For eksempel:
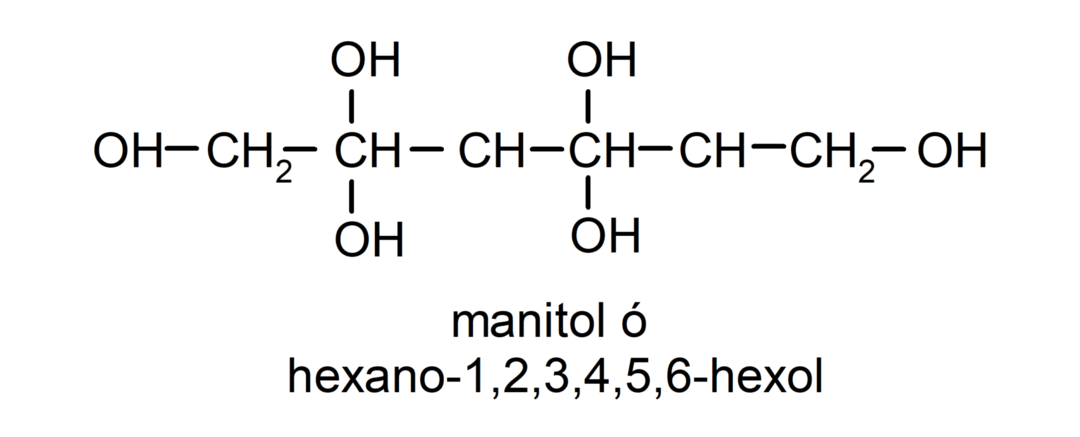
Fysiske egenskaper til alkoholer
Noen av de fysiske egenskapene til alkoholer er:
- Kokepunkt. Kokepunktet i alkoholer er ganske høyt på grunn av tilstedeværelsen av hydroksylgruppen, som tillater dannelse av hydrogenbindinger. Videre, jo flere hydroksylfunksjonelle grupper er tilstede i karbonkjeden, jo høyere er Kokepunkt av alkoholer.
- Polaritet. Alkoholer er ganske polare forbindelser.
- Løselighet. Lavmolekylære alkoholer er løselige i vann. På den annen side, jo større karbonkjeden av alkoholer, desto lavere er deres løselighet i vann. I tillegg, jo flere hydroksylgrupper alkoholer har, desto større er deres løselighet i vann.
- Aggregeringstilstand. De fleste alkoholer er flytende ved romtemperatur (25ºC) og har karakteristiske lukter.
Kjemiske egenskaper til alkoholer
Noen av de kjemiske egenskapene til alkoholer er:
- Alkoholer oppfører seg som syrer og baser.. Deres oppførsel som syrer kan sees i reaksjoner med aktive metaller for å frigjøre hydrogengass og danne alkoksyder.

Deres oppførsel som baser kan sees i reaksjoner som reaksjonen av metanol med hydrogenbromid for å danne metyloksoniumbromid.
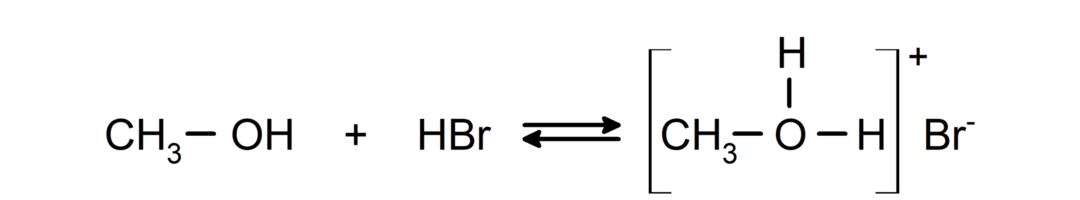
- Alkoholer gjennomgår halogeneringsreaksjoner. De reagerer med hydrogenhalogenider for å danne alkylhalogenider.
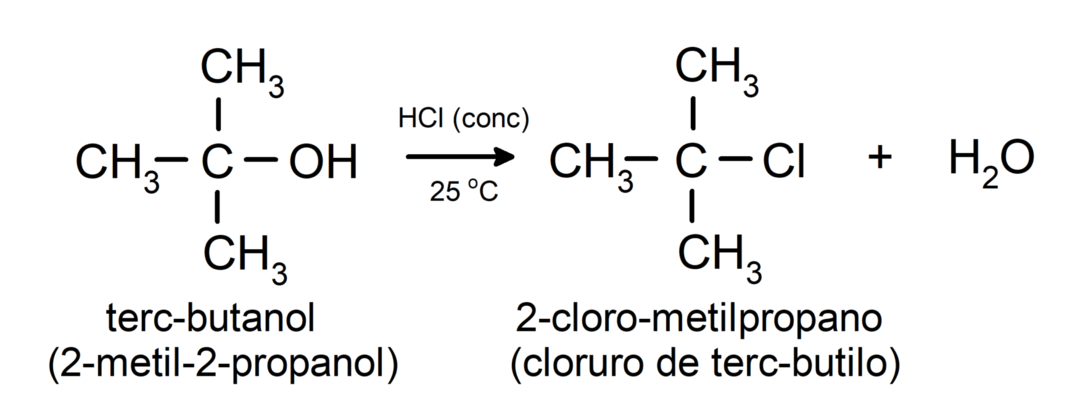
-
Alkoholer gjennomgår oksidasjonsreaksjoner når de reagerer med visse oksiderende forbindelser. Produktene av oksidasjonsreaksjoner avhenger av typen alkohol som reagerer, det vil si om den er primær, sekundær eller tertiær.
Oksidasjon av primær alkohol for å danne aldehyd eller karboksylsyre.
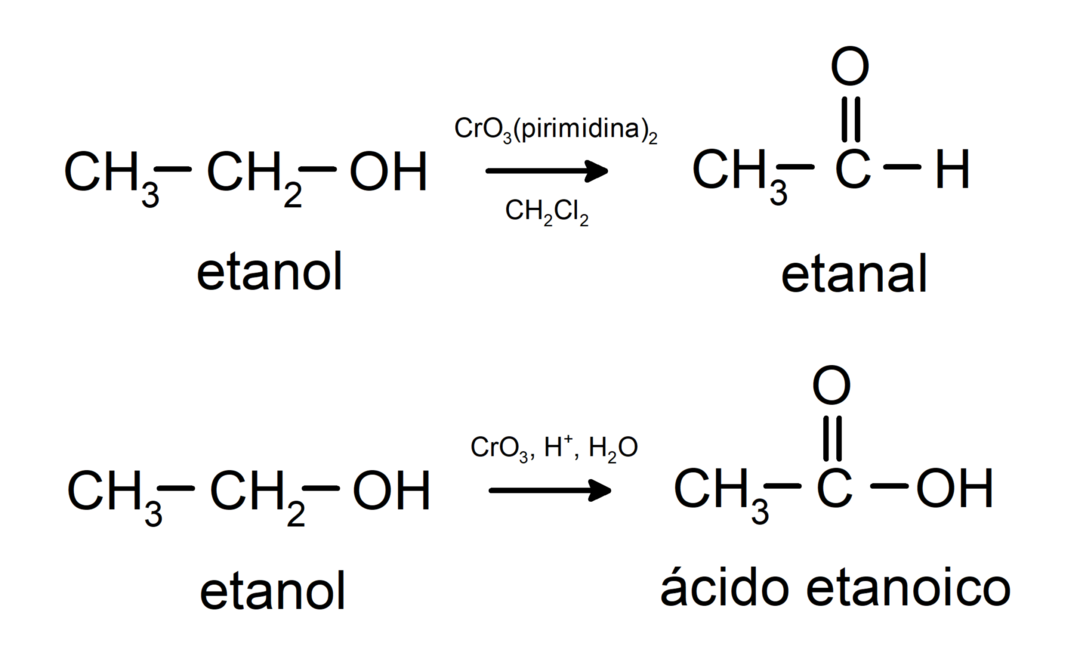
Oksidasjon av sekundær alkohol for å danne keton.
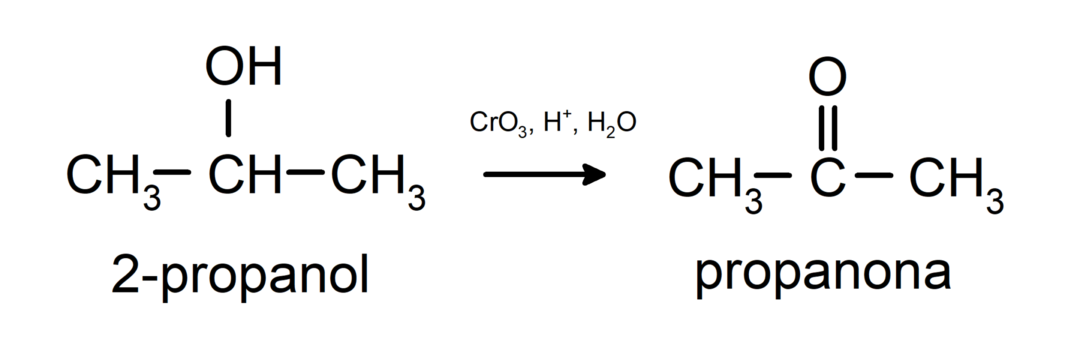
Tertiære alkoholer oksiderer ikke med vanlige oksidanter. Med svært sterke oksidasjonsmidler kan de omdannes til alkener, som deretter kan oksideres.
Alkoholer som har to hydroksylgrupper lokalisert på tilstøtende karboner oksideres med blytetraacetat for å danne to ketoner.
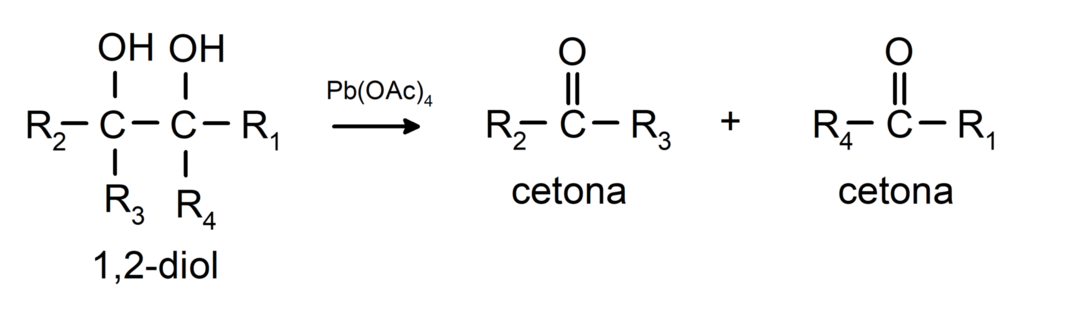
- Alkoholer gjennomgår dehydrogeneringsreaksjoner. Disse reaksjonene forekommer bare med primære og sekundære alkoholer, som når de utsettes for høye temperaturer i nærvær av katalysatorer, frigjør hydrogener.
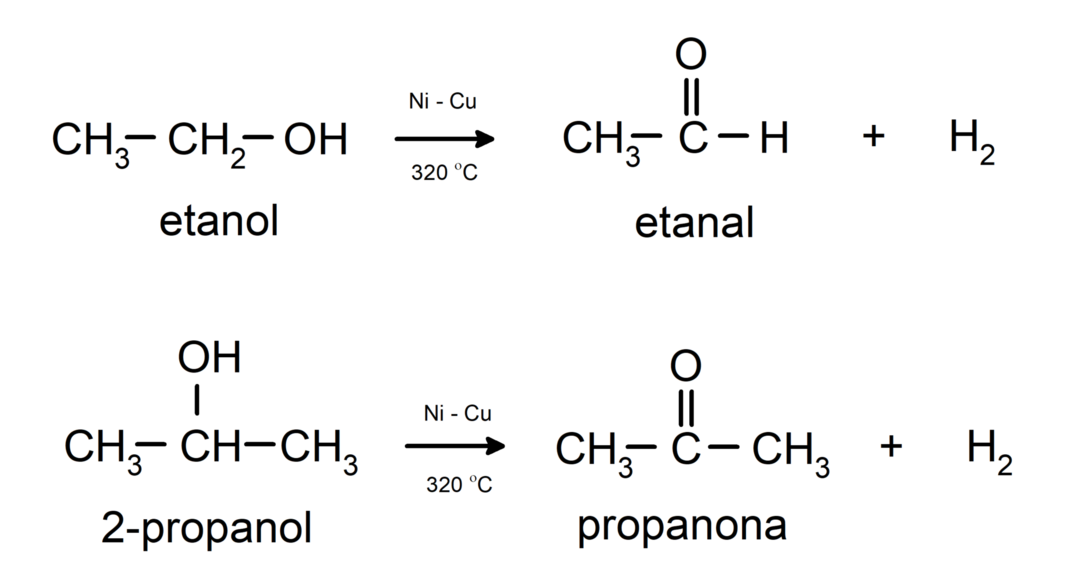
- Alkoholer gjennomgår dehydreringsreaksjoner. Alkoholer dehydrerer for å danne de tilsvarende alkenene. Denne reaksjonen skjer i nærvær av sure og mellomliggende temperaturer.
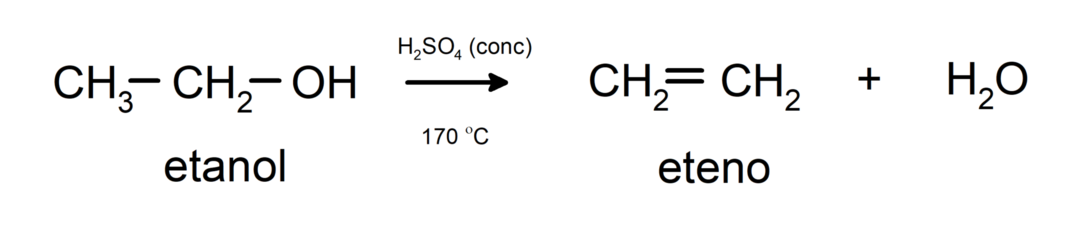
Alkoholnomenklatur
I henhold til nomenklaturen etablert av IUPAC (International Union of Pure and Applied Chemistry), er alkoholer navngitt etter følgende regler:
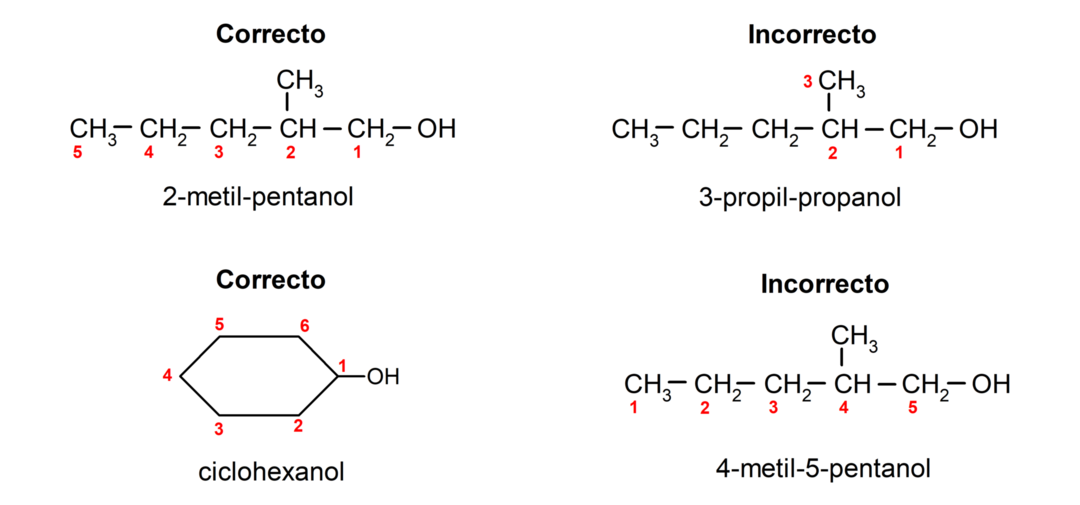
- Plasseringen av hydroksylgruppen er valgt under hensyntagen til at den opptar lavest mulig antall i karbonkjeden. Hvis strukturen til alkoholen er syklisk, vurderes 1-posisjonen på karbonet som har hydroksylgruppen festet, og prefikset syklo- brukes for å navngi det.
- Navnet på alkoholen skrives ved hjelp av prefikser som indikerer antall atomer i karbonkjeden, og i tillegg plasseres suffikset -ol.
- Hvis strukturen til alkoholen har forgreninger, velges den lengste kjeden som også inneholder hydroksylgruppen som hovedkarbonkjede.
I følge tradisjonell nomenklatur navngis alkoholer ved å skrive ordet "alkohol" og deretter skrive navnet på alkoholen. alkan som tilsvarer karbonkjeden, men i stedet for å bruke -an-enden av alkanen, -yllisk.
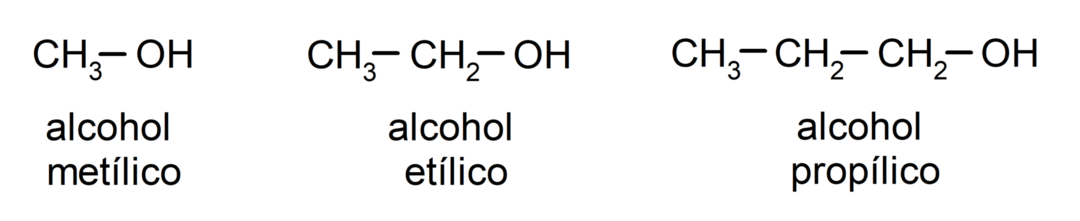
Eksempler på alkoholer
- metanol
- etanol
- 1-propanol
- 2-propanol
- 1-butanol
- 3-etylheksan-2-ol
- glyserol
- fenol
- 2-metyl-2-butanol
- 1,2-etandiol
- 1,5-heptadien-3-ol
- 3-metyl-2-butanol
- benzylmetanol
- 3-pentanol
- 2-metylfenol
- 1,2-dihydroksyfenol
- cycloheaxnol
- 1-fenyletanol


Bruk av alkoholer
De vanligste bruken av alkoholer er:
- De brukes som desinfeksjonsmidler og antiseptiske midler siden de stopper veksten av noen mikroorganismer eller ødelegge dem. Etanol og isopropylalkohol er de mest brukte til dette formålet.
- De brukes i syntesen av forskjellige kjemiske forbindelser. Metanol brukes for eksempel for å oppnå metanal (formaldehyd).
- De brukes til å produsere frostvæske. Metanol er en av de mest brukte til dette formålet.
- De brukes som løsemidler i farmasøytisk industri. Etanol er en av de mest brukte i denne forstand.
- De brukes som løsemidler for lakk, fargestoffer og blekk. Metanol er mye brukt til dette formålet.
- De brukes som drivstoff og det er en viktig tendens til å delvis erstatte bruken av fossilt brensel ved bruk av bioetanoldrivstoff.
- De brukes til å lage harpikser. Fenol brukes i denne forstand.
Farer ved alkoholforbruk
Selv om alkoholforbruk er sosialt akseptert i dag, genererer misbruk av dette stoffet avhengighet og avhengighet.
Etanol er alkoholen som er tilstede i alkoholholdige drikker, som når det konsumeres i overkant påvirker kognitive evner, og kan forårsake hjerte- og karsykdommer, levercirrhose og kreft.
Videre, når graden av alkoholforgiftning er nådd, det vil si en tilstand av beruselse, hvis dosen av alkohol er for høyt, kan en alkoholisk koma oppstå, noe som kan føre til luftveislammelse og til og med død. død.
Referanser
- T. TIL. Geissman. (1974) "Principles of Organic Chemistry" Andre utgave. Redaksjonell Reverté, S.A. ISBN: 8429171800
- Ahumada-Cortez, J. G., Gámez-Medina, M. E., & Valdez-Montero, C. (2017). Alkoholforbruk som et folkehelseproblem. Ra Ximhai, 13(2), 13-24.
- Morrison, R. T., & Boyd, R. N. (1998). Organisk kjemi. Pearson utdanning.
- Weininger, S. J., & Stermitz, F. R. (1988). Organisk kjemi. Jeg snudde.
Følg med:
- Etyl alkohol
- Drivstoff
- organisk kjemi


