Eksempler på endotermiske reaksjoner
Eksempler / / November 09, 2023
EN endoterm reaksjon Det er en reaksjon som absorberer energi fra mediet i form av varme. I disse reaksjonene, for at reaktantene skal omdannes til produkter, er det nødvendig at de absorberer varme, noe som gjør at produktene har større energi enn reaktantene som ga opphav til dem. Noen eksempler på endoterme reaksjoner er: fotosyntese og vannelektrolyse.
- Se også: Kjemiske reaksjoner
Eksempler på endoterme reaksjoner i hverdagen
Noen av de viktigste endoterme reaksjonene er:
Ozonproduksjon i atmosfæren. Ozon produseres i atmosfæren når molekylært oksygen (O2) absorberer ultrafiolett stråling og brytes ned. Da kan et oksygenatom (O) samhandle med et annet oksygenmolekyl (O2) og danner ozon (O3).

Vannelektrolyse. Det er prosessen den brukes på elektrisk energi til vann for å skille det i de to komponentene, hydrogen (H) og oksygen (O).
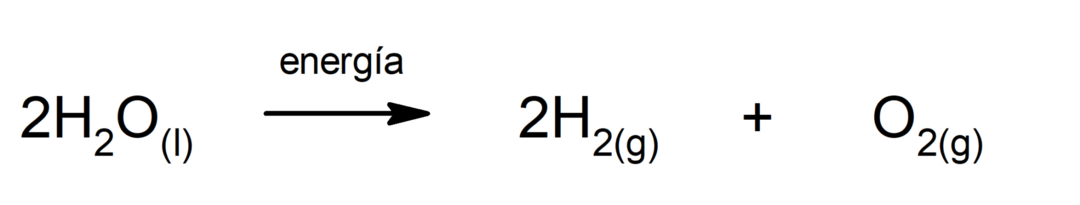
Fotosyntese. Det er den kjemiske reaksjonen som absorberer solenergi, karbondioksid (CO2) omdannes til glukose. Denne reaksjonen utgjør hovednæringsveien for planter.
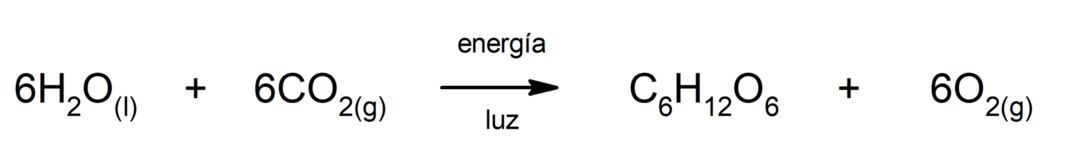
Jern(II)sulfidproduksjon. For at reaksjonen mellom svovel og jern skal skje, er det nødvendig å gi energi i form av varme.
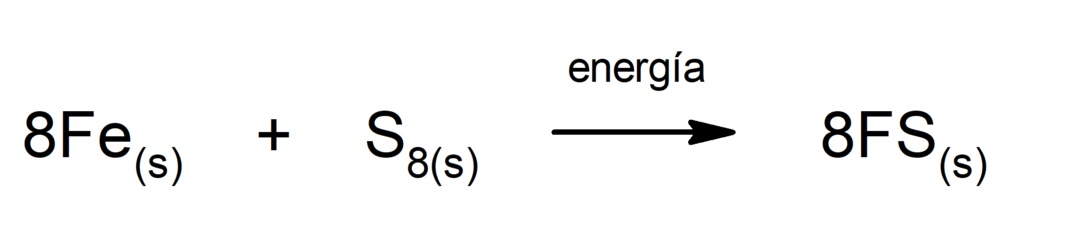
Dekomponering av karbondioksid (CO2). Nedbrytningen av CO2 Ved høye temperaturer produserer den karbonmonoksid (CO) og oksygen (O2).
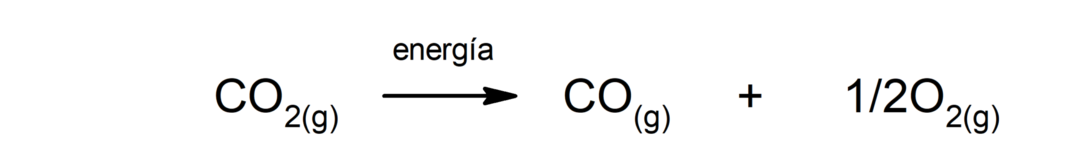
Dekomponering av kalsiumkarbonat (CaCO3). Kalsiumkarbonat brytes ned med absorpsjon av varme for å produsere kalsiumoksid (CaO) og karbondioksid (CO2).
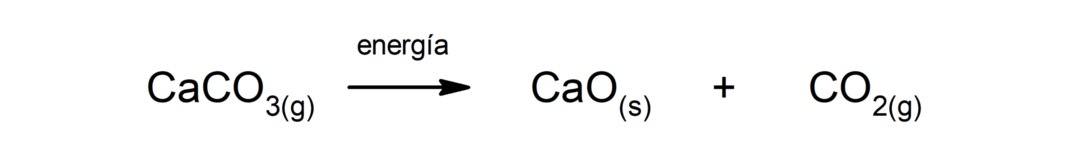
Forskjellen mellom endoterm og eksoterm reaksjon
Hovedforskjellen mellom endoterme og eksoterme reaksjoner er at endoterme reaksjoner absorberer varme, mens eksoterme reaksjoner frigjør varme.
Videre er endoterme reaksjoner preget av en økning i entalpi, mens eksoterme reaksjoner er assosiert med en reduksjon i entalpi.
Entalpi er en termodynamisk størrelse som definerer strømmen av termisk energi ved konstant trykk under en kjemisk reaksjon. Den er representert med bokstaven H, og variasjonen er en av hovedindikatorene for å definere om en kjemisk reaksjon er endoterm eller eksoterm.
- Hvis en kjemisk reaksjon har en entalpiendring større enn null (ΔH > 0) er endotermisk.
- Hvis en kjemisk reaksjon har en entalpiendring mindre enn null (ΔH < 0) er eksoterm.
Følg med:
- Fysiokjemiske fenomener
- Kjemi i hverdagen
- Kjemi i hverdagen
- Organisk og uorganisk kjemi
Referanser
- Soto-Córdoba, S. (2016). Endotermiske reaksjoner. Tech Repository Teknologisk institutt i Costa Rica.
- Corominas, J. (2017). Kjemiske reaksjoner i hverdagen. Alembic, (90), 8-26.
- Sánchez, M. T. M., & Sánchez, M. M. (2002). Eksperimentell studie av endoterme reaksjoner for ESO-studenter. Annals of Chemistry av RSEQ, (4), 36-39.



