Eksempel på volumetrisk analyse
Kjemi / / July 04, 2021
På Analytisk kjemi, den Volumetri er en analysemetode som består av Måling av reagensvolumet som trengs for å reagere støkiometrisk med analytten, som er stoffet som skal bestemmes.
Reager støkiometrisk refererer til stoffene som samhandler kjemisk, ifølge proporsjon som markerer den kjemiske ligningen allerede balansert.
Stoffet som skal undersøkes kalles Analytt. Fra dette stoffet vil et kjent og nøyaktig målt volum tas som en prøve, som vi vil kalle Alikvot, inneholdt i en Erlenmeyer-kolbe for å starte analysen.
Konsepter for volumetrisk analyse
Volumetrisk analyse, som en type Kjemisk analyse, bære involverte en kjemisk reaksjon. Denne kjemiske reaksjonen vil bli utført mellom prøven med en ukjent mengde av det undersøkte stoffet, og en kjent mengde av et annet stoff som er i stand til å reagere med førstnevnte.
De Reaksjonsstoffer vil være i vandig løsningog volumene av løsninger som samhandlet for å nå slutten av reaksjonen vil bli målt, som vil være synlige takket være en indikator som vil gi farge inne i kolben.
I volumetrisk analyse er den vandige løsningen av Kjent konsentrasjon kalles standardløsning, Standard eller Titrant, og vil tjene som en referanse for, avslutte reaksjonen, for å gjøre beregningen som vil avsløre mengden av det undersøkte stoffet.
Denne prosedyren for å få begge løsningene til å reagere kalles Kjemisk grad Verdsettelse, som er den grunnleggende delen av volumetrisk analyse. Består av å gå gradvis helle standardløsningen (Titrant) i alikvoten (Eksempel), til indikatoren viser endringen med en fargeforskjell.
EN Indikator Det er et kjemisk stoff som tilsettes alikvoten, som viser en farging, og at når reaksjonen slutter, vil den endre farge.
En volumetrisk analyse består av en enkel serie trinn:
1.- Utarbeidelse av standardløsning
2.- Klargjøring av prøven eller alikvoten
3.- Kjemisk grad
4.- Volummåling
5.- Beregning av det undersøkte stoffet.
Til det punktet de allerede har reagerte fullstendig de to stoffene, heter det Ekvivalenspunkt.
Som i alle kjemiske analysemetoder, er det i Volumetrisk analyse krav til gode resultater:
-Den kjemiske reaksjonen må være SelektivDet vil si at standardløsningen bare reagerer med prøven.
-Den kjemiske reaksjonen må være Støkiometriskdet vil si adlyde proporsjonene markert i den balanserte kjemiske ligningen.
-Den kjemiske reaksjonen må være Kvantitativ; refererer til 99,9% fullføring ved ekvivalenspunktet.
-Det må være et detekterbart sluttpunkt i reaksjonen, som bekreftes bedre av indikatoren.
Primærmønster
De Primære mønstre De er stoffer med høy renhet hvis konsentrasjon i oppløsningen beregnes direkte fra den veide mengden og volumet av vann.
A) Ja, kan reageres med arbeidsløsninger, å kjenne konsentrasjonene av sistnevnte og konvertere dem til standardløsninger.
Eksempler på primære mønstre er:
-Natriumkarbonat (Na2CO3): Brukes til å standardisere syrer, som svovelsyre.
-Kaliumbifthalat: Det er den primære standarden for å fremstille standardløsninger av baser, for eksempel natriumhydroksid.
-Natriumklorid (NaCl): Det brukes til å standardisere sølvnitratløsninger.
-Kalsiumkarbonat (CaCO3): Primær standard for EDTA (etylendiamintetraeddiksyre).
Et primært mønster må oppfylle flere viktige egenskaper:
Må ha en Høy renhet, Atmosfærisk stabilitet, Fravær av hydratiseringsvann, Lav pris og lett å få, Y Høy ekvivalent vekt.
Klassifisering av volumetrisk analyse
Avhengig av den kjemiske arten du jobber med å lage en analyse med, vil det være typen volumetri:
Syrebasevolumetri: Det fungerer, enten med en syre eller med en base, for å analysere prøver som inneholder syrer eller baser.
Nedbørsvolumetri: Også kalt Argentometry, den bruker en standard løsning av sølvnitrat for å bestemme hvor mange klorider som er i en prøve.
Kompleksitetsvolumetri: En standardløsning av et kompleksdannende middel, som EDTA, brukes til å måle konsentrasjonen av hardhet, det vil si kalsium og magnesiumkarbonater, i vannet.
REDOX-volumetri: Reaksjonen skjer mellom et oksiderende stoff og et reduserende stoff.
Indikatorer
Av de mange indikatorene som brukes i Volumetrics, tre skiller seg ut:
1.- Metyloransje: Det tar en oransje farge i alikvoten, som vil bli titrert med en syre. Når ekvivalenspunktet er nådd, blir indikatoren gul.
2.- Fenolftalein: Den er gjennomsiktig i begynnelsen i alikvoten, som vil ha tittelen med en base. Når ekvivalenspunktet er nådd, blir indikatoren rosa.
3.- Eriochrome Black: Det er indikatoren som brukes til å bestemme hardheten i vann. I begynnelsen er den lilla i alikvoten, til den titreres med et kompleksdannende middel. På slutten av reaksjonen blir den blå.

Instrumenter i en volumetrisk analyse
I en volumetrisk analyse vil en rekke instrumenter brukes som, hvis de ikke er tilgjengelige, ikke kan utvikles tilstrekkelig:
1.- Volumetrisk kolbe: Det er en beholder som en pære i nedre del, flatt i bunnen, som har en tynn kolonne der væsken tilsettes. Den har et merke som indikerer hvor menisken på væsken skal være, slik at den dekker det nøyaktige volumet. Den brukes til å inneholde standardløsninger; takket være nøyaktigheten av volumet, sikres en kjent konsentrasjon.

2. - Pipetter: De er graduerte tynne rør som gjør det mulig å måle pålitelige nøyaktige mengder væske. De er tilgjengelige opptil 25 milliliter, og tillater nøyaktig prøvetaking.
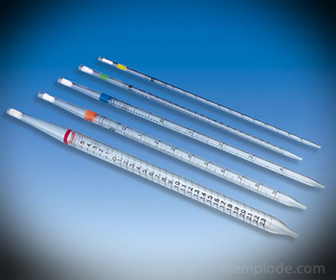
3.- Burette: Det er et langstrakt rør med en kapasitet på 50 milliliter, som inneholder standardløsningen. I den ene enden har den en strømningsregulerende ventil som vil tømme løsningen inn i alikvoten.
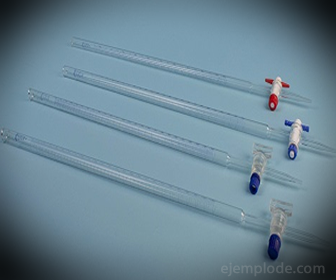
4.- Erlenmeyer-kolber: De er beholdere med en flat, konisk form som ender i en sylindrisk kant. Denne designen gjør dem egnet for kjemiske titreringer, siden de ikke lar risting av løsningene renne over dem. Minimum tre vil være påkrevd hvis gjentatt testing skal utføres for å sikre et pålitelig resultat.

Beregninger i en volumetrisk analyse
Når vandige løsninger håndteres, er mengdene som er viktige for en volumetrisk analyse, konsentrasjon og volum.
Hovedligningen for Volumetry er basert på fire hoveddata:
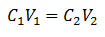
C1= Prøvekonsentrasjon (ukjent)
V1= Volum av alikvoten, som analysen ble arbeidet med
C2= Konsentrasjon av standardløsning brukt for å nå ekvivalenspunktet
V2= Volum Standardløsning nødvendig for å komme til slutten av reaksjonen
Dataene er erstattet i ligningen, slik at bare konsentrasjonen som er ønsket er ukjent. Selvfølgelig må alle dataene være på de samme stasjonene.
Eksempler på volumetriske analyser
Bestemmelse av klorider (Cl-) ved Argentometry, med sølvnitrat.
Bestemmelse av bromider (Br-) ved Argentometry, med sølvnitrat.
Bestemmelse av cyanider (CN-) ved Argentometry, med sølvnitrat.
Bestemmelse av magnesiumkarbonat (MgCO3), ved kompleksmetri, med EDTA.
Bestemmelse av kalsiumkarbonat (CaCO3), ved kompleksmetri, med EDTA.
Svovelsyreanalyse (H2SW4) med natriumhydroksid (NaOH).
Analyse av natriumhydroksid (NaOH) med saltsyre (HCl).
Bestemmelse av antimon (III) med kaliumpermanganat (KMnO4).
Bestemmelse av arsen (III) med kaliumpermanganat (KMnO4).
Bestemmelse av titan (III) med kaliumpermanganat (KMnO4).
Bestemmelse av molybden (III) med kaliumpermanganat (KMnO4).
Bestemmelse av jern (II) med kaliumpermanganat (KMnO4).
Bestemmelse av oksalation med kaliumpermanganat (KMnO4).



