Peptidbindingseksempel
Kjemi / / July 04, 2021
De Peptid Bond er den der to aminosyremolekyler er forbundet med kondens.
For å bedre forstå peptidbindinger, må aminosyrer først defineres:
De Aminosyrer er organiske molekyler kort inneholder minst en aminogruppe (-NH2), alkalisk i naturen, og en karboksylgruppe (-COOH), sur i karakter.
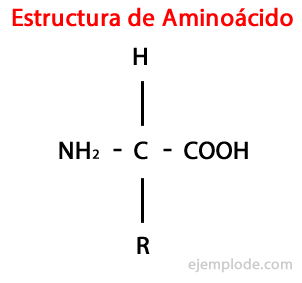
Selv om levende vesener for forskjellige formål syntetiserer svært forskjellige typer aminosyrer, er de viktigste de som er en del av proteiner, som alle tilhører klassen til α-aminosyrer.
Α-aminosyrene er preget av å ha syre- og aminogruppene bundet til samme karbonatom, kalt α Carbon. Videre binder dette α-karbonet, som en tredje substituent, et hydrogenatom og som et fjerde substituent, en ytterligere gruppe av forskjellig størrelse og egenskaper, som skiller hver aminosyre fra andre.
Den fjerde substituenten heter Sidekjede av aminosyre og er ofte representert i forenklet form med bokstaven R.
Ettersom de fire substituentene til α-karbon er forskjellige, og vedtar et tetraederarrangement rundt det, er a-aminosyrene til stede
optisk isomerisme, som er når et molekyl har en alternativ form som ser ut som en speilbilde hans, som til slutt ikke er et like molekyl. Disse to isomere formene av molekylet tildeles bokstavene D eller L, avhengig av hvordan substituentene er ordnet i rommet. Alle aminosyrene som er i proteiner er L.Aminosyrer klassifiseres i henhold til deres kjemiske karakter Polar og Apolar. Polarene er i sin tur delt inn i Nøytral og ladet (som kan være sur eller basisk). De Ikke-polær kan være alifatisk eller aromatisk.
Peptider og Peptidbindingen
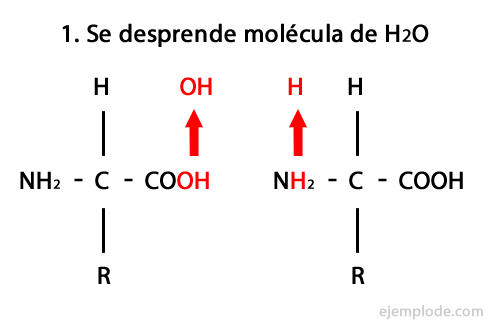
Peptider er produktet av den kovalente foreningen av aminosyrer gjennom amidbindinger, og danner ved kondensering av karboksylenden av den ene og aminoenden av den andre, og frigjør et vannmolekyl i reaksjon. Denne unionen heter Peptide Bond.
Mekanismen for denne reaksjonen er presentert nedenfor, der Amino- og karboksylgrupper, og kondensasjonen av aminosyremolekylene oppstår for å danne peptidet.
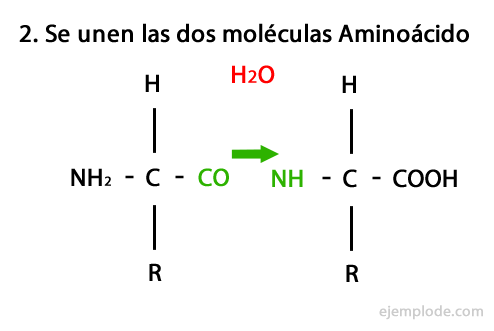

Peptider, som aminosyrer og proteiner, har en aminogruppe og en karboksylgruppe i endene uten å reagere.
For å spesifisere formelen til et enkelt peptid, og til og med et protein, er det nok å liste opp aminosyrene som komponerer det, starter med den med en gratis Amino-gruppe, og slutter med den med sin gratis karboksylgruppe.
Noen peptider som finnes i kroppen er Vasopressin, som øker blodtrykket og øker vannopptaket i nyrene; de Enkephalin, som reduserer følelsen av smerte; og Oksytocin, som får livmoren til å trekke seg sammen.
Peptidbindingsegenskaper
Kondensasjonen av aminogruppen til en aminosyre med karboksylen til en annen, foregår i vandig løsningsmiddel, så det det er ikke spontant, og derfor krever proteinsyntese tilførsel av energi.
Peptidbindingen, som i enhver amidbinding, presenterer resonans mellom to ekstreme former: den nøytrale formen, med en enkeltbinding som forbinder karbonylkarbonet i den første aminosyren og aminonitrogenet i den andre (C-N), og skjemaet med separasjon av ladninger der de to atomene er bundet av en dobbeltbinding (C = N). I virkeligheten adopterer ikke peptidbindingen noen av de to ekstreme situasjonene, men er en resonanshybrid av begge.
Det er samtalen Peptidplan, bestående av alle atomene involvert i peptidbindingen, som forbinder de to innledende aminosyrene. På den ene siden atomene til nitrogen og hydrogen, med deres respektive karbon α i den første aminosyren. På den annen side, karbon α av den andre aminosyren, med oksygen og karbon i karbonylgruppen.
Forskjeller mellom peptider og proteiner
De peptider har et lavt antall aminosyrer, som spenner fra to til noen få dusin av dem, og deres konformasjon i løsning blir fleksibel.
De små proteiner, strukturelt nær store peptider, har en definert konformasjon og mye mindre fleksibel.
Det er proteiner som, i likhet med peptider, har en forstyrret og fleksibel konformasjon, men som orden når de samhandler med andre makromolekyler i cellen.
20 eksempler på aminosyrer som deltar i peptidbinding
- Blåregn
- Til jenta
- Valine
- Leucine
- Isoleucin
- Proline
- Metionin
- Fenylalanin
- Tyrosin
- Tryptofan
- Serine
- Treonin
- Cystein
- Asparges
- Glutamin
- Asparaginsyre
- Glutaminsyre
- Lysin
- Arginin
- Histidin
