Eksempel på kjemisk energi
Kjemi / / July 04, 2021
De Kjemisk energi er den som kommer fra kjemiske reaksjoner. Samspillet mellom kjemiske arter genererer brudd og / eller generering av bindinger, noe som innebærer henholdsvis frigjøring eller absorpsjon av energi. Kjemisk energi kalles frigitt energi, som for eksempel kan brukes som termisk energi og elektrisk energi.
Energi i kjemiske reaksjoner
Kjemisk energi kan oppnås maksimalt fra to hovedkilder: forbrenning og elektrolytiske løsninger. På den annen side er det på nivået med menneskekroppen mulig å skaffe energi gjennom den kjemiske oppløsningen av mat.
Forbrenningsenergi
For eksempel når drivstoffmetan CH4, det enkleste hydrokarbonet, begynner å brenne i nærvær av Oxygen Oxidizer, det vil gå i oppløsning og danne karbondioksid CO-produkter.2 og vann H2ELLER. I tillegg vil brudd på bindinger av hydrogenatomer med karbonatomer frigjøre energi i form av varme.
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2 O (l) ∆H = -212,8 Kcal / mol
Metan forbrenning ligning. Varmen til denne reaksjonen er representert med ΔH. Det negative tegnet indikerer frigjøring av energi. Reaksjonen er eksoterm.
 Forbrenning av metangass. Reaksjonen manifesteres med en flamme.
Forbrenning av metangass. Reaksjonen manifesteres med en flamme.
Eksempler på forbrenningsvarme av organiske forbindelser ved 25 ° C.
Forbindelse |
Formel |
ΔH (Kcal / mol) |
Metan (g) |
CH4 |
-212.80 |
Etan (g) |
C2H6 |
-372.82 |
Propan (g) |
C3H8 |
-530.60 |
n-butan (g) |
C4H10 |
-687.98 |
n-pentan (g) |
C5H12 |
-845.16 |
Etylen (g) |
C2H4 |
-337.23 |
Acetylen (g) |
C2H2 |
-310.62 |
Benzen (g) |
C6H6 |
-787.20 |
Benzen (l) |
C6H6 |
-780.98 |
Toluen (l) |
C7H8 |
-934.50 |
Naftalen (er) |
C10H8 |
-1,228.18 |
Sukrose (r) |
C12H22ELLER11 |
-1,348.90 |
Metanol (l) |
CH3Åh |
-173.67 |
Etanol (l) |
C2H5Åh |
-326.70 |
Eddiksyre (l) |
CH3COOH |
-208.34 |
Benzosyre (r) |
C6H5COOH |
-771.20 |
For at et drivstoff skal gi all forbrenningsvarmen det er i stand til, må det være i gassform. Som det fremgår av tabellen, bidrar flytende benzen til en forbrenningsvarme som er 6,22 Kcal / mol mindre enn den som frigjøres av gassbenzen. Dette betyr at 6,22 Kcal / mol må investeres for å gjøre overgangen fra væske til gass.
Klikk for mer informasjon om Drivstoff.
Elektrolytiske løsninger Energi
En elektrolytisk leder er et medium der en eller flere ioniske arter er involvert, som er spredt med sin elektriske ladning, slik at en elektrisk strøm kan passere gjennom sin Grunnlov. Elektrolytiske løsninger er elektrolytiske ledere.
Elektrolytiske ledere inkluderer, i tillegg til elektrolyttløsninger, Smeltede salter, og også noen faste salter, slik som natriumklorid NaCl og sølvnitrat AgNO3.
Elektronoverføring skjer ved ionisk migrasjon, positiv og negativ, mot elektrodene. Denne migrasjonen innebærer ikke bare en overføring av elektrisitet, men også transport av materie fra en del av lederen til en annen.
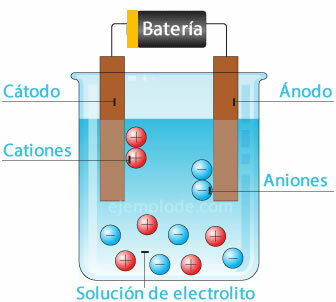 Elektrokjemisk celle
Elektrokjemisk celle
Koble en potensiell kilde til metallelektrodene (katode og anode), og senk disse i en Vandig løsning, elektronene vil bevege seg gjennom anoden for å unnslippe løsningen til den positive polen på fontene. Dette er for eksempel tilfelle med et kloridion, som frigjøres fra elektronet, og som allerede har en nøytral ladning, forbinder det et annet kloratom for å danne det diatomiske molekylet. Klorgass vil rømme fra løsningen.
2Cl- = 2Cl + 2e-
Elektroner som forlater den negative polen til kilden, vil bli plassert i den nedsenkede katoden. Artene som er tilstede i den vandige løsningen (ioner) vil ta elektronene fra katoden. For eksempel tok hydrogenionene som utgjør vann, etter å ha vært i en positiv ladning et elektron som skal nøytraliseres, og sammenføyes med et annet hydrogenatom for å danne molekylet diatomisk. Det vil rømme som hydrogengass fra løsningen.
2H+ + 2e- = 2H
2H = H2 (g)
Denne utvekslingen av elektroner kan støtte driften av bilbatterier, som består av bly Pb-elektroder nedsenket i en løsning av svovelsyre H2SW4.
Den samme energien er oppnådd i alle typer batterier som håndteres på hjemmemarkedet: 9V, AA, AAA, D, for å nevne noen eksempler.
Mat Energi
Mennesker assimilerer energien som frigjøres ved å oppløse maten vi spiser i kroppen vår. Denne energien er det kroppen vår bruker til ikke-bevisste funksjoner (fordøyelse, hjerterytme, mobilfunksjoner) og de som vi utfører.
Så lenge du ikke har intens fysisk aktivitet og stoffskiftet er tregt, anbefales det å ha et regelmessig kaloriinntak fordi mat med høyt innhold Komplekse lipider og karbohydrater, som har veldig store strukturer, er vanskeligere å bryte ned, noe som resulterer i en reversering av Energi. I så fall ville effekten være en motsatt stund.
Det anbefales å konsumere frukt når du må jobbe om natten, fordi frukten inneholder fruktose, et enkelt karbohydrat som er lett å bryte ned og vil ha energi tilgjengelig for deg etter din forbruk.
Kjemisk energi og dens transformasjoner
Termoelektriske anlegg
Tunge drivstoff brukes i termoelektriske kraftverk for å ha en høy og langvarig brennverdi. Generelt er det fyringsolje (fyringsolje). Forbrenning, som er det kjemiske stadiet i prosessen, vil tjene som et oppvarmingsmiddel for en kjele, som vil generere mettet damp. Denne dampen vil komme ut under trykk gjennom dampdistribusjonsnettverket og vil begynne å bevege generatorturbinene. Disse enhetene vil produsere elektrisk energi for å forsyne den tilsvarende befolkningen.
Kjemisk energi → Mekanisk energi → Elektrisk energi
Drift av biler
Biler er avhengige av en strømkilde, som er batteriet. I batteriet er det allerede kjent at elektrolytisk ledning skjer, og driver strøm til tenningssystemet, instrumenttilbehør og ekstra stikkontakter. Takket være denne tilgjengelige strømmen vil bilen kunne bevege seg for å ta sjåføren til ønsket sted.
Kjemisk energi → Elektrisk energi → Mekanisk energi



