Eksempel på organiske og uorganiske molekyler
Kjemi / / July 04, 2021
De Generell kjemi det er vitenskapen som studerer alle typer materier som eksisterer, og deres interne endringer ha kontakt mellom forskjellige typer dette.
De Organisk kjemi er den delen av generell kjemi som skal studere materie hvis hovedbestanddel er Karbonelement, Hva så det er en del av levende organismer.
De Uorganisk kjemi Det er den delen av generell kjemi som har ansvaret for å studere den såkalte "mineralsk materie", som er en del av Jeg lever ikke miljø.
De Molekyl er foreningen av forskjellige atomer av forskjellige elementer kjemikalier for å danne nye stoffer, med sine spesielle egenskaper.
I generell kjemi, Elementer Er det rene stoffer som er dannet av atomer av en enkelt type. Elementene er klassifisert i det periodiske systemet for kjemiske elementer.
Akkurat som han Atom er den grunnleggende enheten til elementene, den Molekyl er hovedenheten til forbindelser, som er stoffer som har en karakteristisk kjemisk oppførsel.
De Forbindelser kan dannes som en konsekvens av naturfenomener
, eller opprettes i laboratorier eller i Industrielle anlegg, så molekyler er til stede overalt. Molekylene er i mineraler, i treblader, i mat, i medisiner, i vannet vi drikker, i luften vi puster, og til og med i forurensningen av miljøet.Generell kjemi er hovedsakelig delt inn i Uorganisk kjemi Y Kjemisktil OrgnicaDerfor kan molekyler også klassifiseres som uorganisk og organisk.
Uorganiske molekyler
I uorganisk kjemi dannes molekyler for det meste av kombinasjon av atomer med positive valenser med andre av negative valenser, i ioniske bindinger. Disse bindingene dannes hovedsakelig av de elektromagnetiske kreftene mellom atomene, generert av tilstedeværelsen av valenselektronene.
Dermed oppstår alle ioniske forbindelser, slik som salter, oksisalter, syrer, oksysyrer, oksider og hydroksider.
Uorganiske molekyler som elektrolytter
Hovedegenskapen til ioniske molekyler er at når de kommer i kontakt med vann H2ELLER, de er skilt i to deler: positive og negative. Disse to delene, elektrisk ladede atomer eller grupper av atomer, er spredt i vannet. Til det uorganiske stoffet som er i stand til å skille seg i vann, det kalles elektrolytt.
Løsningen dannet av vann og positivt og negativt ladede partikler kalles "Elektrolytisk løsning". Denne typen løsning har evnen til å lede elektriske strømmer, og det er derfor den brukes i elektrokjemiske celler, for eksempel bilbatterier.
Uorganisk syre og alkaliske molekyler
Når det gjelder uorganiske molekyler som Syrer, den Oksysyrer og Hydroksider, samtidig som de skiller seg inn i en positiv og negativ del, bidrar de til løsningen en egenskap som heter Hydrogen Potential, målt som negativ logaritme av hydrogenionkonsentrasjon.
De Hydrogenpotensial (pH) bestemmer hvor mye løsningen er sur. På pH-skalaen, som varierer fra en verdi på 1 for maksimal surhet til 14, som er fullstendig alkalinitet eller basalitet, varierer syrekarakteren fra verdiene 1 til 6, og den alkaliske er mellom 8 og 14. 7 representerer nøytral pH; verken sur eller basisk. Resultatet av den negative logaritmen til H + -konsentrasjonen vil fortelle oss hvor vi er på skalaen.
Eksempler på syrer:
Saltsyre: HCl: H+ + Cl-
Hydrobromic Acid: HBr: H+ + Br-
Svovelsyre: H2S: 2H+ + S-2
Cyanhydric Acid: HCN: H+ + CN-
Saltsyre: HI: H+ + Jeg-
Eksempler på oksysyrer:
Svovelsyre: H2SW4: 2H+ + SÅ4-2
Karbonsyre: H2CO3: 2H+ + CO3-2
Salpetersyre: HNO3: H+ + NEI3-
Fosforsyre: H3PO4: 3H+ + PO4-3
Perklorsyre: HClO4: H+ + ClO4-
Eksempler på hydroksider:
Natriumhydroksyd: NaOH: Na+ + OH-
Kalsiumhydroksyd: Ca (OH)2: Ca+ + 2OH-
Ammoniumhydroksid: NH4OH: NH4+ + OH-
Kaliumhydroksid: KOH: K+ + OH-
Magnesiumhydroksid: Mg (OH)2: Mg+ + 2OH-
Uorganiske molekyler i kjemiske reaksjoner
Når uorganiske molekyler deltar i en kjemisk reaksjon, er det fire grunnleggende og enkle reaksjonsmekanismer: Syntese, spaltning, enkel substitusjon og dobbel substitusjon. Her er et eksempel på hver:
Syntese
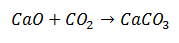
En syntese-reaksjon er en der to molekyler kommer sammen i et sluttprodukt bestående av et enkelt molekyl. I eksemplet er det tilfellet med kalsiumoksyd kombinert med karbondioksid for å danne et kalsiumkarbonatmolekyl.
Nedbrytning:

En nedbrytningsreaksjon er en der et innledende molekyl skilles i to nye stabile molekyler. Slik er tilfellet med kalsiumhydroksid, som skilles i et molekyl av kalsiumoksid og et annet av vann.
Enkel erstatning:

I en enkel substitusjonsreaksjon, et atom av et element byttes ut med et av atomene i et molekyl. Slik er tilfellet med metallisk sink, plasserer seg i stedet for hydrogen i hydrogenklorid, frigjør det og danner sinkkloridmolekyler.
Dobbeltbytte:
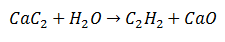
I en dobbel substitusjonsreaksjon, visse atomer av to innledende molekyler byttes ut, for å generere to forskjellige molekyler som produkter. Slik er tilfellet med kalsiumkarbid, som gjennomgår frigjøring av karbon, som vil kombineres med hydrogen fra vann for å danne acetylen. Kalsium vil binde seg til oksygen for å danne kalsiumoksyd som et andre produkt.
Organiske molekyler
Organisk kjemi er karbonkjemi, som betyr at alle organiske molekyler vil ha tilstedeværelse av dette elementet, i forskjellige strukturelle ordninger.
Organiske molekyler er preget av konstant tilstedeværelse av kovalente obligasjoner. Kovalente obligasjoner med de to atomer går sammen for å dele valenselektronene sine og dermed fullføre oktettene sine gjensidig.
Dette er tilfelle med karbon, som binder seg til andre atomer av samme element. Kjeder med svært varierte lengder dannes, fra to til seksti karbonatomer, og til og med disse kjedene de forgrener seg med andre kjeder med samme lengde, og oppnår et enormt mangfold av molekyler organisk.
Joniske bindinger er også til stede, men disse forekommer i mellomtrinn av lange reaksjonsmekanismer der et ønsket molekyl blir dannet.
De enkleste organiske molekylene inkluderer karbon og hydrogen. Sistnevnte fullfører karbonvalensen som krever det.
I organisk kjemi kan molekyler være lineære eller alifatiske, forgrenede, sykliske og aromatiske.
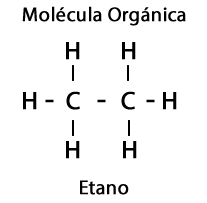
I tillegg er elementene oksygen, nitrogen, svovel og fosfor involvert i organiske molekyler, noe som gir et imponerende mangfold av funksjonelle grupper for molekylene.
Funksjonelle grupper i organiske molekyler
De Funksjonelle grupper er grupper med to eller flere atomer som, når de går sammen med en karbon-hydrogen-kjede, danner forskjellige kjemiske arter, med en spesiell oppførsel. Deretter er de syv hovedtypene av organiske molekyler listet opp, med deres respektive funksjonelle grupper. Bokstaven "R" brukes til å betegne karbon-hydrogen-kjeden.
Alkylhalider - Form: R-X / Funksjonell gruppe: Et halogenelement (klor, brom, jod)

Alkoholer - Form: R-OH / funksjonell gruppe: -OH eller hydroksyl.
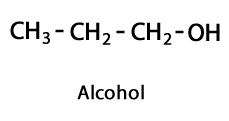
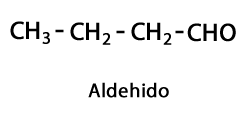
Aldehyder - Form: R-CHO / funksjonell gruppe: -CHO, som alltid går til enden av kjeden.
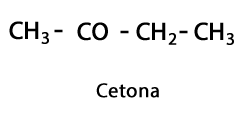
Ketoner - Form: R-CO-R / Funksjonell gruppe: -CO- eller karboksy, alltid i midten av kjeden.
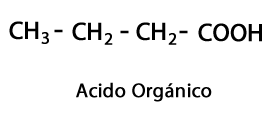
Organiske syrer - Form: R-COOH / funksjonell gruppe: -COOH eller karboksyl, alltid på enden av kjeden.
Syreestere - Form: R-COO-R / Funksjonell gruppe: -COO-, er resultatet av å forbinde en syrekjede med en annen karbon-hydrogen-kjede.
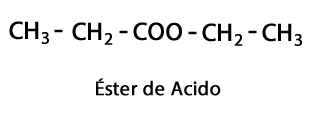
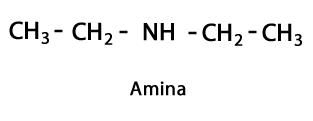
Amines - Form: R-NH2, R-NH-R, R-N-2R / funksjonell gruppe: -NH2, -NH-, -N = eller Amino, som er et nitrogen tilsatt hydrogen på de stedene der det ikke er noen karbon-hydrogen-kjede. Som nevnt kan den gå i enden av kjedet, eller i midten. Nitrogenatomet kan ledsages av en, to eller tre organiske kjeder for å danne et endelig molekyl. Aminer kan betraktes som organiske derivater av ammoniakk NH3.
Organiske molekyler i kjemiske reaksjoner
Organiske molekyler, jo lengre karbon-hydrogen-kjeder, jo flere steder eller atomer tilgjengelig for å delta i en kjemisk reaksjon.
Oftest blir elementer eller kjeder tilsatt til et av karbonene som er tilstede, eller en del av hovedkjeden løsnes for å generere en annen organisk forbindelse fra hverandre.
Ettersom slike reaksjoner er langsomme, brukes katalysatorer, som er kjemiske midler for å akselerere reaksjonene. I noen tilfeller er Catalyst et fint nett av platinametall.
Eksempler på uorganiske molekyler
Natriumklorid NaCl
Kaliumklorid KCl
Ammoniumklorid NH4Cl
Natriumnitrat NaNO3
Kaliumnitrat KNO3
Ammoniumnitrat NH4IKKE3
Svovelsyre H2SW4
Fosforsyre H3PO4
Fosforsyre H3PO3
Saltsyre HC1
Jodvannsyre HI
Natriumhydroksyd NaOH
Kaliumhydroksid KOH
Ammoniumhydroksid NH4Åh
Kalsiumhydroksyd Ca (OH)2
Magnesiumhydroksid Mg (OH)2
Jernholdig hydroksid Fe (OH)2
Jernhydroksyd Fe (OH)3
Jernsulfid FeS
Jernsulfat FeSO4
Ferrisulfat Fe2(SW4)3
Eksempler på organiske molekyler
Glukose C6H12ELLER6
Metan CH4
Etan C2H6
Acetylen C2H2
Propan C3H8
Butan C4H10
Etanol C2H6ELLER
Sukrose C12H22ELLER11
Metanol CH4ELLER
Glyserol C3H8ELLER3



