Eksempel på Charles's Law
Fysikk / / July 04, 2021
Charles gasslov eller lov om konstant trykk, er en annen av gasslovene, bekjentgjort av Gay-Lussac, som ga ut arbeidet til Jacques Charles, publisert rundt 20 år før.
Charles lov forutsier oppførselen til en gassmasse når trykket forblir konstant og temperaturen og volumet varierer.
Charles lov er angitt som følger:
Ved konstant trykk er volumet av en gass direkte proporsjonal med endringen i temperaturen.
Konstant trykk: refererer til det faktum at trykket som gassen utøver på beholderens vegger ikke vil variere gjennom opplevelsen.
Volum: det er det okkuperte rommet gassen opptar, generelt regnes det som en beholder med vegger som ikke deformeres, og hvis lokk fungerer som et stempel.
Temperatur: Det er økningen eller tapet av varme gassen gjennomgår under eksperimenteringen. Hvis temperaturen øker, øker volumet. Hvis temperaturen synker, synker også volumet.
Algebraisk uttrykkes Karls lov med følgende formel:

Hvor:
V = gassvolum
T = gass temperatur
k = proporsjonalitetskonstant for den gassmassen.
Dette betyr at for en gitt masse gass, ved konstant trykk, forholdet mellom volum og temperaturvariasjoner, vil alltid ha samme proporsjonalitetsforhold, representert av konstanten k:

Så når konstanten er bestemt, kan vi beregne noen av de andre verdiene fra andre kjente data:
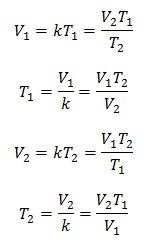
3 Eksempler på Charles's lov gjaldt problemer:
Eksempel 1: Beregn det nye volumet, hvis det i en beholder er en masse gass som opptar et volum på 1,3 liter, ved en temperatur på 280 K. Beregn volumet når du når en temperatur på 303 K.
V1 = 1,3 l.
T1 = 280 K
V2 = ?
T2 = 303 K
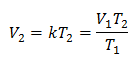
Erstatte verdier:
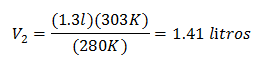
Det nye volumet på 303 K er 1,41 liter.
Eksempel 2. Hvis vi har en gass som opptar 2,4 liter ved 10 grader Celsius, beregner du den endelige temperaturen, hvis den til slutt opptar 2,15 liter.
V1 = 2,4 l
T1 = 10 ° C = 283 K
V2 = 2,15 l
T2 = ?
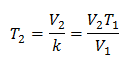
Erstatte verdier:
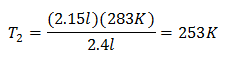
Den nye temperaturen er 253 K, som er lik -20 ° C.
Eksempel 3. Vi har en gass som har en opprinnelig temperatur på 328 K, dens endelige volum er 3,75 l og forholdskonstanten er 0,00885.
V1 = ?
T1 = 328 K
V2 = 3,75 l
T2 = ?
k = 0,00885
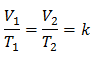
Erstatte verdier:
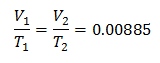
Å vite opprinnelig volum:
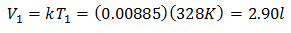
Startvolumet er 2,90 l.
Å vite den endelige temperaturen:
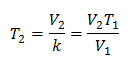
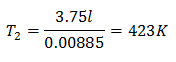
Den endelige temperaturen vil være 423 K, som er lik 150 ° C.



