20 przykładów alkenów
Różne / / July 04, 2021
alkeny Oni są związki zawierające podwójne wiązania węgiel-węgiel. Gdy te związki mają struktury o otwartym łańcuchu, reagują na wzór cząsteczkowy CnieH2n (gdzie nie to liczba atomów węgla). Alkeny nazywane są również olefinami i odpowiadają grupie węglowodory nienasycony. Otrzymywane są głównie w procesie krakingu ropy naftowej oraz poprzez odwodornienie alkanów. Na przykład: eten, propen, cykloheksen.
Są to związki organiczne, które mogą być krótki, średni lub długi łańcuch; istnieją również alkeny cykliczne lub cykloalkeny. Dzięki podwójnemu wiązaniu węgiel-węgiel alkeny mają mniej wodorów niż alkany odpowiadające równej liczbie atomy węgiel.
Jak nazywa się alkeny?
Aby nazwać alkeny, łańcuch węglowy który zawiera największą ilość atomów węgla i który zawiera również podwójne wiązanie. Jeśli ten łańcuch ma kilka podwójnych wiązań, nazywa się je szukając najmniejszej możliwej kombinacji pozycji tych podwójnych wiązań.
Stanowisko podwójne wiązanie Jest to wskazane przez wstawienie przed przyrostkiem -no przedrostka łacińskiego, który wskazuje numer węgla, w którym zaczyna się wiązanie podwójne (di (2), tri (3), tetra (4), penta (5), octa (8) itp.). Podstawniki (zwykle chlor, brom, etyl, metyl itp.) są nazywane przedrostkami (na początku nazwy), szczegółowe i w porządku alfabetycznym, są również nazywane, szukając najmniejszej możliwej kombinacji ich pozycji w łańcuch. Na przykład:
1-buten / 1,2-butadien / 5-chloro-1-penten / chlorek 4-pentenylu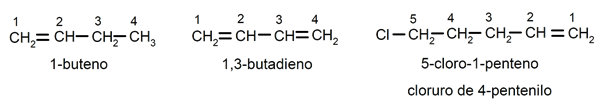
Biorąc pod uwagę, jak złożona nazwa chemiczna ustalona zgodnie z Kryteria IUPACWiele naturalnie występujących organicznych alkenów ma fantazyjne nazwy, często związane z ich naturalnym źródłem. Na przykład: limonen / 1-metylo-4-(1-metyloetenylo)-cykloheksen / geraniol / 3,7-dimetylo-2,6-oktadien-1-ol
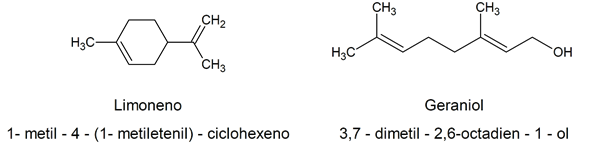
Alkeny zawierające do czterech węgli są gazy w temperaturze pokojowej, te z 4 do 18 węgli Oni są płyny a najdłuższe są solidny. rozpuszczają się w rozpuszczalniki organiczne, takie jak eter lub alkohol i są nieco gęstsze niż odpowiednie alkany (to znaczy mają taką samą liczbę atomów węgla).
Punkt połączenie Tak wrzenie alkenów, podobnie jak w alkanach, wydłuża się łańcuch węglowy.
Z drugiej strony ze względu na napięcie generowane przez podwójne wiązanie, odległość między atomami węgla biorącymi udział w podwójnym wiązaniu w alkenie wynosi 1,34 pm (pikometrów), natomiast odległość pojedynczego wiązania w odpowiednim alkanie wynosi 1,54 po południu
Prezentują reaktywność chemiczna znacznie wyższe niż alkany, właśnie dlatego, że mają te podwójne wiązania, które mają gęstość elektronikę, która jest wysoka i może się zepsuć i umożliwić dodanie innych atomów, często wodoru lub halogeny. Mogą też doświadczyć utlenianie i polimeryzacja.
Zazwyczaj obecne są alkeny izomeria cis-trans lub stereoizomeria, ponieważ atomy węgla połączone wiązaniem podwójnym nie mogą się obracać, co powoduje, że podstawniki znajdują się po tej samej stronie wiązania podwójnego lub po przeciwnych stronach. Na przykład: trans-2-buten / cis-2-buten
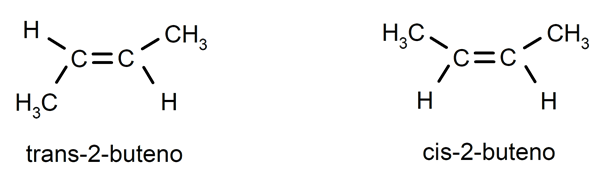
Alkeny z dwoma wiązaniami podwójnymi nazywane są dienami, a te z więcej niż dwoma wiązaniami podwójnymi są ogólnie nazywane polienami.
W świecie roślin alkeny są dość obfite i mają role fizjologiczne bardzo istotne, takie jak regulacja procesu dojrzewania owoców czy filtrowanie niektórych promieniowania słonecznego.
Struktura chemiczna organicznych alkenów jest zwykle dość złożona i obejmuje łańcuchy i pierścienie węglowe. Niektóre owoce (takie jak marchewka lub pomidory) i niektóre skorupiaki (jak kraby) wytwarzają znaczne ilości beta-karotenu, ważnego alkenu, który jest prekursorem witaminy A.
Przykłady alkenów
- eten
- 2-metylopropen
- propen
- 2,3-butadien
- mircen
- limonen
- geraniol
- likopen
- lanosterol
- mentofuran
- tetrafluoroetylen
- 1,3,5,7-cyklooktatetraen
- 5-bromo-3-metylo-3-heksen
- 3,5-dietylo-4-propylo-2,5-dimetylo-2-hepten
- 7,7,8-trimetylo-3,5-nonadien
- 3,3-dietylo-1,4-heksadien
- cykloheksen
- 1-chloro-2-metyloprop-1-en
- 3-bromo-5-metylo-cyklopenten
- 1-metylo-cykloheksen
Schematy związków chemicznych tych alkenów:




